Nature | 中国科学院化学研究所乔燕、王树合作团队在人工细胞不对称分裂领域取得重要进展
研究背景
人工细胞的可控分裂是模拟细胞行为的关键挑战。目前,研究人员可通过蛋白质机器介导、外部剪切、光刺激、离子强度调节和热流等手段,调控膜张力、膜流动性和渗透压,从而诱导囊泡分裂;也可通过热梯度、耗散自组装、浸润能及化学反应等机制,实现乳液和凝聚液滴体系中的对称分裂行为。相比之下,细胞的不对称分裂是生命体系实现细胞分化、发育和功能多样化的重要基础。然而,这一过程因涉及复杂的时空调控与结构重构机制,难以在人工细胞体系中复现。
成果略影
在国家自然科学基金委、中国科学院和北京分子科学国家研究中心的支持下,化学研究所高分子物理与化学实验室乔燕课题组围绕人工细胞的构筑及其类细胞行为开展研究,取得了系列研究进展(Nat. Chem.2024, 16, 158-167; Nat. Chem.2025, 17, 986-996; Nat. Commun.2025, 16, 10554; J. Am. Chem. Soc.2025, 147, 45004-45014.)。
最近,乔燕、王树研究员合作团队联合国内外科学家,在国际学术期刊《自然》(Nature)上发表题为“Asymmetric splitting in dividing lipid-nucleotide multilamellar droplets”的研究论文。研究团队提出了一种基于瞬态化学不均匀性和界面能梯度驱动人工细胞不对称分裂的新思路,构筑了具备不对称分裂潜能的结构化液滴人工细胞模型,实现了母代人工细胞自发分裂为内核液滴和外壳囊泡两种形态与性能不同的子代。
研究团队构筑了一种由脂质分子与核苷酸自组装形成的层状液晶液滴人工细胞模型。在碱性磷酸酶催化下,液滴表面首先形成一个局部凹陷;随着酶催化反应持续进行,凹陷沿液滴表面周向逐渐扩展,同时液滴形成清晰的外壳—内核界面。当凹陷张开角度达到临界值,液滴内核被完整“挤出”,剥离后的外壳则通过边缘弛豫闭合,形成具有内水相的多层囊泡结构。最终,一个母代液滴分裂形成两个结构、组成和性质显著不同的子代结构。研究结果表明,酶主要富集于液滴表面,其催化的去磷酸化过程可导致液滴层间距增大并引发结构失稳。在非酶条件下,多价离子介入或pH变化同样能够触发液滴分裂,这不仅证明了静电屏蔽作用是不对称分裂的核心驱动力,也表明该分裂机制具有较好的普适性,其本质来源于瞬态化学不均匀性与界面能梯度的协同作用。此外,层状液晶结构及其层内微小结构缺陷对液滴分裂至关重要,而内部无序的液滴则仅表现为均匀解体。进一步研究发现,分裂后的子代液滴能够保留酶活性和分子浓度,而子代囊泡由于持续的去磷酸化,内部结构逐渐疏松并释放部分分子,pH也随之降低。这说明不对称分裂能够在子代体系中形成差异化化学微环境,从而为后续功能分化提供基础。该研究不仅为理解生命功能涌现提供了新的实验模型,也为构筑具备自主增殖、分化和演化能力的高复杂度人工细胞体系奠定了基础。
相关研究成果近日发表于Nature期刊(Nature 2026. DOI: 10.1038/s41586-026-10489-5),论文共同第一作者为化学研究所孟何和贾丽艳,通讯作者为化学研究所乔燕研究员、王树研究员、北京化工大学林艺扬教授、英国布里斯托大学Stephen Mann教授。化学研究所邱东研究员作为论文合作作者为小角/广角X射线散射实验提供了重要支持。该研究工作得到了化学研究所工程塑料实验室(SAXS/WAXS)和怀柔研究中心(STED超高分辨显微镜系统)的技术支撑。
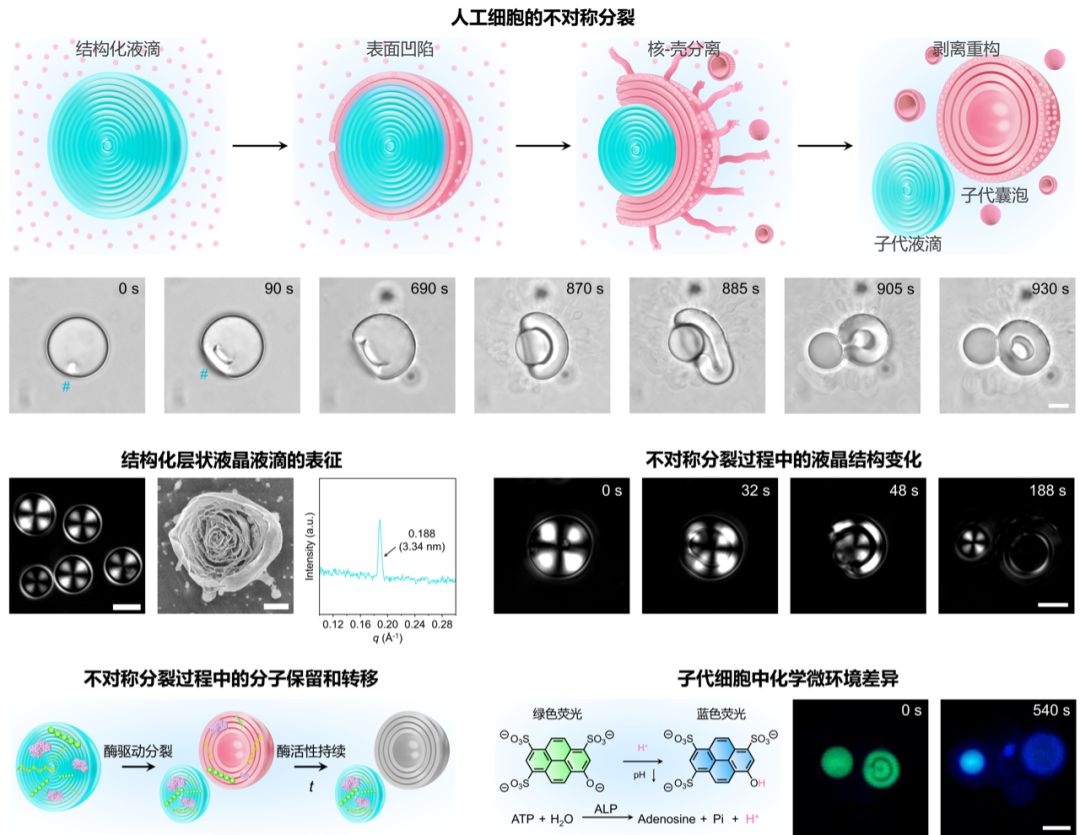
▲ 液晶液滴人工细胞的不对称分裂
