中国团队首创乳腺癌血液诊疗新范式:一管血同步实现极早期筛查、分子分型与淋巴结转移的超高灵敏度预测

在威胁全球女性健康的恶性肿瘤中,乳腺癌始终高居发病率榜首。尽管现代医学已取得长足进步,但“早发现、早治疗”这一朴素的生存法则,在现实中仍面临严峻挑战。统计数据显示,中美两国在乳腺癌诊断分期上存在显著差异:美国仅有约 11.8% 的患者在确诊时已处于晚期,而中国这一比例高达 24.1%。
在乳腺癌筛查领域,超声和钼靶是目前应用最广泛的传统影像学手段,但两者均存在一定的技术局限性。钼靶基于 X 射线成像,在亚洲女性普遍具有的致密性乳腺中,微小病灶容易被遮蔽,漏诊率可能达到 50% 以上。而超声检查高度依赖形态学改变和医生的经验水平,对于尚未形成典型肿块的早期病变,难以作出客观统一的判断。
目前液体活检的主流方向——基于 ctDNA 突变位点的检测和基于甲基化的泛癌筛查,在乳腺癌早筛中表现亦不尽如人意。前者在早期人群中的检出率不足 20%,后者则在乳腺癌上的特异性有待提高。
因此,临床急需一种非侵入性、可规模化推广的底层技术方案,以填补现行筛查体系的“真空地带”。
近日,浙江大学医学院附属第二医院、奥明星程等中心合作在 Nature Communications 上发表了最新研究成果。该研究基于奥明星程自主研发的 TuFEst® 模型,可专门识别游离 DNA 的碎片特征(cfDNA 片段组学)。仅需少量血液,即可在一次检测中同步实现乳腺癌的极早期检测、分子分型及淋巴结转移评估。
“片段组分析的核心思路在于通过广度覆盖来弥补深度不足的问题。该方法采用全基因组测序,不局限于特定突变点,而是全面捕捉 cfDNA 在片段大小、末端序列、断裂模式等方面的整体特征。通过构建专门针对乳腺癌的早筛模型,在方法学上具有创新性。”这项研究的通讯作者之一,浙江大学医学院附属第二医院研究员、博士生导师倪超告诉 DeepTech。
解码 cfDNA 的“碎片规律”
细胞游离 DNA(cfDNA)是存在于血液、尿液等体液中无细胞保护的游离核酸片段,主要来源于细胞凋亡、坏死或主动释放。它作为一种非侵入性“液态活检”工具,广泛应用于癌症筛查、肿瘤疗效监测、无创产前诊断及器官移植后排异分析。
在 cfDNA 的碎片特征上,正常细胞与乳腺癌细胞呈现出显著的本质差异,同时乳腺癌不同分子分型的 cfDNA 也带有独特的亚型特异性碎片“指纹”。
具体而言,正常细胞凋亡释放的 cfDNA,其碎片化图谱高度一致、排列规整,核小体定位与转录因子结合位点无异常,4bp 末端基序、6bp 断点基序及 Alu、LTR 等重复元件的频率也保持稳定;而乳腺癌细胞的 cfDNA 则表现出明显紊乱的碎片化特征,且肿瘤分期越高,碎片化异常越显著,还存在特异性的末端基序、断点基序变异与重复元件频率改变,同时因表观遗传重编程,出现与乳腺癌相关的转录因子结合位点碎片化异常,这一差异在 I 期早期乳腺癌中即可被检测到。
因此,TuFEst® 模型可以通过读取这些碎片规律,实现乳腺癌的早筛。
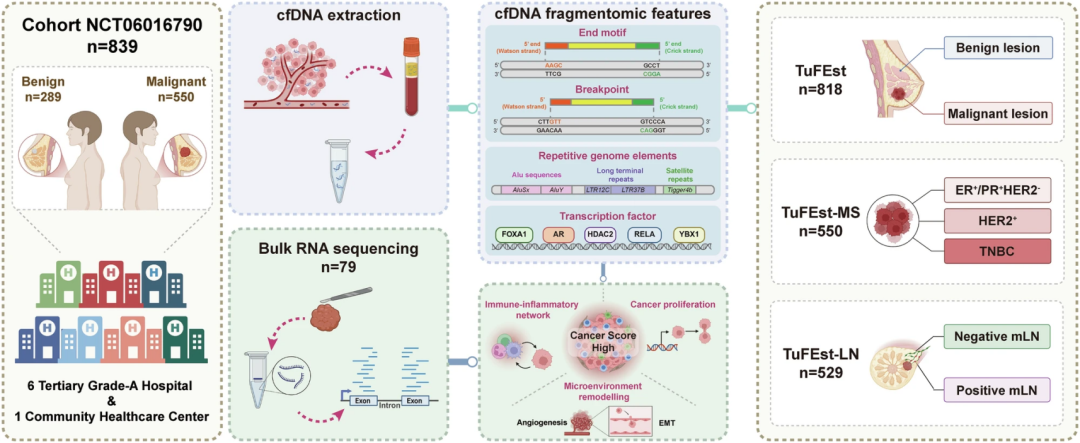
图 | 乳腺癌筛查中 cfDNA 片段组学分析的研究设计和队列特征(来源:上述论文)
在这项研究中,团队分析了 503 例乳腺癌患者和 289 例良性对照者的样本。不同于仅关注基因突变的常规方案,研究团队对患者血浆中的 cfDNA 进行低深度全基因组测序,并深度分析 DNA 片段长度、断裂位点和序列特征等多维度信息,实现了在极低成本下对肿瘤微弱信号的“高信噪比”提取,使大规模人群筛查成为可能。
结果发现,TuFEst® 模型在区分乳腺癌与良性病变方面表现卓越。在训练集和验证集中,其检测灵敏度分别达到 95% 和 92%,特异性分别为 78% 和 87%。
尤为重要的是,在 26 例被超声和钼靶均判定为良性(BI-RADS 3 级)、但后续病理证实为恶性肿瘤的影像漏诊病例中,TuFEst® 模型成功识别出其中 25 例,灵敏度高达 96.2%,且全部为早期或无淋巴结转移的肿瘤。表明该技术能有效弥补现有影像学筛查的不足,显著降低漏诊风险。
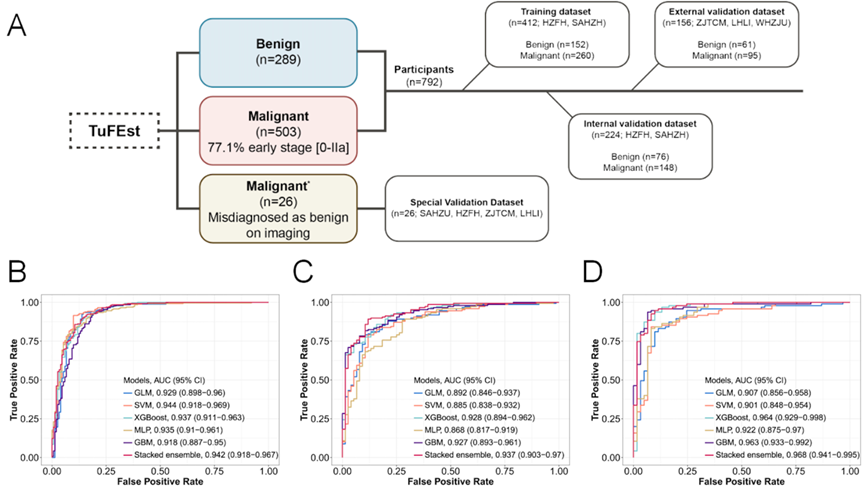
图 | TuFEst® 模型在乳腺癌检测中的性能(来源:上述论文)
对于乳腺癌不同分子分型而言,不同亚型的 cfDNA 在末端基序、断点基序、拷贝数变异相关特征及重复元件分布上,均存在可被精准识别的亚型特异性模式。
基于此,团队进一步开发了分子分型判定模型 TuFEst-MS,仅凭血液 cfDNA 数据,即可高精度区分管腔型(ER+/PR+/HER2-)、HER2+型和三阴性乳腺癌(TNBC)。甚至在 21 例已发生转移的患者中,该模型预测转移灶分子分型的准确率也达到 85.7%,为监测肿瘤进化与方案调整提供了无创化的“实时向导”。
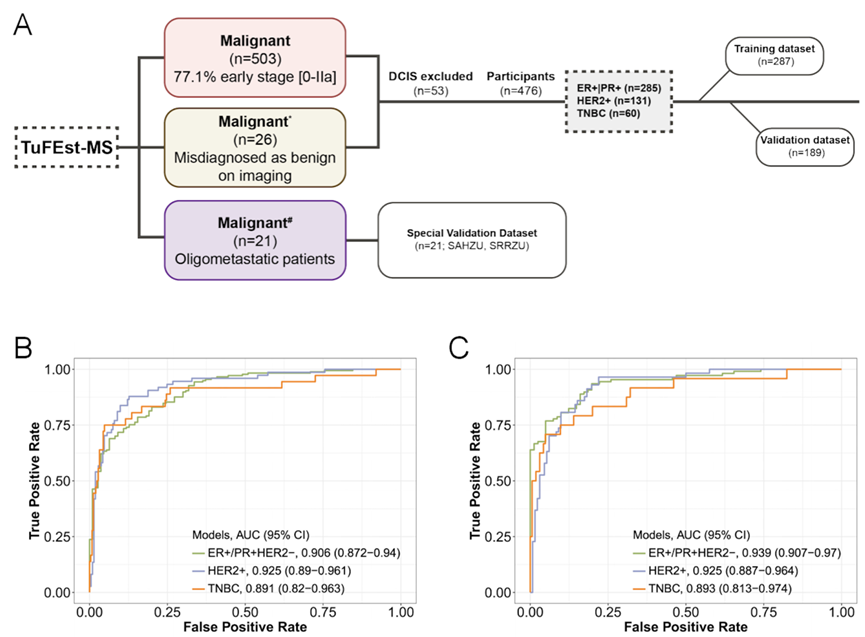
图 | 使用 TuFEst-MS 进行非侵入性分子分型(来源:上述论文)
腋窝淋巴结是否转移是决定治疗方案的关键。传统的影像学评估准确性有限,常导致不必要的淋巴结清扫或治疗不足。
团队开发的腋窝淋巴结转移预测模型 TuFEst-LN 在一个独立的、影像与病理结果不符的挑战性病例组中,对影像阳性但病理阴性患者的阴性预测值高达 97.6%。这一结果意味着,该技术未来有望帮助更多临床评估淋巴结阴性的患者避免不必要的腋窝手术,从而实现更加精准的“降阶梯”治疗。
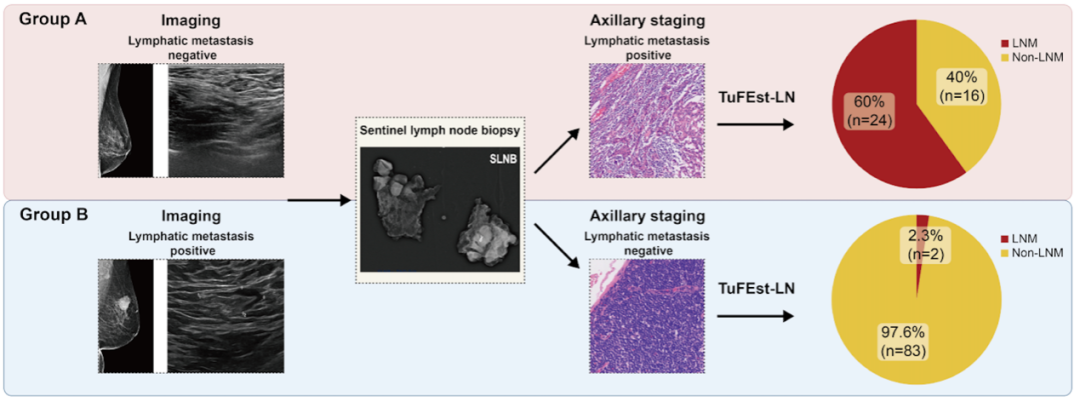
图 | 使用 TuFEst-LN 预测淋巴结转移(来源:上述论文)
“TuFEst® 之所以能实现检测、分型、预判转移,并非依靠单一模型解决所有问题,而是源于其方法学强大的可扩展性。”
倪超解释道,由于研究采用了全基因组测序,在数据采集阶段,团队并不针对某一特定临床问题,而是全面捕捉 cfDNA 数千个维度的片段组特征。在这一庞大的底层数据基础上,可以针对不同的临床任务分别构建专门的预测模型。
只要底层数据足够丰富,后续可以根据临床需求持续开发和迭代新的模型。倪超表示:“未来如果积累了足够多的随访数据,发现部分受试者罹患其他癌症,我们同样可以基于现有的 cfDNA 数据重新建模,探索其对肺癌等其它恶性肿瘤的预测能力。”
补充现有筛查方案
针对液体活检领域普遍关注的假阳性问题,如血栓、系统性红斑狼疮等自身免疫性疾病是否会干扰检测结果,倪超持严谨客观的态度。
他表示,理论上这些疾病确实可能产生类似的 cfDNA 碎片特征。因此,在目前的模型构建和临床研究入组中,团队设定了严格的筛选标准,暂时剔除了以下人群:处于急性感染期的患者、近期有过输血史或大型手术史者、患有自身免疫性疾病者以及妊娠期女性。
“没有任何一项临床研究是完美的,我们采取的是‘分步走’的策略。”倪超指出,TuFEst® 模型目前的重点是解决 90% 以上核心人群的筛查需求。虽然目前的模型尚未泛化到能完全排除所有复杂特殊疾病的干扰,但由于这类特殊病例在普通筛查人群中占比极低,并不影响技术在主流受众中的应用价值。先解决共性问题,再通过后续数据积累逐步攻克复杂疾病状态下的预测效能,是团队未来持续迭代的方向。
尽管 TuFEst® 模型在实验数据中表现卓越,但对于临床医生而言,衡量一项技术成败的最终标准在于它能否实质性地改变诊疗决策。
倪超表示,该模型对临床决策的帮助目前正通过后续的前瞻性研究进行严谨验证,而其中的“重头戏”就在于评估其对腋窝淋巴结转移状态的预测能力,尤其是能否准确筛选出那些真正没有淋巴结转移的患者。
目前,超声、钼靶等手段对淋巴结转移的阴性预测值一般在 0.7-0.8 左右,若该模型能将其提升至 0.9 以上,将实现里程碑式的跨越。这意味着,对于预测为淋巴结阴性、且预后较好的 Luminal 型患者,未来有望豁免有创的腋窝淋巴结活检或清扫。甚至对于经过新辅助治疗达到病理缓解的患者,也能基于此结果减少手术创伤,大幅改善术后生活质量。
访谈的最后,倪超直言,在临床场景中,cfDNA 片段组模型并非要替代超声或钼靶,而是作为补充工具辅助风险分层。针对影像学检出的结节,结合液体活检结果,医生能更准确地判断哪些可以安全随访、哪些需积极干预。这在有效降低漏诊率的同时,也避免了大量不必要的有创检查。
目前,基于现有成果,团队已经在文章投稿阶段同步启动了后续多项临床研究。部分研究已接近尾声,其余工作正在有序推进中。这些研究将进一步验证该模型在分子分型、淋巴结转移状态预测等方面的实际临床性能,为其未来在临床场景中的应用提供数据支持。
奥明星程是一家立足 AI for Science(AI4S)底层范式,基于大模型的个体健康趋势预测及疾病干预的人工智能科技企业。公司由三位哈佛大学青年博士科学家联合创立,始终以 AI 为核心引擎,推动 AI 与生命科学前沿融合,打造支撑生物医药上下游产业链的战略级核心平台,为新质生产力发展与全球科技创新提供范式引领与底层支撑。已参与承担国家人工智能创新高地建设任务、国家科技重大专项(“四大慢病”专项)、浙江省重大科技专项、深圳市重大项目等多层级项目,累计布局 60 余项知识产权,2 项行业标准制定等。目前,公司已获得超亿元 A 轮战略融资,投资方包括深创投、复星医药(复健资本)、中国太平、广东中医药大健康基金(国开金融与恒健控股联合设立)、杭实集团等多家知名产业资本与政府投资基金,并与包括深圳湾实验室在内的多家国际顶尖科研机构建立了深度成果转化合作机制,形成覆盖技术研发、临床应用及产业生态赋能的全链条布局。
浙江大学医学院附属第二医院是中国及浙江省西医发源地、全国首家三甲医院,拥有 10 余个国家级平台,连续六年跻身全国三级公立医院绩效考核第一方阵,“自然指数”居全球医疗机构第 25 位,国家自然科学基金获批数连续 5 年全国第 2、15 年领跑,是 G20 杭州峰会和杭州亚运会核心医疗保障单位,获中国质量奖等荣誉。汇聚院士等高层次人才数十人,建有国内最大规模基础到临床完整科研链,首创“医-学-政-企”机制,获国家科技进步奖 9 项,临床核心指标全国领先,是国内效率最高的大型公立医院之一和“互联网+医疗”先行者。
参考链接:
1.Zhu, Y., Zheng, S., Shao, Y.et al. Fragmentomic liquid biopsy enables early breast cancer detection, molecular subtyping and lymph node assessment. Nat Commun 17, 2276 (2026).
2.https://zucc.zju.edu.cn/2020/1105/c54377a2214627/page.htm
3.https://www.thermofisher.cn/blog/accelerating-science-in-china/cfdna-vs-ctdna/
排版:胡巍巍
