Cell子刊 | 打破胃癌发生的认知!口腔细菌“离家出走”到肠道,竟是胃癌的“隐藏帮凶”!

胃癌在全球癌症发病率和癌症相关死亡率中均位列第五[1]。东亚地区疾病负担尤为沉重,尤其是中国。全球超过一半的胃癌患者在中国[2],每年新发病例约为68万例,大部分患者诊断时已为进展期胃癌[3]。
尽管幽门螺杆菌(Helicobacter pylori, Hp)作为I类致癌物早已被学界公认,但仅有不到5%的幽门螺杆菌感染者会发展为胃癌[4]。这一现象提示,除Hp之外,还有其他微生物因素在胃癌的发生发展中扮演着重要角色。然而,这些非Hp微生物究竟如何影响胃癌,学界仍在探索之中。

图片来源:Cell Reports Medicine
近日,上海交通大学医学院附属仁济医院房静远院士团队联合华大基因科研团队,在国际医学期刊Cell Reports Medicine上发表了重要研究论文,这也是该团队在Gut论文[5]发表后的又一重大进展。(点击文末“阅读原文”,查看研究原文)
研究团队发现,在胃癌患者的肠道中,有一群原本属于口腔的产乳酸菌“离家出走”并在肠道定植,不仅形成共生网络,还通过异常的乳酸代谢推动胃癌进展。这项研究不仅揭示了“口腔-肠道菌群轴”在胃癌中的关键作用,更为胃癌的无创早期筛查和精准干预提供了全新的生物标志物。
肠道里的“不速之客”:
口腔菌株的跨界迁移
为了找出与胃癌相关的特定细菌,研究人员对317例个体、404份粪便与唾液样本进行高精度宏基因组测序。结果显示,与慢性胃炎患者相比,胃癌患者肠道中共有28种细菌存在显著差异。其中23种细菌在胃癌患者的肠道中显著富集,5种则呈现减少趋势。进一步分析发现,胃癌患者肠道中富集的这23种菌种里,有20种都是既能在口腔、又能在肠道检测到的“共享物种”。
这些细菌真的是从口腔“搬家”到肠道的吗?研究团队接着对87例配对的唾液-粪便样本进行了菌株水平分析。他们比较了同一个体中口腔和肠道中同一种细菌的基因相似度(群体平均核苷酸一致性,popANI)。结果显示,对于8种链球菌,在同一个体的口腔-肠道配对样本中,42%至83%的比较显示出极高的遗传相似性(popANI>99.9%)。这为“口腔-肠道传播”提供了直接证据。
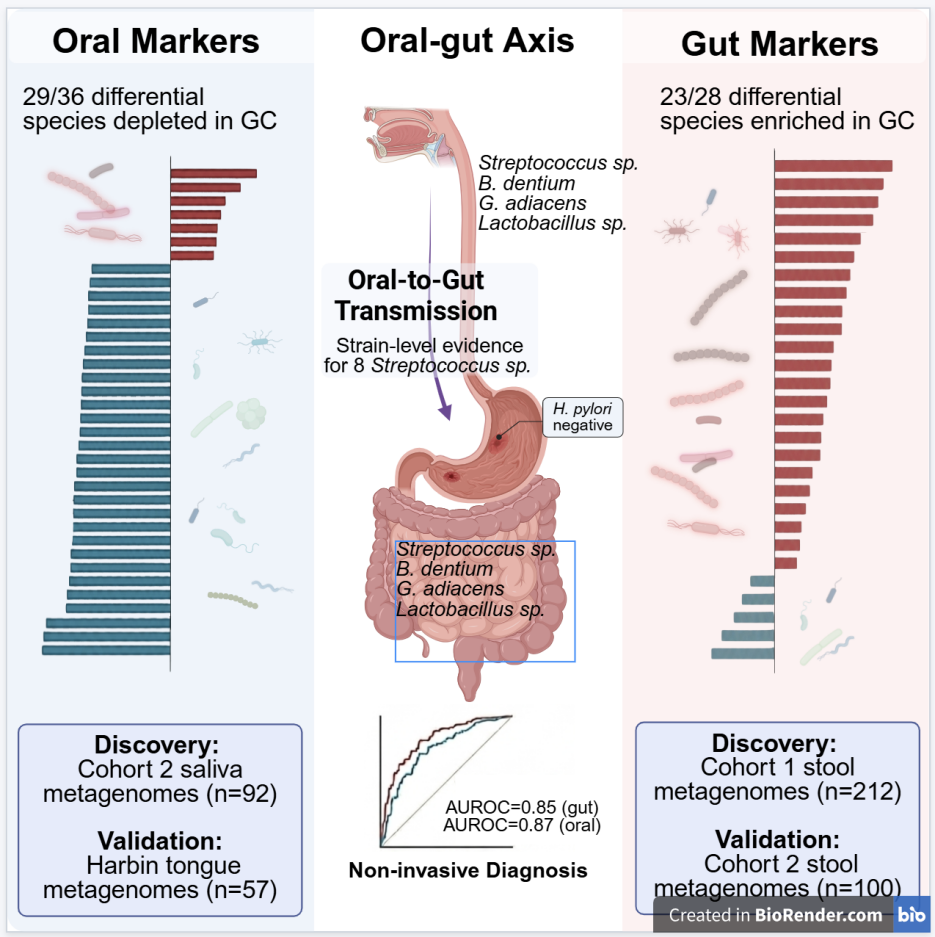
文章摘要
口腔来源的链球菌是
胃癌肠道菌群失调的主角
进一步研究发现,在胃癌患者肠道中富集的23种微生物中,有8种属于链球菌属(Streptococcus),其中咽峡炎链球菌(Streptococcus anginosus, Sa)与胃癌的关联最为强烈。
除了链球菌,研究人员还发现,胃癌患者肠道中富集的物种多为产乳酸菌(lactic acid bacteria, LAB),包括多种乳杆菌(Lactobacillus)和双歧杆菌(Bifidobacterium)。这些产乳酸菌之间存在紧密的共丰度网络,暗示它们可能通过协同作用,在胃癌患者的肠道中形成一个“促癌联盟”。
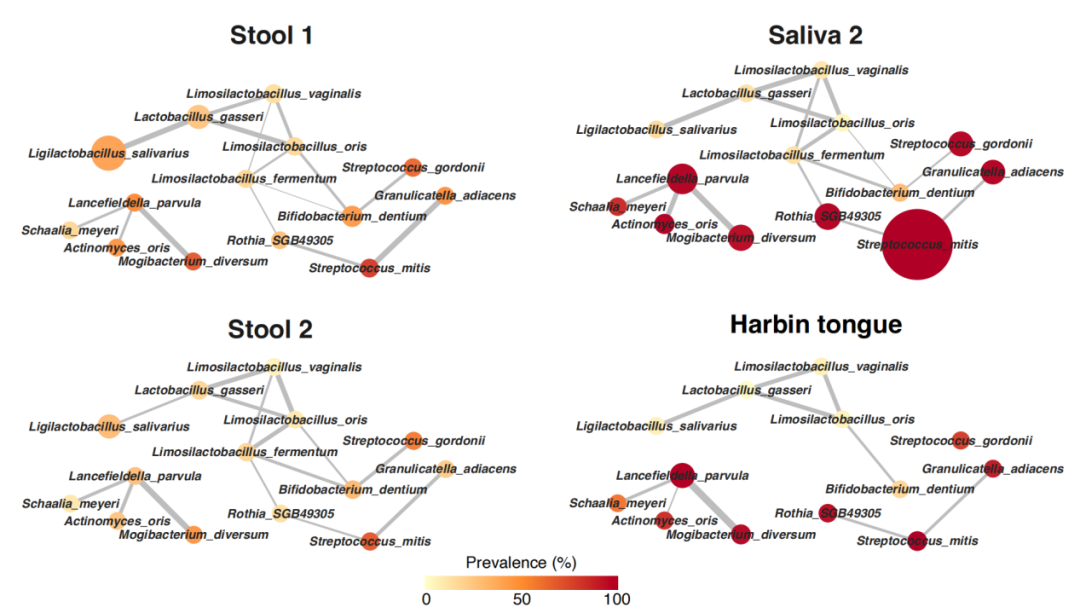
胃癌富集型“口腔-肠道”共享菌种的共丰度网络
更为关键的是,功能分析显示,胃癌患者粪便中同型乳酸发酵和异型乳酸发酵通路显著富集。特别是异型乳酸发酵通路中的所有7种关键酶,包括磷酸酮醇酶和乳酸脱氢酶,均在胃癌组中显著升高。这一发现与胃癌患者胃液中乳酸水平升高的临床观察相吻合。
在此基础上,研究首次描绘了胃癌患者从口腔到肠道的完整微生物组图谱,揭示了“口腔-胃-肠道”连续性的菌群失调轴。以上发现,与经典的“启动子-促进子”(initiator-promoter)胃癌发病模型假说吻合:
1.启动子(幽门螺杆菌): Hp的慢性感染作为“启动子”,引发了黏膜损伤、炎症、萎缩,深刻破坏了胃部的微环境和生态屏障,创造了一个低酸的“宽松”环境 。
2.促进子(乳酸菌): 那些“离家出走”的口腔乳酸菌作为机会主义者,趁机在受损的微环境中定植,并通过形成生物膜、大量产酸以及免疫调节等机制,继续协同甚至独立地促进胃癌的进一步发展。
这一假说解释了为什么很多Hp阴性的患者依然会得胃癌,以及为什么根除Hp后仍存在残余的患癌风险。这为理解Hp阴性胃癌的发病机理提供了新思路。
从机制到转化:
预测模型与临床新方向
研究团队基于这组微生物标志物开发出新的预测模型,在区分胃癌与慢性胃炎方面表现出高准确率(粪便标志物的模型预测准确率达到0.85;基于唾液标志物的模型预测准确率则达到0.87),为胃癌的无创风险分层和早期预警提供了有力工具。
另外,口腔唾液/舌拭子模型的表现优于肠道(粪便)模型,这暗示着口腔微生物的改变可能发生得更早或更显著。口腔唾液采集完全无创、患者依从性极高,极有希望转化为胃癌的高性价比早期筛查工具;同时,本研究为破解临床“Hp阴性胃癌”病因学难题提供了新方向,未来靶向阻断“口-肠菌群轴”或特异性清除致病菌,可能成为肿瘤预防与辅助治疗的新策略。更重要的是,该研究结合了“哈尔滨消化道肿瘤和四高筛查”民生项目的数据,相关发现在哈尔滨项目中得到验证,是一个“民生+科研”的典范。
这项大规模的宏基因组研究首次以“菌株级”极高分辨率实锤了胃癌标志微生物的“口腔溯源”及其传播路径,不仅清晰描绘了胃癌在“口腔-肠道”轴上的微生物生态景观,更重塑了我们对非Hp细菌在胃癌中作用的传统认知,为未来胃癌的非侵入性精准诊断(尤其是唾液活检)及微生态靶向干预奠定了坚实的科学基础。
上海交通大学附属仁济医院消化科周澄蓓副研究员、房静远院士和深圳华大基因覃友文博士为通讯作者。深圳华大基因覃友文博士、仁济医院张雅暄医师(现任职北京中日友好医院)和深圳华大基因刘莉萍博士为该论文共同第一作者。该成果获得了多项国家自然科学基金、上海市“启明星”、上海市“东方英才”等项目的支持。
*研究严格遵守科研伦理规范,已通过伦理审查和人类遗传资源行政许可,原始样本、数据保留在中国境内。
*点击文末“阅读原文”,查看研究原文
参考资料:(滚动查看)
关注我们!获取公司最新资讯!




