首项临床数据出炉!强生软组织手术机器人

2026年5月5日,强生在美国代谢与减重外科学会(ASMBS)年会上公布了其手术机器人Ottava的首项人体临床研究(FORTE研究)结果。这是Ottava自2020年首次公开以来,第一次披露正式临床数据。该研究在30例Roux-en-Y胃旁路手术患者中达到了主要安全性和性能终点,所有手术均以机器人方式完成,无一例中转非机器人术式。术后30天,患者平均减重约30磅。
强生已于2026年1月向FDA提交审批申请,目标适应症覆盖上腹部多个普外科术式,包括胃旁路术、胃袖状切除术、小肠切除术及食管裂孔疝修补术。
# 产品架构:围绕手术室空间约束做文章
Ottava的核心设计特征是将四条机械臂集成于标准尺寸手术台中,机械臂不使用时收纳于台面下方,强生将其描述为"隐形设计"(invisible design)的统一架构。这一设计直接指向当前手术机器人推广中的一个现实瓶颈——手术室空间限制。
FORTE研究的数据提供了一组具体参照:6家参与医院的手术室面积从243平方英尺(约22.6㎡)到694平方英尺(约64.5㎡)不等;其中5家医院的手术在此前从未用于机器人手术的手术室中完成,这些手术室此前被认为因空间限制而"不适合"机器人系统进入。
这组数据的意义在于:如果Ottava确实能在22.6㎡的手术室中完成减重手术,这将显著低于达芬奇系统通常所需的手术室面积门槛。达芬奇Xi的患者侧推车(patient cart)需独立占地并进行对接,对手术室面积的实际要求通常在400平方英尺(约37㎡)以上。Ottava的台式集成方案在物理层面取消了独立推车,理论上可降低对手术室面积和布局调整的要求。
# 竞争格局:多平台竞逐,各处不同阶段
Ottava的临床推进发生在软组织手术机器人赛道加速拥挤的时间窗口中。达芬奇系统长期主导该市场,但过去两年中多个新平台相继进入或逼近商业化阶段。
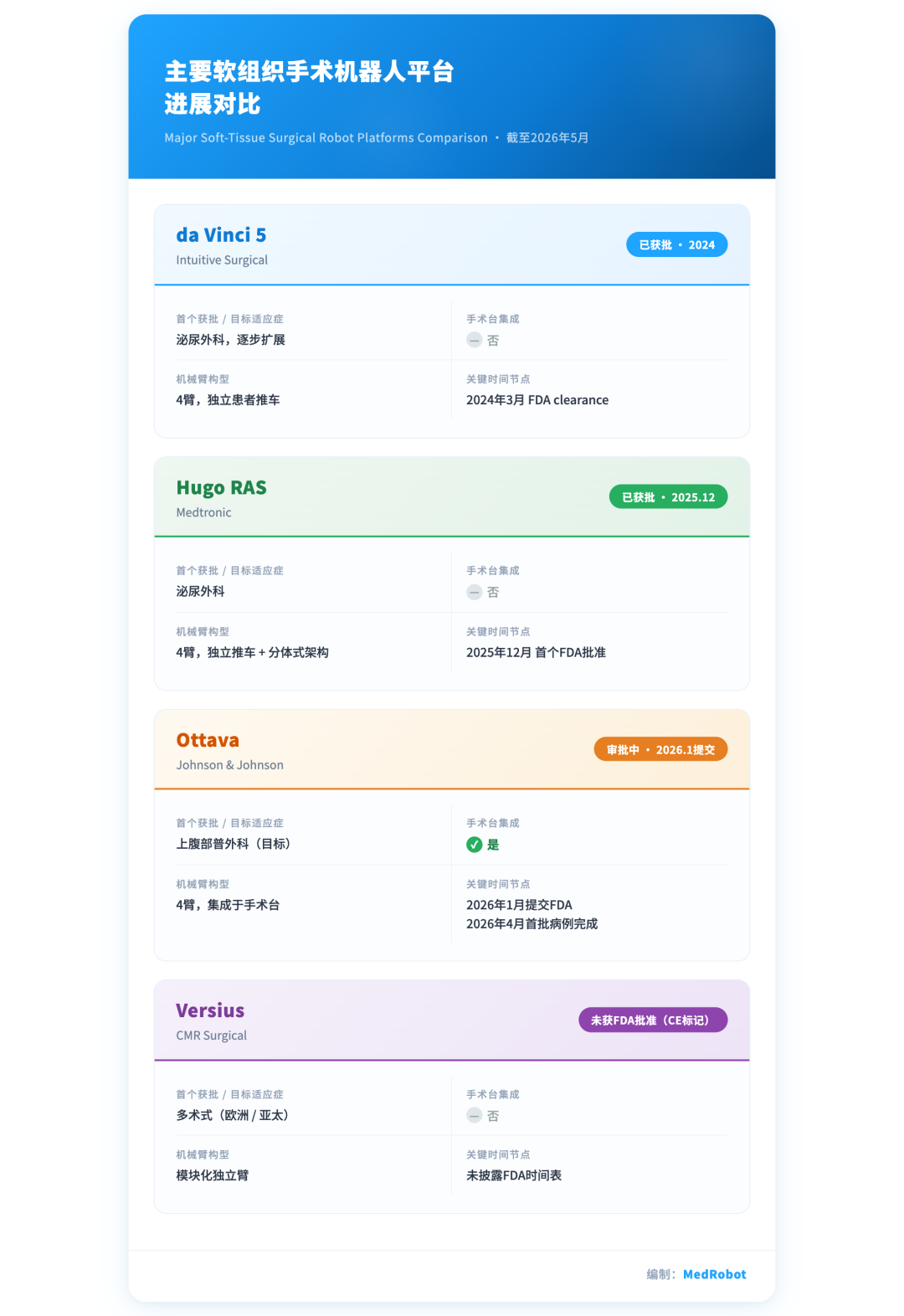
几个值得关注的差异点:
适应症切入策略不同。 Medtronic Hugo首个FDA批准落在泌尿外科——这是达芬奇装机量最大、临床证据最成熟的领域,属于正面竞争。强生Ottava选择以减重/普外科切入,避开了泌尿外科的直接对垒,而减重手术目前正处于需求增长期(GLP-1药物渗透带来的手术量变化尚存争议,但减重手术总量在2024-2025年仍维持增长)。
架构差异决定了商业叙事的不同侧重。 Hugo强调模块化和开放生态;Ottava强调手术台集成带来的空间适应性;da Vinci 5则在已有庞大装机基数上迭代性能和力反馈。三者分别指向不同的医院采购决策痛点。
# 时间线回溯:一个延迟了两年的项目
Ottava的开发节奏值得梳理。2020年首次公开时,强生将其定位为挑战达芬奇的核心产品。但2021年末,公司以"多重因素"为由将开发时间线推迟约两年,期间几乎未对外披露进展。直到2024年10月提交IDE申请,同年11月获FDA批准启动临床,2026年1月提交de novo申请,4月完成首批病例——从IDE获批到提交上市申请,间隔仅约14个月,推进节奏明显加快。

De novo审批路径本身也透露信息:这意味着FDA将Ottava视为无现有对等产品(predicate device)的新型器械分类,而非通过510(k)路径参照达芬奇等已有产品。这一分类可能与其手术台集成架构有关,也意味着审评周期和要求可能不同于传统路径。
# 结语
FORTE研究30例的样本量属于早期可行性/关键性研究的典型规模,足以支撑安全性和基本性能信号,但不足以进行与现有术式的比较分析。研究未设对照组(如腹腔镜或达芬奇辅助的同类手术),术后30天的随访窗口也仅覆盖围手术期安全性,尚未涉及中长期减重效果和并发症数据。
此外,强生提及Ottava未来将整合Ethicon器械及Polyphonic数字生态系统,但目前未披露具体整合时间表和功能细节,这部分信息仍停留在战略愿景层面。
FDA对申请的审评决定将是Ottava商业化进程的下一个关键节点。根据审批的历史周期,决定通常在提交后数月至一年内作出,但强生未披露预期获批时间。
知名手术机器人整机公司及上下游企业
综合▌微创机器人 | 佗道医疗 | 直观复星 | 威高
腔镜▌精锋医疗 | 思哲睿智能医疗 | 康诺思腾
骨科▌罗森博特 | 元化智能 | 长木谷 | 鑫君特| 史赛克
血管介入▌爱博合创 | 唯迈医疗
穿刺机器人▌真健康 | 惟德精准
手术机器人工具▌良医

