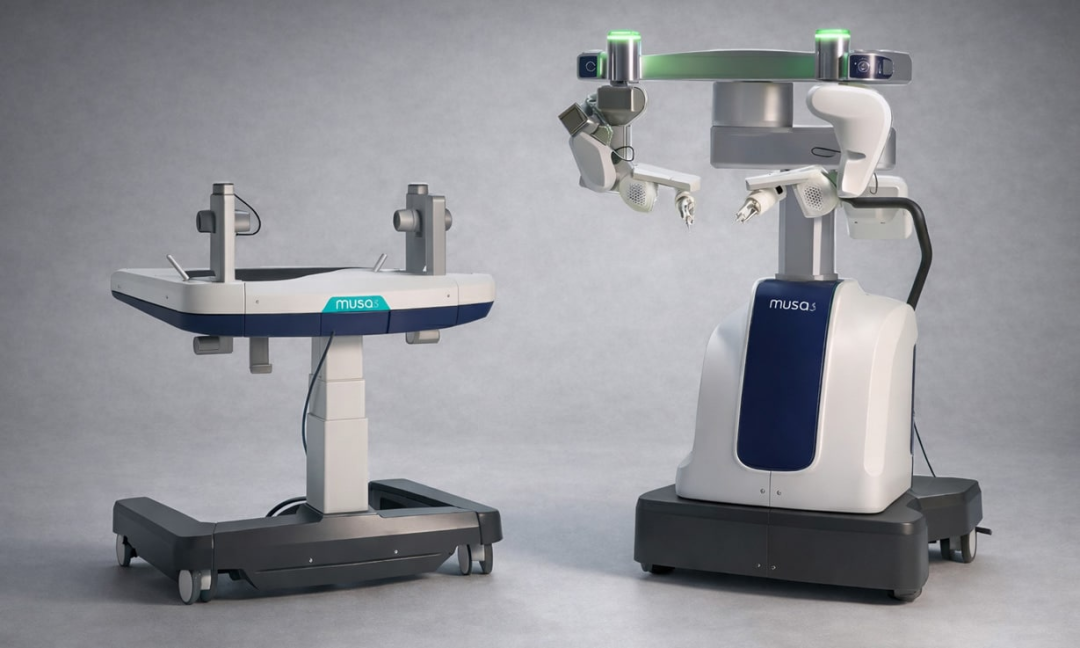
获批CE!显微外科手术机器人
发布时间:2026-05-08来源:MedRobot
2026年5月7日,创新医疗科技公司Microsure宣布其显微外科机器人MUSA-3获得CE认证,可在欧洲进入临床使用。同日,公司任命Alex Joseph为新任CEO,接替联合创始人Iwan van Vijfeijken。Joseph此前深度参与MUSA-3的开发工作,此次职位交接在时间节点上与认证同步,具有明确的战略信号意义——公司将运营重心从产品开发转向市场准入与临床推广。Microsure 2016年由埃因霍温科技大学(TU/e)与马斯特里赫特大学医学中心联合创立,现有30余名技术人员。2023年10月完成B2轮融资约3800万欧元,投资方包括欧洲创新委员会基金(EICF)、Invest-NL及多家私人投资机构,并额外获得荷兰经济部RvO创新贷款及EIC Accelerator Grant。融资用途即为推进MUSA-3完成临床研究及CE/FDA双轨注册。CE认证落地,意味着2023年融资设定的欧洲准入目标已达成;FDA清零仍未披露时间表。MUSA-3定位于开放式超显微外科(open super-microsurgery),目标血管/淋巴管直径在0.3–0.8mm量级,覆盖淋巴管-静脉吻合(LVA)、游离皮瓣血管吻合及周围神经修复三类适应症。系统通过运动缩放与震颤过滤提升操作精度,外科医生在控制台通过操纵杆操控,搭配数字外窥镜或混合手术显微镜使用。MUSA-3的一个显著设计取向是兼容外科医生惯用的多品牌显微器械,即系统本身不捆绑专有耗材——这与同赛道主要竞争对手MMI(Medical Microinstruments)的策略形成对比。MMI的Symani系统采用自研NanoWrist专有微型腕式器械,器械与机器人深度集成,且已获FDA 510(k)清关(2024年anastomosis适应症,2025年12月NanoWrist Scissors & Forceps扩增软组织分离适应症)。在监管进展上,MMI目前处于更领先的商业化阶段:Symani在欧洲和美国均已获准临床使用,2025年12月已在Tampa General Hospital完成首例全程机器人辅助淋巴静脉旁路手术(从切皮到关皮),并于2025年底获得CMS针对LVB手术的CPT专项代码(CPT 1019T),覆盖Medicare报销,这是显微外科机器人领域首个正式支付路径。MUSA-3的CE认证使Microsure进入可对比的起点,但在临床证据积累量和支付体系建设上,两者差距明显。CE认证本身是准入门槛,不等于市场落地。Microsure新任CEO Alex Joseph在官方声明中明确将"生成临床证据"列为近期首要任务——这一表述指向真实世界数据(RWD)的系统收集,而非延续此前MUSA-2原型机在马斯特里赫特大学医学中心和瑞典乌普萨拉学术医院进行的50例探索性研究。对于这类高精度、低手术量的细分赛道,商业化面临的核心约束并不仅是监管,而是:具备超显微外科手术能力的外科医生基数本身极为有限(全球约500–1000名),系统定价与医院采购预算的匹配,以及缺乏类似MMI已争取到的CPT报销支撑。Microsure已与融资方kineo建立资产融资协议,计划以租赁模式降低医院的初始采购门槛,但具体定价和实际租赁条款未公开披露。FDA注册进展是另一个悬而未决的变量。2023年B2轮融资时,公司明确将"FDA clearance"列入资金使用计划,但截至本次CE认证公告,未见任何510(k)提交或IDE申请的公开信息。
综合▌微创机器人 | 佗道医疗 | 直观复星 | 威高
腔镜▌精锋医疗 | 思哲睿智能医疗 | 康诺思腾
骨科▌罗森博特 | 元化智能 | 长木谷 | 鑫君特| 史赛克
血管介入▌爱博合创 | 唯迈医疗
穿刺机器人▌真健康 | 惟德精准
手术机器人工具▌良医
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。