12635个原子!量子计算摸到蛋白质了吗?


量子计算正在从小分子演示,进入与超级计算共同处理真实生物体系的工程阶段。
蛋白质像一座折叠的城市。每一个原子都是灯点,电子在灯点之间移动,药物分子只有找到恰当的缝隙,才可能改变一条生命通路。量子计算谈医药已经谈了很多年,但很长一段时间里,它更像远处的灯塔:方向清楚,距离模糊。
5月5日,IBM、RIKEN和克利夫兰诊所把这盏灯往前推了一段。三方宣布,研究团队用量子中心超级计算方法模拟了一个由12635个原子组成的蛋白质-配体复合物,IBM称其为“已知最大规模的量子计算蛋白质模拟”。与其说这是一场关于单台量子计算机的胜利,不如说它展示了量子处理器、算法、超算与生命科学问题第一次以更接近真实任务的方式扣在一起。
这不是“量子优势”的宣布,也不是药物研发被一夜改写。它更像一个清晰信号:量子计算正在从小分子演示,进入与超级计算共同处理真实生物体系的工程阶段。

指数之墙与生物医学的算力危机
在当代制药工业的宏大叙事中,寻找一种能够精准锁定蛋白靶点的药物分子,无异于在银河系中寻找一颗特定的尘埃。蛋白质作为生命功能的执行者,其结构之复杂、动态之微妙,使得传统的计算化学方法在它们面前显得捉肘见襟。
计算化学的核心困境在于求解多电子系统的薛定谔方程。虽然方程的形式在物理学家眼中简洁优美,但在处理生物大分子时,其计算量会随着系统规模的增加而呈指数级增长。每一个电子不仅受到原子核的吸引,还受到其他所有电子的排斥和相互关联,这种被称为“电子关联”的现象是化学反应和分子结合的本质。目前主流的经典计算方法在处理这些问题时面临着严重的权衡:密度泛函理论(DFT)虽然能够处理成千上万个原子,但它依赖于近似,往往难以准确捕捉药物分子与蛋白之间关键的弱相互作用;而被称为“金标准”的耦合簇方法(CCSD)虽然精度极高,但其计算复杂度随轨道数量的七次方增长,这使其只能处理几十个原子的微小系统。
这种算力的匮乏直接导致了药物研发的时间博弈。由于无法在模拟中获得足够的精度,制药公司不得不依赖昂贵的物理实验和反复的临床测试。目前,开发一种新药平均需要耗费超过10年的时间,投资额高达数十亿美元。如果能够利用量子计算的特性,在计算机中准确预测候选药物与蛋白质的结合亲和力,将极大地缩短研发周期,为人类对抗致命疾病赢得宝贵时间。

12000原子的跨代跃迁
2026年5月5日,科学界迎来了一个分水岭时刻。克利夫兰医学中心、日本理化学研究所与IBM联合发布的研究成果显示,他们利用量子处理器与全球最强大的超级计算机协同工作,完成了对包含12635个原子的蛋白质复合体的高精度模拟。这一成果不仅刷新了量子计算模拟生物分子的规模纪录,更证明了量子计算机在当前的“效用阶段”已经具备了解决实际科学问题的能力。
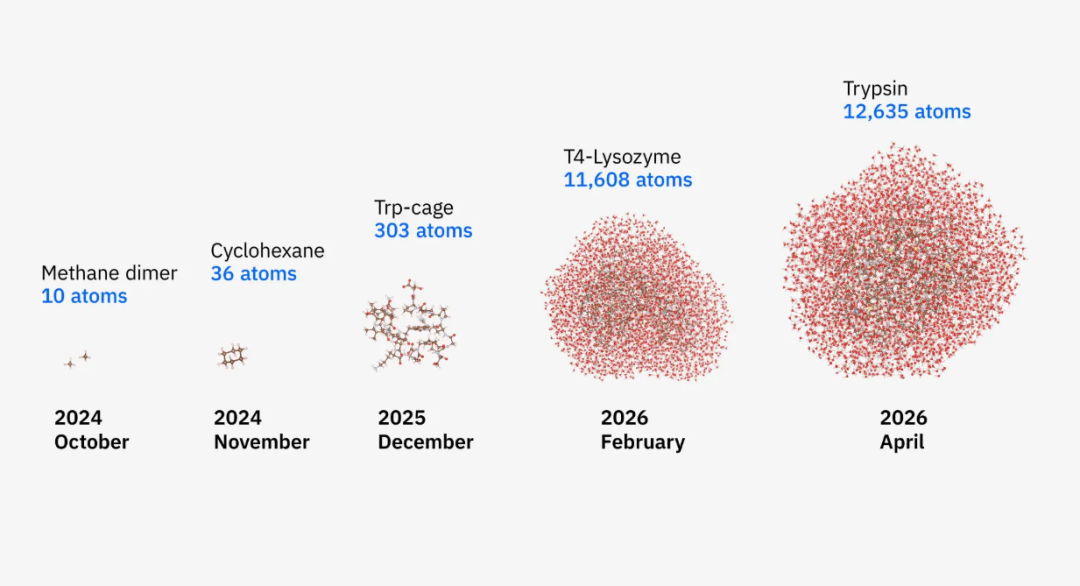
研究团队并未选择结构简单的实验分子,而是选择了具有重大医疗价值的系统:胰蛋白酶和T4溶菌酶。胰蛋白酶是人体消化系统中不可或缺的酶,而T4溶菌酶则是免疫系统对抗细菌入侵的关键。更重要的是,这些系统被置于真实的液态水溶液环境中进行模拟,而非真空的孤立状态。
来源:IBM
在数月前,同类研究的模拟规模还仅限于303个原子的Trp-cage微蛋白。在半年内实现40倍的规模飞跃,其背后的技术驱动力令人惊叹。这项任务动用了跨越国界的顶级算力资源:位于美国克利夫兰和日本神户的两台156量子比特IBM Quantum Heron r2处理器,以及日本的“富岳”(Fugaku)超算和Miyabi-G超算系统。在大约100小时的连续运行中,系统执行了9200个量子电路,收集了多达13亿次的测量结果。这是迄今为止量子化学领域资源投入最为密集、计算规模最为宏大的异构计算实验。

量子中心超级计算
为了实现这种海量原子的模拟,单纯增加量子比特的数量是不够的。IBM提出的“量子中心超级计算”(QCSC)框架提供了一种全新的范式,将量子计算机作为高性能计算工作流中的核心加速单元,而非独立的孤岛。
这种QCSC架构打破了量子计算与经典计算之间的界限。在这一框架下,硬件基础设施被划分为多个层级:第一层是负责实时操作和纠错解码的量子系统;第二层是与之紧密相连的CPU和GPU系统,用于低延迟的任务管理;第三层则是远程的大规模超算集群,负责处理海量的数据拼接。

来源:IBM
在模拟12635个原子的胰蛋白酶时,传统的“串行”模式——即量子算完再传给经典——会导致严重的效率瓶颈。QCSC架构实现了闭环的数据交换,使得量子处理器(QPU)能够像经典CPU访问缓存一样,高效地参与到整个迭代计算中。日本理化学研究所的“富岳”超算拥有超过15万个计算节点,其惊人的并行处理能力与量子处理器的采样能力相结合,实现了72.5%的并行效率。这种紧密的编排证明,量子与经典并非竞争对手,而是可以完美合奏的伙伴。

EWF-TrimSQD的精妙逻辑
如果没有算法上的突破,即便拥有最强大的硬件,也无法在有限的时间内处理1.2万个原子的电子纠缠。研究团队开发的EWF-TrimSQD算法结合了“分而治之”的数学思想与量子物理的深刻洞察。
首先是波函数嵌入技术(EWF)。算法基于一个深刻的物理前提:在大多数蛋白质系统中,电子的强关联效应具有局域性,一个原子的电子行为主要受到其周围7-10埃范围内环境的影响。通过将巨大的蛋白质复合体分解为成千上万个相互重叠的小碎片,算法将整体计算的复杂度降低到了线性阶次。对于大多数简单的碎片,系统使用经典方法处理;而对于涉及药物结合位点的关键核心,则交给QPU进行高精度模拟。
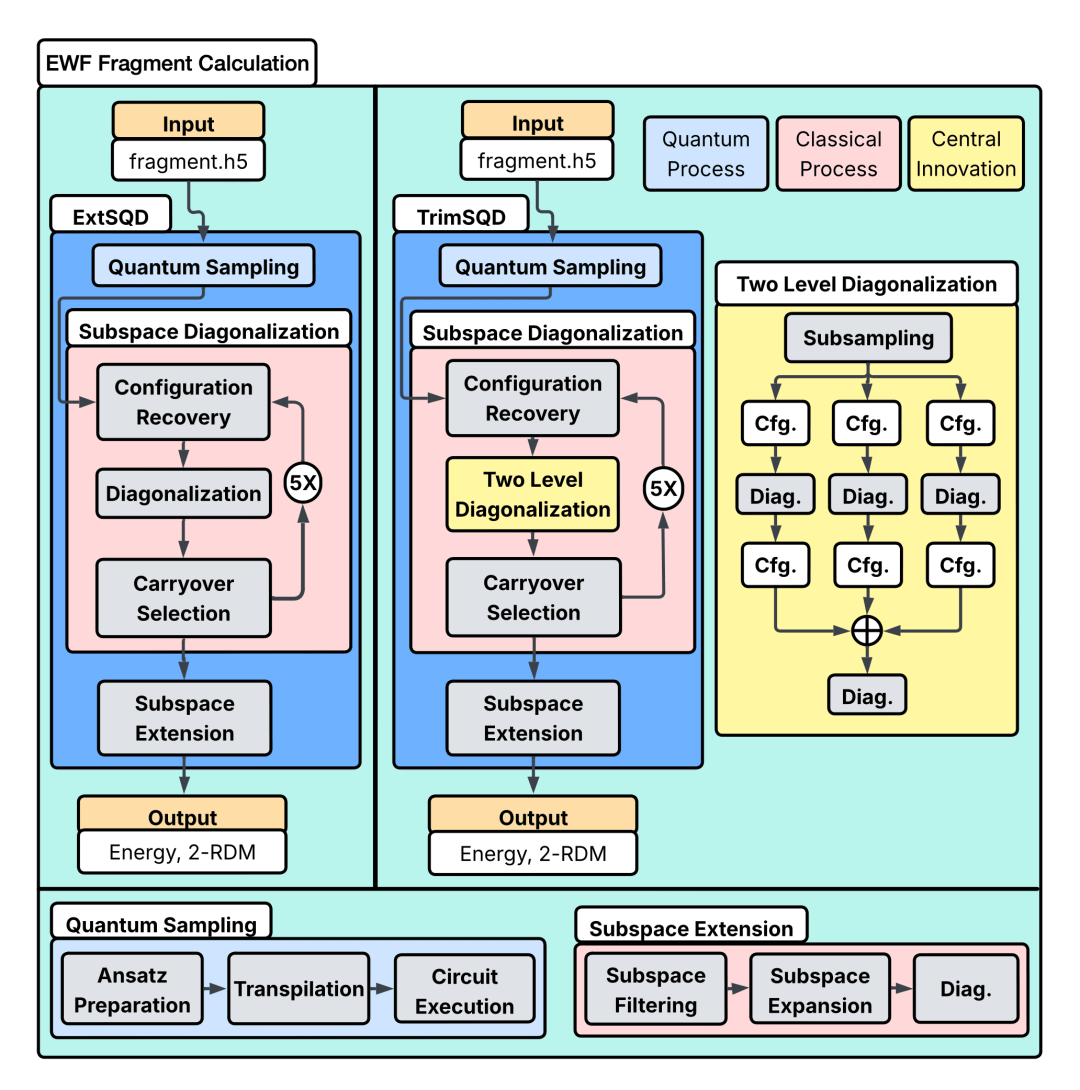
接下来的关键是采样量子对角化(SQD)。电子构型空间是一个组合爆炸的汪洋大海,而真正决定能量稳定的构型只是极小部分。理论化学家Klaus Ruedenberg曾用“活木”和“死木”来形容这种差异:在海量的构型中,超过99%是毫无意义的“死木”。量子计算机通过SQD算法,像是在海量的拼图碎片中迅速找出了构成画面核心的那几块“活木”,而经典超算随后在这些精选出的碎片基础上完成最后的拼图。这种“修剪”机制将计算精度提升了210倍,使得结果能够与经典计算的最高标准相媲美。

从效用到容错的远征
虽然12635个原子的模拟已是壮举,但这仅仅是量子计算星辰大海的起点。根据IBM更新的路线图,我们正站在通往“容错量子计算”的关键节点上。
2025年,名为“Loon”的处理器将测试新型纠错码,旨在将纠错成本降低90%;2026年,“Kookaburra”将引入模块化架构,让量子信息在芯片间自由流动。而所有的目光都锁定了2029年,届时IBM计划推出首个大规模容错系统“Starling”。Starling将拥有200个逻辑量子比特,能够执行1亿个量子门操作。这意味着到那时,我们或许不再需要将分子拆解成碎片,而是可以直接对整个蛋白质核心进行无损的量子重构。
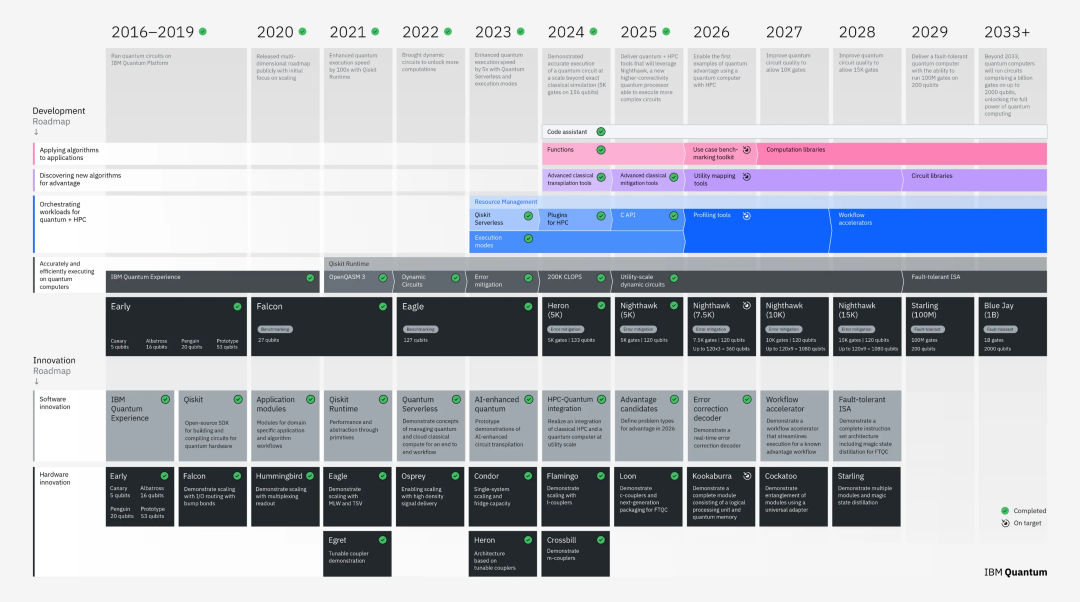
来源:IBM
更令人振奋的是量子计算与人工智能的汇流。正如IBM首席执行官Arvind Krishna所指出的,量子计算负责生成极其精确的微观能量数据,而AI则学习这些数据中的模式。这种协同将彻底改写新材料和新药物的发现规则:量子提供真理的深度,AI提供探索的广度。

量子计算正在从“能跑”转向“能嵌入”
过去几年,量子计算的新闻多围绕硬件指标展开:量子比特数、门错误率、相干时间、纠错码距、逻辑错误率。它们仍然重要,但这次新闻给出的信号更偏应用侧:一个有真实科学意义的问题,如何被拆成可交给量子处理器和超算共同完成的作业?如何在不同硬件之间调度?如何把量子采样变成经典求解的有效输入?如何让结果能被化学家和药物研究者理解?
这种转向也会改变企业和科研机构评估量子计算的方式。过去看一台量子计算机,常问它有多少量子比特、线路保真度多高;未来还要问它能否稳定接入超算调度,能否支持长时间作业,能否与经典化学软件、数据格式、误差分析和任务管理系统衔接。对真实用户来说,可用性往往不只来自芯片,而来自整条链路。
如果说早期NISQ阶段的许多演示是在证明“量子设备确实能运行”,那么这类工作开始证明“量子设备可以嵌入科学计算基础设施”。这也是它对产业判断的价值所在。近期量子计算最值得关注的方向,并不只是单机性能竞赛,而是量子处理器、GPU/CPU超算、低时延控制、软件栈和具体科学任务之间的耦合能力。谁能把这些环节接成稳定流水线,谁就更接近可用量子算力。

还不能过度乐观,但也不该低估
当算力不再是制约认知的障碍,人类对生命的掌控将达到前所未有的高度。这项技术突破最直接的影响在于个性化医疗的普及。未来,我们可以根据每个人的基因特征,在量子空间中预演药物的相互作用,实现真正的“精准打击”。在下一次突发流行病侵袭时,量子中心超级计算机可以在数周内完成对病毒蛋白的扫描,筛选出最佳候选药物,而非被动地等待实验结果。
冷静地看,这次实验距离药物研发的日常可用仍有几道门槛。精度要提高,基组要更接近真实化学需求,误差缓解和片段策略要更稳,量子硬件要更低错误率、更高可用性,整条工作流还要从论文级演示走向可重复、可计费、可维护的平台服务。即便如此,它仍然值得被认真记录。
原因很简单:量子计算的进步从来不是一夜之间替代经典计算,而是先在经典计算最吃力的角落打开缝隙。
目前,量子计算还没有成为药物发现的发动机。它更像是被接入一台巨大的科研机器中的新部件,第一次在真实生物体系的尺度上发出稳定的声响。今天我们听到的不是终点的礼炮,而是车间里一枚齿轮开始咬合的声音。对于量子计算来说,这也许正是更重要的开始。
[1]https://newsroom.ibm.com/2026-05-05-cleveland-clinic,-riken,-and-ibm-model-a-12,635-atom-protein-the-largest-known-to-be-simulated-with-quantum-computers
[2]https://arxiv.org/abs/2605.01138
[3]https://www.ibm.com/quantum/blog/cleveland-clinic-protein-qcsc
[4]https://www.ibm.com/quantum/blog/cleveland-clinic-riken-chemistry
[5]https://research.ibm.com/blog/quantum-centric-supercomputing-system-reference-architecture