大卫贝克团队从头设计小分子结合蛋白质家族:开启按需定制生物传感器的新纪元
将 ScienceAI 设为星标
第一时间掌握
新鲜的 AI for Science 资讯

编辑丨&
小分子结合蛋白在生物传感、环境监测、疾病诊断等领域有广泛应用。然而,天然蛋白质的配体结合特异性有限,而传统工程改造耗时费力。近年来,深度学习在蛋白质设计领域取得了突破性进展,但从头设计高亲和力、高特异性、且可转化为传感器的小分子结合蛋白仍然充满挑战。
由华盛顿大学(University of Washington)的 David Baker 团队领衔,联合韩国科学技术院(KAIST)、哈佛大学等多家顶尖科研机构的研究团队,通过结合深度学习与基于物理的方法,成功设计并验证了一个具有多样化几何口袋的 NTF2 蛋白质家族,为环境、生物医学及分析化学领域的小分子检测提供了全新的平台。
相关研究以「Small-molecule binding and sensing with a designed protein family」为题,于 2026 年 3 月 28 日发布在《Nature Communications》。

论文链接:https://www.nature.com/articles/s41467-026-70953-8
支架生成与多样化口袋
该研究的核心策略是利用 NTF2(Nuclear Transport Factor 2)样折叠作为基础支架。这个折叠由 3 个螺旋和一个弯曲的 6 链 β 片层组成,形成一个天然的大空腔,许多 NTF2 家族蛋白在自然界中就能结合类固醇类小分子。
研究团队希望利用这个「特权」折叠,生成一系列结构多样的骨架,以适应不同小分子的形状和化学性质。
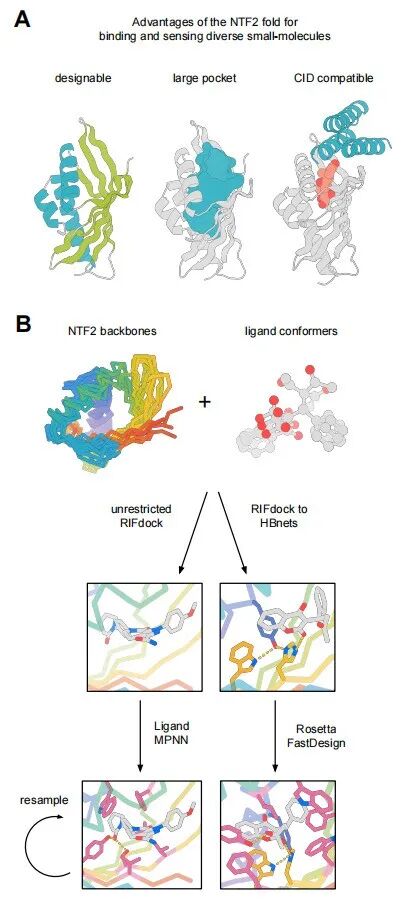
图 1: 基于NTF2的小分子结合与传感设计策略。
研究团队通过三种主要路径生成了超过 10,000 个具有多样化口袋几何形状的蛋白质支架:
基于家族范围内的「幻觉」(Hallucination)生成方法,保留天然氢键网络,产生了 1,615 个支架。
通过 ProteinMPNN 重新设计上述支架序列,并使用 AlphaFold 验证其折叠准确性,筛选出 3,230 个支架。
利用 Rosetta 进行参数化生成,结合 ProteinMPNN 重新设计和 AlphaFold 验证,生成了 6,838 个支架。
这套庞大的支架库为针对不同目标小分子进行精确匹配提供了可能。
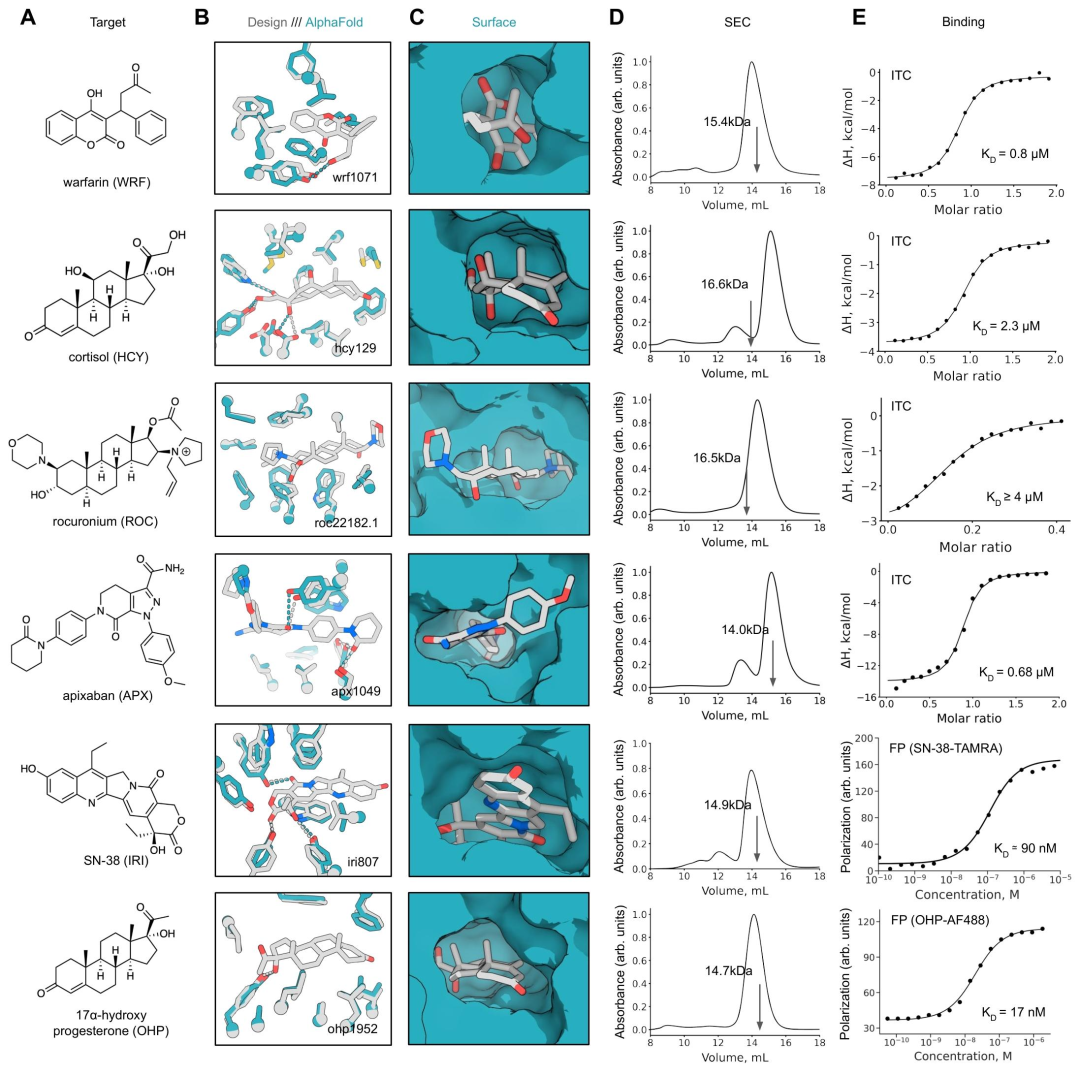
图 2:小分子结合蛋白的表征。
研究人员选取了六种在化学和结构上各异的小分子作为设计目标,利用 RIFdock 工具,研究团队将这些配体分别置于万余个 NTF2 支架的中央口袋中,开启了针对性的结合界面设计。
结合物理与深度学习的设计
针对小分子结合蛋白设计中「极性界面设计」这一难题,研究团队采用了两种互补的设计方法。
策略 1(用于 Set 1 骨架):利用骨架中预存的氢键网络(HBNet)来「锚定」小分子的极性基团。这种方法侧重于物理模拟,通过将小分子的极性官能团对接到 Set 1 支架中预先安装的氢键网络(HBNets)上,并结合 Rosetta 进行序列优化,特别适合那些含有极性官能团的配体。
策略 2(用于 Set 2 和 3 骨架):充分利用了深度学习模型的优势,引入了专门针对蛋白-小分子复合物训练的 LigandMPNN 模型。与传统方法相比,LigandMPNN 能更有效地平衡蛋白质-配体相互作用与蛋白质内部的相互作用。
在实验表征阶段,研究团队将筛选出的数万个设计序列通过合成寡核苷酸的方式在酵母中表达,并利用酵母表面展示技术结合荧光激活细胞分选(FACS)进行筛选。结果显示,所有六个目标分子都成功检测到了结合信号。
皮质醇传感器的构建与应用
作为该研究最具应用价值的案例,团队进一步开发了基于皮质醇(Cortisol)的生物传感器。皮质醇是人体生理样本中重要的生物标志物,其在血浆中的异常升高(大于 38 nM)是库欣综合征等疾病的诊断依据。
为了构建高性能传感器,研究人员首先通过定点饱和突变(SSM)和组合突变筛选,将原始设计 hcy129 的结合亲和力提升至 68 nM(变体名为 hcy129.1),亲和力提高了 31 倍。
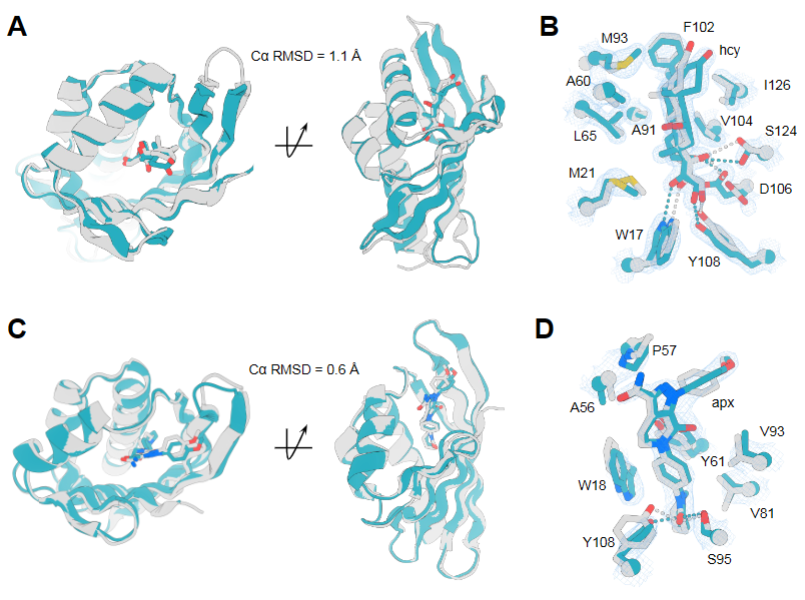
图 3:设计的皮质醇和阿哌沙班结合蛋白的结构分析。
通过对富集群体进行 FACS 分析和 SEC 验证,团队成功获得了一个名为 miniH11 的组件,它能与 hcy129.1_CID 在皮质醇存在的情况下形成稳定的化学诱导二聚体(CID)系统。最后,研究团队通过将这两个 CID 组件分别与 NanoBiT 系统的 SmBiT 和 LgBiT 荧光素酶片段融合,构建了一个发光传感器。
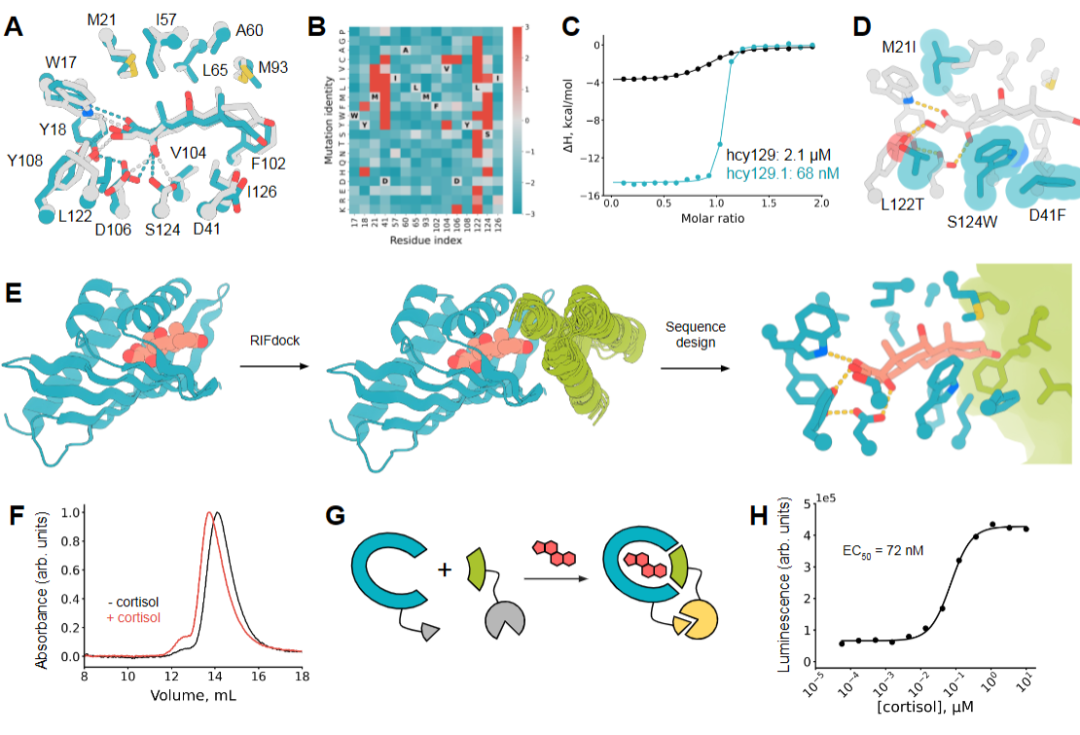
图 4:用于皮质醇传感的化学诱导异二聚体的设计与表征。
该传感器对皮质醇、可的松和 17α-羟孕酮有响应,但对皮质酮(缺少 17 位羟基)无响应,与设计模型中关键极性相互作用的预测一致。
技术洞察
该研究展示了深度学习工具(如 ProteinMPNN, LigandMPNN 和 AlphaFold)与传统物理建模(Rosetta)深度融合的巨大潜力,尤其是如何从头设计出针对多种小分子的高亲和力结合蛋白,并将其转化为功能性传感器。特别是化学诱导二聚化系统的设计为构建模块化、可调控的生物传感器提供了通用平台。
尽管目前在处理疏水性较强的配体或极度相似的化学异构体时,特异性仍面临挑战,但这一平台的建立为未来开发面向全球环境监测或个人健康管理的即时感测技术奠定了理论与实验基础。随着未来深度学习模型对蛋白-配体相互作用预测精度的进一步提升,定制化生物传感器的开发将变得更加精准和高效。
相关链接:https://phys.org/news/2026-04-ai-proteins-built-specific-compounds.html
人工智能 × [ 生物 神经科学 数学 物理 化学 材料 ]
「ScienceAI」关注人工智能与其他前沿技术及基础科学的交叉研究与融合发展。
欢迎关注标星,并点击右下角点赞和在看。
点击阅读原文,加入专业从业者社区,以获得更多交流合作机会及服务。
