上交大团队提出Meta-encoder框架,释放病理大模型集群力量,在多项国际公认数据集上刷新纪录
将 ScienceAI 设为星标
第一时间掌握
新鲜的 AI for Science 资讯

编辑丨%
在数字病理学领域,病理基础模型(Pathological Foundation Models, PFMs)正引领着一场诊断革命。这些模型通过在数以亿计的病理图像切片上进行预训练,展现出了惊人的特征提取能力。
但随着 UNI、CTP、Virchow 和 PLIP 等多个顶尖模型的涌现,研究者们发现了一个尴尬的现状:没有任何一个模型能在所有类型的癌症检测和分型任务中始终保持领先。每个模型都有其独特的「知识偏好」和局限性。如何有效地将这些「专家模型」的力量整合在一起,而不引入巨大的计算负担,成为了临床应用前的核心课题。
2026 年 4 月 15 日,上交大团队提出了一种名为 Meta-encoder 的统一集成框架,以「Meta-encoder: a unified integration framework for multiple pathological foundation models in cancer detection」为题发表在《Nature Communications》上,为这一难题提供了极具启发性的解决方案。

论文链接:https://www.nature.com/articles/s41467-026-71558-x
多模型协同的架构设计
目前的病理 AI 模型面临着「术业有专攻」的问题。例如,有些模型在检测肺癌微小病灶方面表现优异,而另一些则在识别乳腺癌转移方面更具优势。传统的做法要么是简单地对多个模型的输出取平均值,要么是根据经验选择某一个模型。但这两种方式都无法在原子级别(即每个组织小块)实时判断哪个模型更可靠。
Meta-encoder 框架的设计初衷是构建一个「大脑」,它能够动态地判断在面对当前的病理切片时,应该听取哪位「专家」的意见。
该框架的核心由两个关键组件组成:权重预测器(Weight Predictor)和特征聚合器(Feature Aggregator)。研究团队首先冻结了所有预训练的病理基础模型,这意味着不需要对这些庞大的模型进行昂贵的重新训练,从而确保了方案的轻量化。
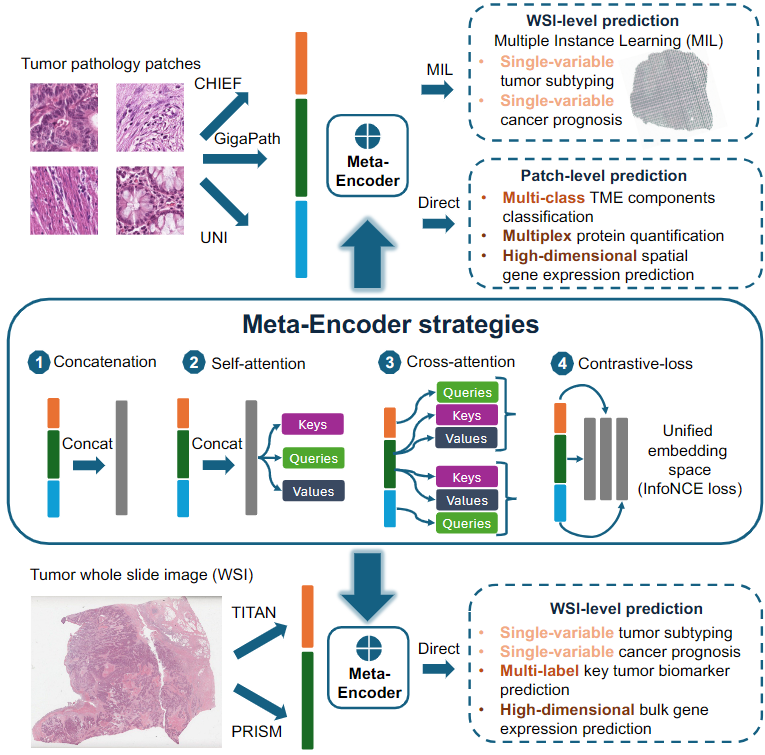
图 1:Meta-encoder 框架。
在工作流程中,一张全切片图像(WSI)被切分成成千上万个小方块(Patch)。每个小方块会同时进入多个基础模型进行特征提取。此时,权重预测器(由简单的多层感知机组成)会根据这些特征,为每个模型分配一个分值。
如果某个小方块的特征在 A 模型中表现得极具辨识度,它就会获得更高的权重。随后,特征聚合器会将这些带有权重信息的特征进行融合。这种方法本质上是一种「参数高效微调」(PEFT)策略,它仅需调整极少数的新增参数,就能让多个基础模型产生协同效应。
跨任务与跨数据集的严苛验证
为了验证 Meta-encoder 是否真的优于单一模型,研究团队在多个具有挑战性的癌症检测任务上进行了测试,包括肺癌亚型分类(NSCLC)、乳腺癌淋巴结转移检测(Camelyon16)以及结肠癌组织分类。
实验结果显示,Meta-encoder 在所有测试任务中均显著超越了单一的最佳基础模型。在肺癌分类任务中,Meta-encoder 能够整合来自 CTP 和 UNI 等模型的不同维度信息,使得诊断的曲线下面积(AUC)达到了新的高度。
更重要的是,研究团队发现,简单地增加基础模型的数量并不一定会导致性能下降,Meta-encoder 能够通过动态权重分配,有效地过滤掉那些对当前任务贡献较小甚至有干扰的模型信息。
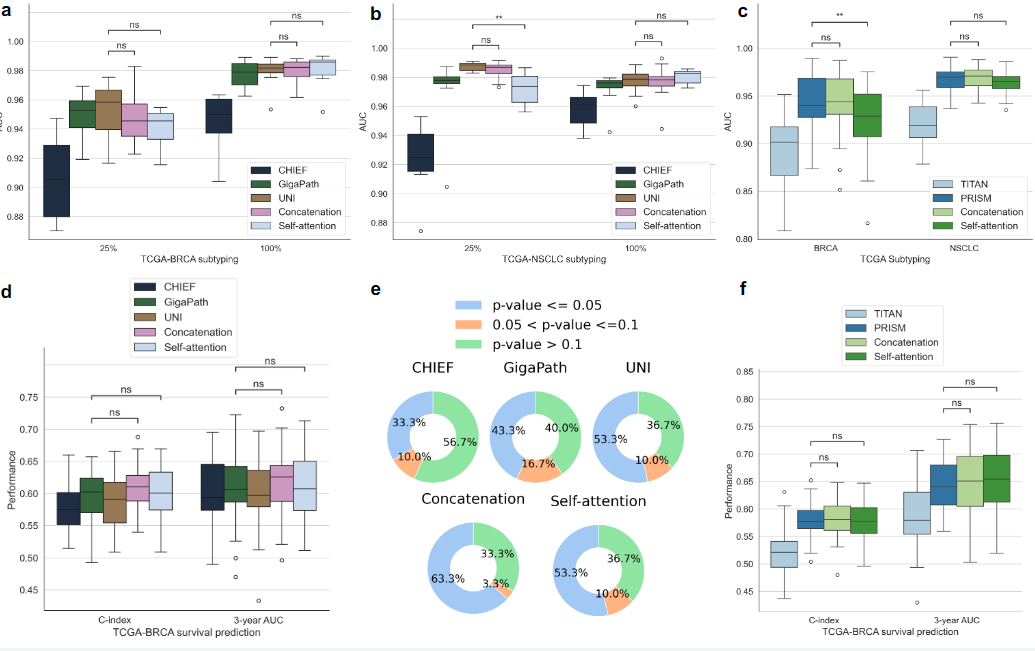
图 2: 单变量亚型分型和预后任务中 Meta-Encoder 策略的性能对比。
对于输出单一数值的任务,Meta-Encoder无需猜哪个模型最好,直接拼接即可获得与最优模型相当的性能,大幅降低了模型选择成本。
计算效率与临床应用潜力
对于临床部署而言,算力成本是一个绕不开的话题。如果为了提升一点点精度而需要成倍的 GPU 资源,那么这项技术很难在基层医院普及。Meta-encoder 巧妙地平衡了这一点。由于它采用了冻结基础模型参数的策略,实际需要训练的参数量极小。
与需要大规模重预训练的融合方法 GPFM 相比,Meta-encoder 在蛋白定量任务上,自注意力策略的平均 Spearman 相关系数(0.813)优于 GPFM(0.797)。在空间基因表达任务上,自注意力在所有三个数据集的Pearson 和 SSIM 指标上均显著优于 GPFM。
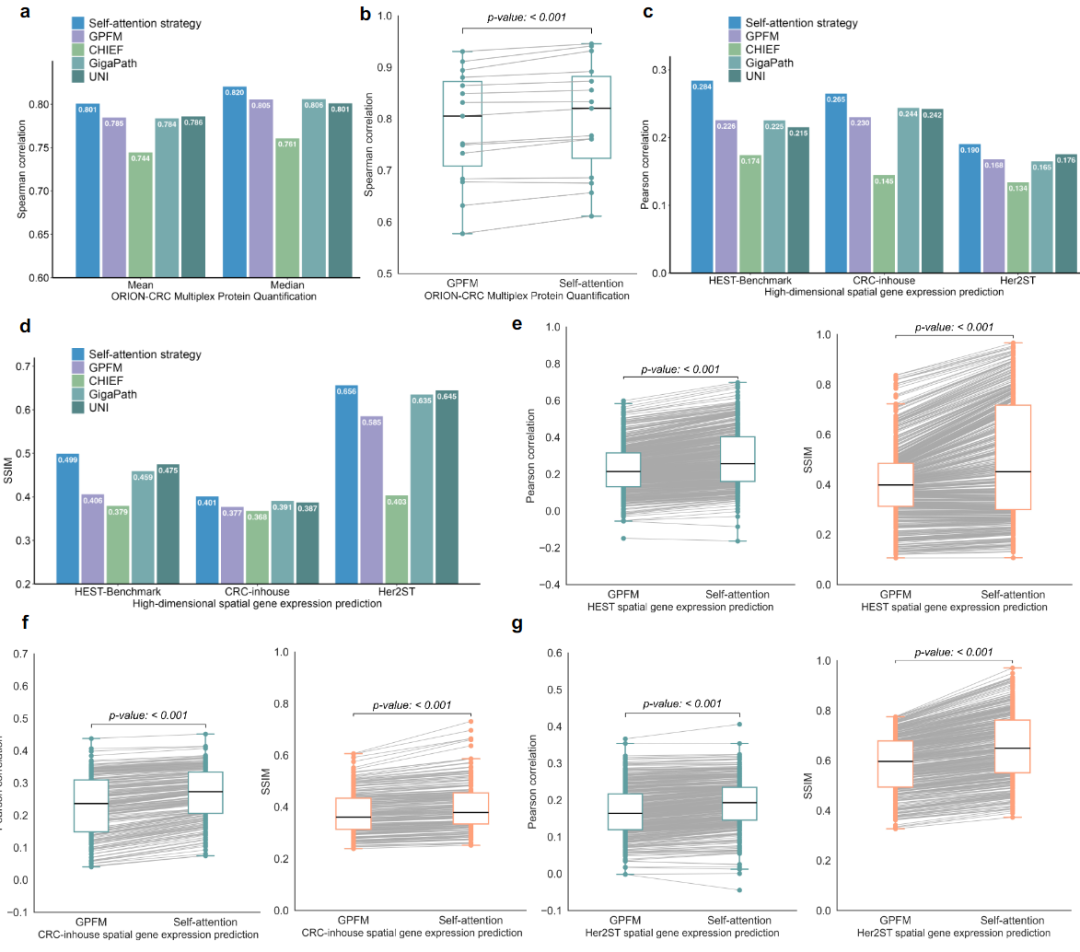
图 3:在多重蛋白质定量和高维基因表达预测任务上,元编码器的自注意力策略与 GPFM 的对比。
GPFM 需要重预训练,计算成本极高。Meta-Encoder 只需在微调阶段进行特征融合,以自注意力策略为例,训练时间和显存开销与单模型相当,真正做到「轻量级即插即用」。
总结与技术洞察
Meta-encoder 框架的提出代表 AI 正逐步从「追求单个最强模型」转向了「追求最优集成策略」迈进。通过动态权重预测和高效的特征聚合,该框架不仅突破了单一模型在处理复杂异质性组织时的性能瓶颈,还极大地降低了多模型协同的计算门槛。
没有任何一种算法能够穷尽生命的变数,但通过合理的机制将人类现有的算法智慧凝聚在一起,研究者就得以无限接近精准医疗的目标。随着更多专注于特定领域的基础模型被开发出来,Meta-encoder 这种「博采众长」的整合模式,将成为推动 AI 在临床病理诊断中真正落地的核心引擎。
人工智能 × [ 生物 神经科学 数学 物理 化学 材料 ]
「ScienceAI」关注人工智能与其他前沿技术及基础科学的交叉研究与融合发展。
欢迎关注标星,并点击右下角点赞和在看。
点击阅读原文,加入专业从业者社区,以获得更多交流合作机会及服务。
