Adv Sci:北京大学李蓉等团队找到修复多囊卵巢综合征患者子宫内膜的“钥匙”——IGFBP5蛋白
多囊卵巢综合征(PCOS)是一种代谢疾病,也是导致不孕的主要原因。越来越多的证据表明,子宫内膜内在缺陷在 PCOS 相关不孕中发挥关键作用,但其具体分子机制仍不明确。
2026年3月12日,北京大学李蓉、庞艳莉、Wang Yue、周平共同通讯在
Advanced Science(IF=14.1)
在线发表题为
IGFBP5 Restores Endometrial Receptivity and Rescues Implantation Failure in Polycystic Ovary Syndrome
的研究论文。本研究证明,白介素22(IL-22)信号直接调节子宫内膜功能,IL-22-STAT3通路的下调导致PCOS子宫内膜接受性受损。
在类PCOS小鼠模型中,外源性IL-22施用一致地恢复了STAT3的磷酸化,并通过增强子宫内膜受体性有效缓解着床失败。在机制上,研究鉴定出胰岛素样生长因子结合蛋白5(IGFBP5)是STAT3的直接下游靶基因。在PCOS样小鼠子宫中敲低IGFBP5可消除IL‑22的保护作用,而补充IGFBP5则可恢复子宫内膜容受性并挽救胚胎着床。
综上,本研究表明IL‑22‑STAT3‑IGFBP5轴抑制是PCOS子宫内膜容受性受损的关键机制,为通过补充IGFBP5改善妊娠结局提供了潜在治疗靶点。

多囊卵巢综合征(PCOS)是育龄期女性最常见的内分泌与生殖系统疾病。不孕与妊娠并发症仍是该病最主要的临床问题。近年来,越来越多的证据表明,除了公认的排卵异常外,子宫内膜功能异常是导致PCOS 患者不孕的独立因素。
研究显示,子宫内膜功能受损可显著降低PCOS 患者体外受精(IVF)的妊娠结局。然而,由于其内在病因尚不明确,目前在种植窗期(WOI)改善子宫内膜功能的临床干预手段仍然有限。
子宫内膜容受性是指子宫内膜接受胚胎着床的能力,由雌激素与孕激素调控的子宫内膜细胞增殖与分化所决定。在胚胎着床过程中,母体信号与胚胎信号共同调控上皮细胞功能,协调着床过程。宫腔上皮细胞与胚胎之间的初始接触与相互作用,是囊胚成功黏附与侵袭的关键。
近期单细胞空间转录组分析显示,PCOS患者子宫内膜存在上皮增生与功能异常亚群,直接将上皮缺陷与子宫内膜容受性受损相关联。但上皮功能异常导致着床失败的机制研究仍较为缺乏,阻碍了针对PCOS患者子宫内膜功能异常的靶向干预研究。
在影响子宫内膜功能的因素中,免疫调节细胞因子越来越被认可为着床的关键调节因子。尽管促进胚胎着床的趋化因子下调,PCOS子宫内膜的促炎状态表现为白介素(IL)-6、IL-8、IL-18和C反应蛋白水平升高,进一步损害子宫内膜功能和受体性,表明免疫失调是PCOS着床失败的重要因素。
IL-22属于IL-10家族,调控黏膜免疫和组织稳态,并被认为与妊娠维持有关。之前的研究表明,IL-22能改善胰岛素抵抗并抑制肉芽细胞炎症,缓解多囊卵巢综合征中的代谢和卵巢功能障碍。然而,IL-22是否直接调控PCOS中的子宫内膜功能和子宫内膜接受性尚不明确。
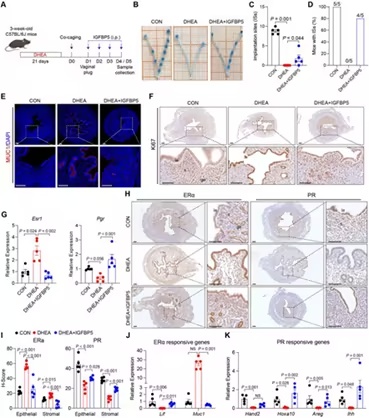
IGFBP5可改善PCOS样小鼠的胚胎着床障碍(摘自
Advanced Science
)
本研究观察到PCOS患者分泌性子宫内膜IL-22水平低于对照组,伴有JAK-STAT3信号通路下调。为进一步探究其机制,研究构建了PCOS患者来源的子宫内膜类器官及脱氢表雄酮(DHEA)诱导的PCOS样小鼠模型。在两种模型中,外源性补充IL‑22均可通过增强STAT3磷酸化改善子宫内膜容受性、促进胚胎着床。
子宫内膜类器官实验证实,STAT3可直接结合胰岛素样生长因子结合蛋白5(IGFBP5)的启动子区域并正向调控其转录。此外,在PCOS样小鼠模型中补充IGFBP5可改善子宫内膜容受性。上述结果表明,靶向IL‑22‑STAT3‑IGFBP5轴具有改善PCOS患者生育能力的治疗潜力。
原文链接:https://doi.org/10.1002/advs.202520455
