Cell Death & Differ:中南大学殷刚团队发现p53的“守护者”MEIS1!它化身分子诱饵“舍己救人”,为癌症治疗提供全新靶点
通过破坏MDM2与p53的相互作用或抑制其E3连接酶活性来靶向MDM2,是恢复p53功能的一种有前景的策略。然而,在实现抗癌疗效的同时最大限度地减少剂量限制性毒性,仍然是一个重大挑战。此外,MDM2还能泛素化多种非p53靶点,这使其治疗性靶向变得复杂。
2026年3月14日,中南大学殷刚独立通讯在
Cell Death & Differentiation
在线发表题为
Ubiquitination of MEIS1 by MDM2 serves as a switch for p53 stabilization and DNA damage response activation
的研究论文。
该研究证实,MDM2直接促进MEIS1蛋白K178位点发生K48连接的多聚泛素化,从而导致其被蛋白酶体降解。值得注意的是,MEIS1能与MDM2和p53形成非竞争性三元复合物,有效促进泛素向自身转移,并阻止p53泛素化。
缺乏泛素化能力的MEIS1 K178R突变体无法抑制MDM2介导的p53泛素化,这证明了MEIS1自身泛素化与p53稳定化之间的机制联系。此外,在DNA损伤应答中,MDM2介导的MEIS1泛素化是p53激活的先决条件。
重要的是,一种模拟MDM2介导的泛素化基序的MEIS1衍生肽,能同时增强MEIS1和p53的稳定性,并抑制细胞增殖和肿瘤生长。综上所述,该研究结果确定MEIS1是一种竞争性获取泛素转移以保护p53的分子诱饵,并强调MEIS1泛素化可能成为重新激活p53依赖性肿瘤抑制功能的一个新治疗靶点。

DNA损伤是细胞完整性的主要威胁之一,可导致细胞死亡或基因组不稳定性,二者均促进肿瘤发生。p53蛋白常被称为“基因组守护者”,因其在检测DNA损伤和响应多种应激信号中发挥关键作用,能够启动细胞周期阻滞、细胞凋亡和衰老等过程。在正常细胞条件下,p53通过快速周转维持在低水平,以防止不必要的凋亡和衰老通路被激活。
然而,在DNA损伤时,p53趋于稳定化,导致其积累并转录多种靶基因(如p21和BAX),从而启动细胞周期阻滞和细胞凋亡。该调控通路的破坏在癌症中普遍存在,尤其在结直肠癌(CRC)中,p53功能失调促进肿瘤进展和治疗抵抗。鉴于其重要的肿瘤抑制功能,恢复p53功能成为一种具有前景的治疗策略。
MDM2是一种关键的E3泛素连接酶,通过泛素-蛋白酶体途径促进p53降解。它通过两种主要机制抑制p53:结合其转录结构域以阻断其活性,以及通过蛋白酶体促进其降解。值得注意的是,p53也能诱导MDM2表达,从而形成一个自我调节的反馈环路。
正常情况下,MDM2维持p53处于低水平。然而,在DNA损伤或细胞应激时,p53从MDM2介导的抑制中释放,使其得以积累并激活导致细胞周期阻滞和细胞凋亡的基因。关键在于,在p53被激活前,必须抑制MDM2介导的p53泛素化。尽管已发现多种p53调控机制,但抑制MDM2介导的p53泛素化以响应细胞应激而激活p53的具体过程仍不清楚。
恢复p53功能的主要策略包括抑制MDM2-p53相互作用或阻断MDM2的E3连接酶活性。尽管如此,由于潜在的毒性和需要平衡肿瘤抑制效应,MDM2抑制剂的临床应用仍面临挑战。此外,MDM2除p53外还参与多种底物的泛素化,这使其自身作为治疗靶点变得复杂。这些挑战凸显了理解p53稳定性调控机制的重要性,特别是MDM2在其众多底物中选择性靶向p53的机制。
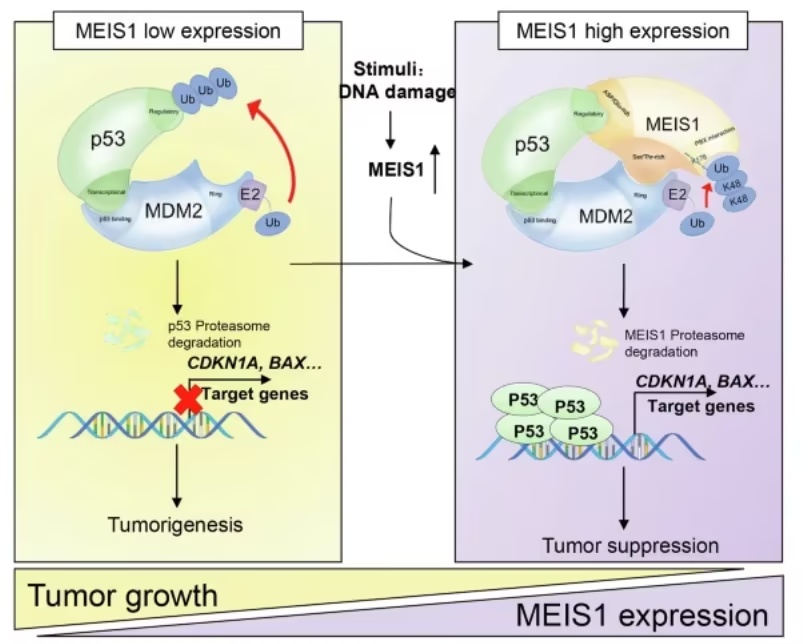
模式机理图(图片源自
Cell Death & Differentiation
)
MEIS1是一种含有同源结构域的转录因子,最初被确定为造血和发育的调节因子,但后来被发现与多种癌症相关。它促进急性髓系白血病、神经母细胞瘤和皮肤癌的进展,而在前列腺癌和非小细胞肺癌中则发挥抑制作用。先前研究表明,长链非编码RNA ELFN1-AS1与EZH2和DNMT3a相互作用,导致DNA甲基化和H3K27me3修饰,从而抑制MEIS1表达并增强其下游靶标FEN1。尽管MEIS1通过其转录活性与肿瘤进展相关,但调控其稳定性的翻译后机制仍知之甚少。
本研究旨在探究调控MEIS1蛋白稳定性的机制,并探索其在调节MDM2-p53轴中的潜在作用。作者发现MEIS1是MDM2的一个新型底物,并证明其可作为分子诱饵,与p53竞争MDM2介导的泛素化,从而阻止p53降解。具体而言,作者发现MEIS1在K178位点发生泛素化,该修饰对其自身降解和稳定p53至关重要。这一机制提示,MEIS1可能在结直肠癌中作为p53的保护因子,为超越直接抑制MDM2的p53稳定性调控提供了新见解。
此外,作者研究了MEIS1在DNA损伤应答中的作用,并证明在基因毒性应激下,MDM2介导的MEIS1泛素化对于p53激活必不可少。基于这些发现,作者设计了一种MEIS1衍生肽,通过增强MEIS1和p53的稳定性来抑制细胞增殖和肿瘤生长。综上所述,该研究结果为理解MEIS1、MDM2和p53之间的相互作用提供了机制框架,并强调了靶向MEIS1泛素化作为增强结直肠癌中p53依赖性肿瘤抑制策略的潜力。
原文链接:https://www.nature.com/articles/s41418-026-01714-9
