中山大学梁晓雨/马骏/唐玲珑合作最新NCB
细胞焦亡是否可控且可逆仍是一个未解之谜。
2026年3月9日,中山大学梁晓雨、马骏及唐玲珑共同通讯在
Nature Cell Biology
在线发表题为
TOLLIP targets GSDME-NT-carrying endocytic vesicles for autophagy to regulate pyroptosis and chemotherapy efficacy
的研究论文。
该研究揭示,自噬能够清除位于不同膜结构上的成孔GSDME N端片段(GSDME-NT),从而抑制细胞焦亡。关键机制在于,质膜上的GSDME-NT可通过内吞作用被清除,其中负载GSDME-NT的囊泡被作为完整单元靶向并降解。
具体而言,质膜上的GSDME-NT孔道可诱导内吞作用,产生携带GSDME-NT但具有渗漏性的内吞囊泡。囊泡渗漏阻碍了其酸化过程,因此需通过自噬进一步降解。内吞发生后,囊泡膜上的GSDME-NT被钙离子激活的E3泛素连接酶NEDD4L标记泛素化。
这些被标记的囊泡由TOLLIP识别,进而引导继发自噬体的形成,促进囊泡酸化、与溶酶体融合并最终降解GSDME-NT。此外,在多种肿瘤模型中,通过靶向TOLLIP干扰自噬或阻碍GSDME-NT囊泡的识别,均能增加肿瘤细胞的焦亡,从而激活抗肿瘤免疫并增强化疗疗效。
另外,2026年3月11日,中山大学孙颖、马骏、周冠群、李济宾共同通讯在
Nature
在线发表题为
Risk-adaptive therapy guided by dynamic ctDNA in nasopharyngeal carcinoma
的研究论文。该研究提出了一种利用动态ctDNA指导下进行鼻咽癌风险适应性治疗的新策略。
该研究启动了一项ctDNA驱动的风险适应性试验(EP-STAR),在该试验中,研究人员对早期新辅助治疗阶段的纵向ctDNA清除轨迹进行了前瞻性分析,以进行精细的风险分层,并指导随后的个体化治疗修改。

细胞焦亡是一种独特的程序性细胞死亡形式,其特征为细胞肿胀和细胞溶解。作为一种程序性细胞死亡,其核心问题在于该过程是否可控且可逆。值得注意的是,细胞焦亡在传递炎症信号中发挥着重要作用。细胞焦亡由gasdermin(GSDM)家族蛋白的N端(NT)形成的孔道所诱导。因此,了解孔道形成后GSDMs-NT的命运,不仅是揭示细胞焦亡可控性的关键,也是理解细胞死亡与炎症信号传递解耦的核心。
在人类中,已鉴定出GSDM家族的六个成员。从进化角度看,GSDME出现最早且表达广泛;它与细胞凋亡密切相关,并能够将caspase-3或颗粒酶B介导的细胞凋亡转变为细胞焦亡。鉴于此,在肿瘤背景下,强力诱导GSDME-NT介导的细胞焦亡对于重塑抗肿瘤免疫具有重要意义。
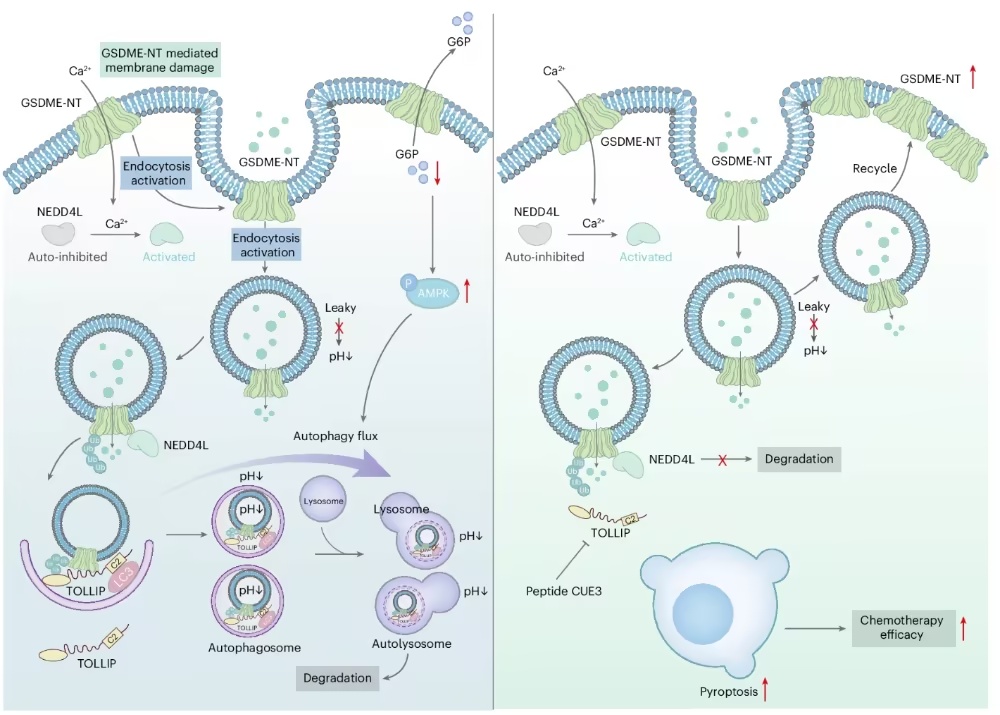
模式机理图(图片源自
Nature Cell Biology
)
GSDMs-NT孔道不仅形成于细胞质膜,也形成于多种膜性细胞器,从而导致损伤。自噬是一个受到严格调控的生物学过程,其特征是形成双层膜囊泡(自噬体),包裹细胞内的靶标(尤其是受损的细胞器或功能失调的蛋白质复合物),并将其递送至溶酶体进行消化。本研究发现,自噬在决定GSDME-NT的命运中起着决定性作用。具体而言,膜损伤诱导的自噬能够降解位于不同位置膜结构上的、已形成孔道的GSDME-NT。
质膜上GSDME-NT的降解最为关键。质膜上的孔道会诱导内吞作用,导致其以内吞囊泡的形式被内化,而囊泡的渗漏会阻碍其酸化过程。通过GSDME-NT孔道流入的钙离子激活了E3连接酶NEDD4L,后者介导了囊泡内GSDME-NT的泛素化修饰。
这些被标记的囊泡随后被选择性自噬受体TOLLIP(Toll相互作用蛋白)识别,并被整合到自噬膜结构中。通过这种“囊泡包被囊泡”的模式,酸化过程以及与溶酶体的融合得以恢复,最终导致GSDME-NT被降解。
原文链接:https://www.nature.com/articles/s41556-026-01902-2
