攻克“不可成药”靶点!《Nature》开发口服环肽,通过“推波助澜”机制选择性杀死小细胞肺癌
小细胞肺癌(SCLC)是一种侵袭性较强的肺癌亚型,目前尚缺乏有效的靶向治疗手段。SCLC中普遍存在 RB1 和 TP53 的功能缺失性突变,这会破坏 G1-S 检查点,并导致 E2F 活性失调。其他癌症同样通过 CDKN2A 的缺失或细胞周期蛋白 D 或细胞周期蛋白 E 的扩增来破坏 G1-S 检查点,这也导致了 E2F 活性的过度增强。
尽管 E2F 的激活对于细胞周期进程至关重要,但过度激活会促进细胞凋亡,从而呈现出一种治疗上的弱点。细胞周期蛋白利用一个保守的疏水性区域与带有短线性 RxL 基序的底物结合。细胞周期蛋白 A 通过依赖于 RxL 的相互作用抑制 E2F,当这种相互作用被破坏时,会过度激活 E2F。然而,这种底物界面一直难以靶向。

2025年8月20日,哈佛医学院Matthew G. Oser团队在
Nature
在线发表题为
Targeting G1–S-checkpoint-compromised cancers with cyclin A/B RxL inhibitors
的研究论文,该研究开发了细胞可渗透、口服生物可利用的环状肽,它们能够抑制细胞周期蛋白通过其与底物的 RxL 介导的相互作用而与底物结合。
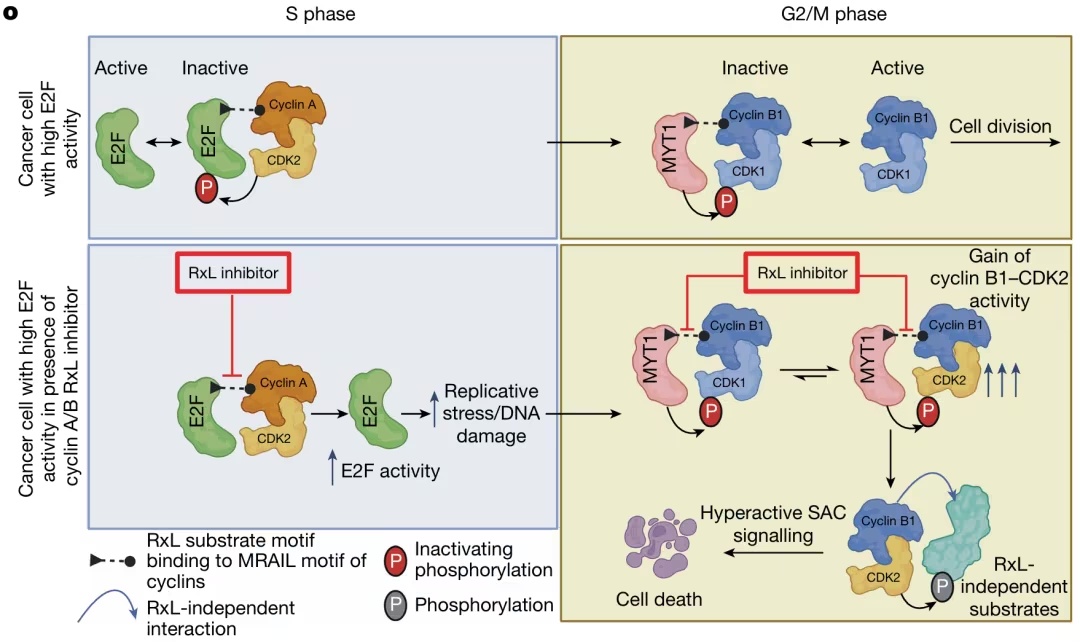
文章模式图(图源自
Nature
)
cyclin A/Bi(针对细胞周期蛋白 A 和细胞周期蛋白 B 的 RxL 基序)能够选择性地杀死 SCLC 细胞和其他具有高 E2F 活性的癌症细胞。基因筛选揭示,细胞周期蛋白 A/Bi 通过依赖于细胞周期蛋白 B 和 CDK2 的纺锤体组装检查点激活来诱导细胞凋亡。从机制上讲,细胞周期蛋白 A/Bi 通过阻断细胞周期蛋白 A - E2F 和细胞周期蛋白 B - MYT1 的相互作用,过度激活了 E2F 和细胞周期蛋白 B。
值得注意的是,细胞周期蛋白 A/Bi 促进了新的细胞周期蛋白 B - CDK2 复合物的形成,这种复合物能够驱动纺锤体装配检查点的激活以及有丝分裂细胞的死亡。最后,口服给药的细胞周期蛋白 A/Bi 在化疗耐药的 SCLC 患者来源的异种移植模型中显示出强大的抗肿瘤活性。这些发现揭示了细胞周期蛋白 A/Bi 引发细胞凋亡的致病机制,并支持其在 E2F 驱动的癌症中的开发应用。
参考消息:https://www.nature.com/articles/s41586-025-09433-w
