刚刚,诺华的自免大药“后手”来了!


3月19日,诺华宣布,其创新生物制剂奥马珠单抗预充式自动注射笔获得国家药品监督管理局批准,用于治疗采用H1抗组胺药治疗后仍有症状的成人和青少年(12岁及以上)慢性自发性荨麻疹(CSU)患者及确诊为IgE(免疫球蛋白E)介导的哮喘患者。


不用进医院,只需在家注射

奥马珠单抗是全球首个获批用于CSU治疗的生物制剂,作为一种抗IgE人源化单克隆抗体,通过靶向结合血清游离IgE,精准阻断IgE及其高亲和力受体通路,从源头抑制肥大细胞激活,阻断其脱颗粒及下游炎症反应。真实世界研究表明,奥马珠单抗快至当天起效,3个月93%患者可实现症状完全控制。
《中国难治性慢性自发性荨麻疹诊治指南(2025版)》明确推荐,对于抗组胺药整体使用时间2-4周后症状依然控制不佳的难治性CSU患者,可在医生综合评估下及时升级治疗策略,促进疾病的长期稳定控制。此次获批的全新自动注射笔设计帮助患者告别传统针头注射带来的不适感,让患者无需到院注射,在家就能轻松实现高效、精准、安全性可耐受的疾病管理。
奥马珠单抗于2017年在国内获批上市,自2019年被纳入国家医保目录后,该药的临床应用迅速拓展,销量逐年稳步攀升。
RPDB药品零售数据库显示,奥马珠单抗在国内药店的销售金额从2019年的约500万元快速增长至2025年突破3亿元,显示出强劲的市场增长势头。随着其全新自动注射笔剂型的推出,患者将能够更加便捷地进行居家注射,有望进一步推动该药物的临床普及与市场份额的提升。

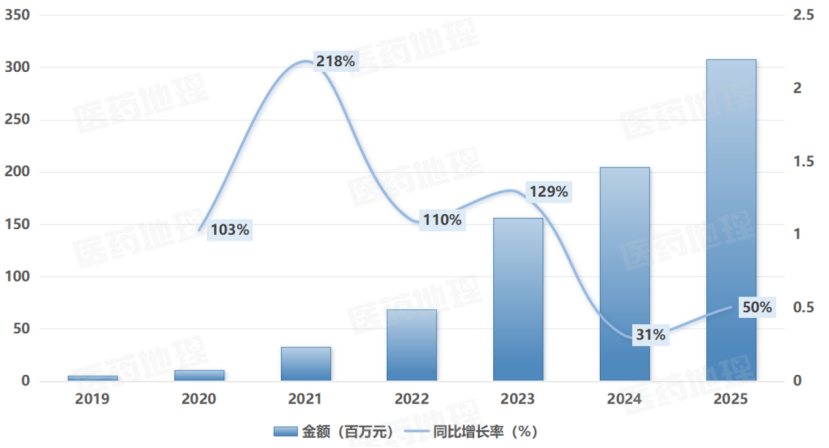
奥马珠单抗国内药店销售金额(2019-2025)
来源:RPDB药品零售数据库,中国医药工业信息中心
点击“阅读原文”获取更多数据
CSU领域,群狼环伺
诺华的奥马珠单抗全球上市超过20年,拥有多个剂型和适应症,在包括中国在内的90多个国家和地区被广泛使用,然而现已深陷专利悬崖。2026,十款重磅药物专利即将失效!
目前,韩国Celltrion公司的奥马珠单抗生物类似药已获得美国FDA批准,且覆盖其全部适应症。Pharma ONE药物研发大数据平台显示,在中国,多款国产生物类似药也已获批上市,包括泰州迈博太科药业和石药集团巨石生物的产品。其中,石药集团的生物类似药于2024年10月获批,成为国内首个获批的奥马珠单抗生物类似药,适用于经H1抗组胺药治疗后仍有症状的成人和青少年(12岁及以上)慢性自发性荨麻疹患者。

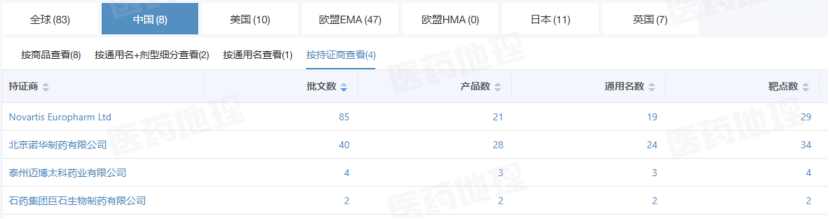
奥马珠单抗中国获批情况
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
今年3月,在美国过敏、哮喘与免疫学会年会(AAAAI 2026)上,天辰生物宣布其自主研发的新一代抗IgE抗体LP-003在CSU适应症的临床试验中“头对头”击败了奥马珠单抗,展现出成为同类最佳(Best-in-Class)药物的潜力。
此外济民可信研发的长效抗IgE单抗ozureprubart(RPT904)有望实现每季度给药一次,相比奥马珠单抗更能提高患者尤其是儿科患者的依从性。2024年,RAPT用最高7亿美元获得了该药物在中国以外地区的权益。而今年年初,GSK宣布收购RAPT,并向其支付每股58美元,估算总股权价值为22亿美元,同时获得ozureprubart大中华区外的全球权益。
别慌,诺华还留了后手
免疫治疗领域是诺华全球四大核心治疗领域之一,除了布局生物制剂,诺华也在口服小分子领域悄然落子,构建起“注射+口服”双重防线,进一步巩固其在CSU治疗领域的市场地位。
去年11月,诺华宣布其创新药物瑞普多®(瑞米布替尼片),一种高选择性共价结合BTK抑制剂,获得国家药品监督管理局批准,适用于H1抗组胺药控制不充分的成人慢性自发性荨麻疹患者。作为全球首个治疗CSU的口服靶向药,瑞米布替尼片的获批有望构建CSU治疗新格局。