中国药科大学涂家生等团队Science Bulletin!局部巨噬细胞启发的新型纳米疫苗凝胶:术后免疫治疗新突破

涂家生教授

外科手术作为实体瘤治疗的主要手段,虽然能直接切除肿瘤组织,但术后免疫抑制微环境常导致肿瘤复发和转移风险显著升高。这一现象与肿瘤相关巨噬细胞(TAMs)的动态行为密切相关。在正常组织修复过程中,巨噬细胞会经历从促炎性的M1表型向促进修复的M2表型转变,然而在肿瘤术后环境中,这一平衡被打破。中国药科大学与天津医科大学的研究团队通过系统分析小鼠模型发现,肿瘤切除后局部微环境中M1型TAMs的主导期异常短暂,仅维持约2天,远低于建立有效抗肿瘤免疫所需的7-10天窗口。同时,M2型TAMs中溶酶体功能过度活跃,导致吞噬的肿瘤抗原被快速降解,严重削弱了抗原交叉递呈能力和CD8+ T细胞的活化。这一发现不仅揭示了术后免疫失败的关键机制,还为开发针对性干预策略提供了重要理论基础。研究强调,延长术后炎症期并调控巨噬细胞表型转换,是提升抗肿瘤免疫效果的核心环节。
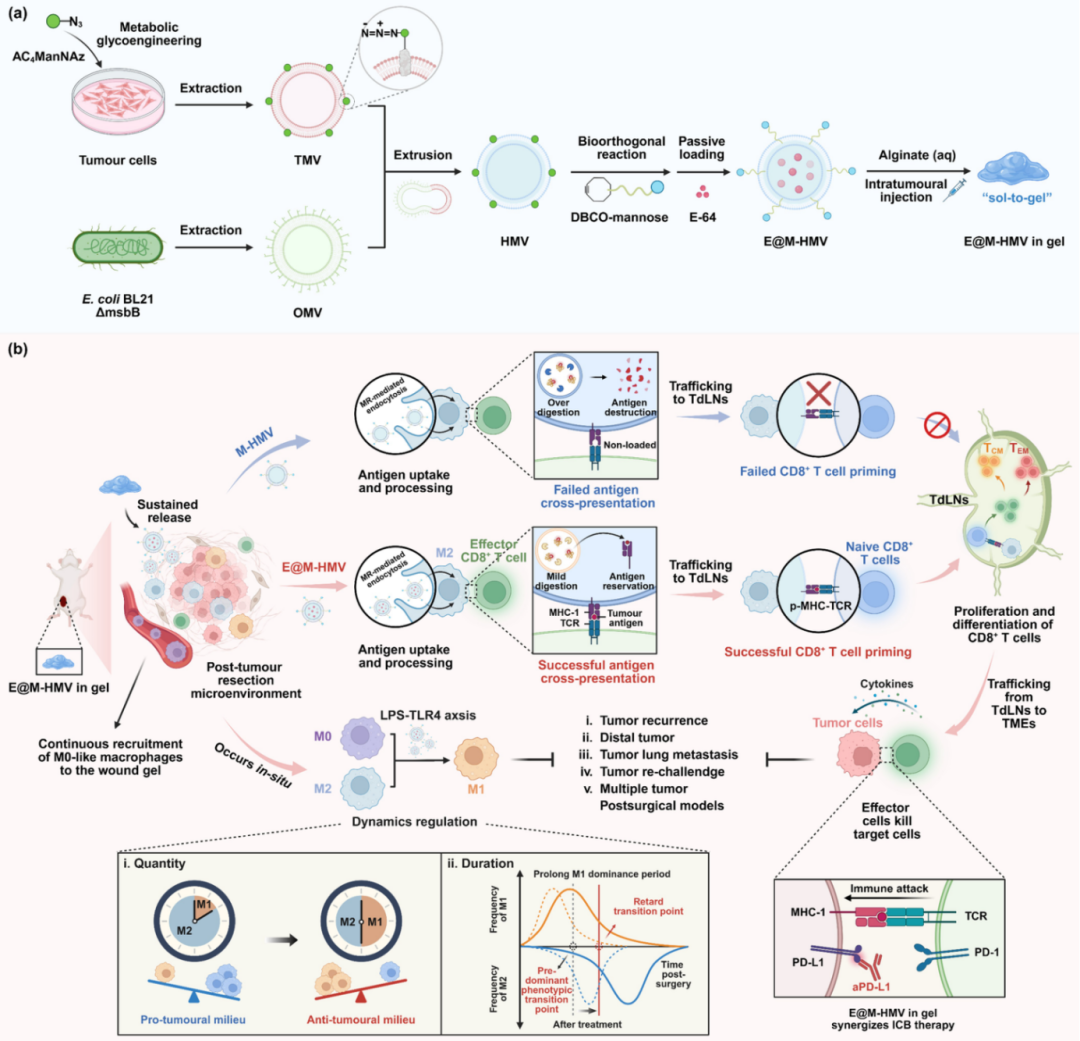
基于上述发现,研究团队设计了一种时空可控的纳米疫苗凝胶系统(E@M-HMV in gel)。该系统的核心在于融合细菌外膜囊泡(OMV)与肿瘤细胞膜囊泡(TMV),形成杂化膜囊泡(HMV),从而整合免疫佐剂和肿瘤抗原的双重功能。通过代谢糖工程技术,在HMV表面修饰甘露糖(M-HMV),实现对M2型TAMs的高效靶向。此外,囊泡内部装载了半胱氨酸蛋白酶抑制剂E-64,用于抑制溶酶体的过度降解活性。整个纳米结构被嵌入海藻酸盐水凝胶中,形成可注射的缓释载体,能在术后局部持续释放疫苗成分超过一周,模拟自然感染过程中的抗原暴露模式。这种设计不仅延长了M1型TAMs的活化期,还通过调节溶酶体功能,挽救M2型细胞的抗原递呈能力。该系统制备工艺简便,且抗原成分可根据不同肿瘤类型灵活替换,展现出良好的通用性和可扩展性。
在实验验证中,E@M-HMV in gel展现出多方面的抗肿瘤效果。体外研究表明,甘露糖修饰的纳米疫苗能特异性被M2型巨噬细胞内化,并有效将其重塑为M1表型,促进肿瘤坏死因子-α(TNF-α)和白细胞介素-12(IL-12)等促炎因子的分泌。体内实验进一步证实,在4T1乳腺癌、HC22肝癌和CT26结肠癌等多种模型中,该凝胶系统能显著抑制局部肿瘤复发和远端转移,延长模型动物的生存期。机制上,治疗组术后微环境中M1/M2巨噬细胞比例大幅提高,CD8+效应记忆T细胞浸润增强,建立了系统性免疫记忆。尤其值得注意的是,该疫苗能与抗PD-L1等免疫检查点阻断疗法协同作用,将“冷”肿瘤转化为“热”肿瘤,实现肿瘤完全消退和长期防护。这一技术为解决实体瘤术后高复发难题提供了创新思路,具有重要的临床转化前景。
信息来源:医学研究前沿




免责声明
“汇聚南药”公众号所转载文章来源于其他公众号平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请在留言栏及时告知,我们会在24小时内删除相关信息。
本平台不对转载文章的观点负责,文章所包含内容的准确性、可靠性或完整性提供任何明示暗示的保证。
喜欢的点个“看一看”和"喜欢"吧

不然微信推送规则改变,有可能每天都会错过我们哦~
