ACS Nano:沈阳药科大学罗聪等团队设计低炎症脂质纳米粒靶向肺部蓄积并沉默黏蛋白5AC用于哮喘治疗
黏蛋白5AC(MUC5AC)的过度表达会导致黏液分泌亢进与气道阻塞,进而增加重症哮喘及黏液阻塞性肺疾病(MOLDs)的死亡率。
2026年3月8日,沈阳药科大学罗聪、北京大学苗蕾和周健共同通讯在
ACS Nano
在线发表题为
Lung-Accumulating Mucin 5AC Silencing by Noninflammatory Lipid Nanoparticles for Asthma Treatment
的研究论文。
尽管基于siRNA沉默MUC5AC表达是治疗黏液阻塞性肺疾病的有效策略,但该研究发现,经气管给予FDA已批准的脂质纳米粒(LNP)载体时,其炎症副作用反而会导致MUC5AC表达异常升高。为解决这一难题,作者通过(1)开发低免疫原性的可电离阳离子脂质;(2)将抗炎天然产物衍生物掺入脂质纳米粒中;(3)降低脂质纳米粒制剂的N/P比率,设计了适用于哮喘治疗的低炎症反应脂质纳米粒。
经过三轮筛选——综合评估基因沉默效率(体内与体外)、脂质纳米粒理化性质及生物安全性,获得最优候选制剂。该制剂在体内实现85%的MUC5AC沉默效率,显著优于整合素αvβ6配体修饰siRNA的69%;与SM102-LNP及MC3-LNP相比,其生物安全性也得到显著提升。屋尘螨(HDM)诱导的哮喘小鼠模型中,siMuc5ac-LNP可有效缓解气道炎症与阻塞,并表现出持久的预防效果。
此外,制剂1在慢性阻塞性肺疾病(COPD)患者来源的类器官模型中,也能显著抑制MUC5AC的分泌。综上,该研究构建了一种具备临床转化潜力的低炎症siRNA递送平台,在哮喘及其他黏液阻塞性肺疾病中具有重要治疗价值。

黏液阻塞性肺疾病(MOLDs)包括哮喘、慢性阻塞性肺疾病(COPD)和囊性纤维化(CF),对人类健康构成严重威胁。炎症引发的黏液过度分泌会导致气道狭窄与呼吸阻塞,甚至可能造成致命后果。目前的治疗手段如抗炎药与支气管扩张剂,在抑制黏液分泌方面疗效有限。
此外,以N
乙酰半胱氨酸为代表的黏液溶解剂也难以实现长期有效治疗。因此,亟需开发能够长效抑制异常黏液分泌的治疗策略。黏蛋白5AC(MUC5AC)是一种可诱导的凝胶形成型黏蛋白,主要由肺部气道表面上皮中的杯状细胞产生。在哮喘及其他黏液阻塞性肺疾病中,炎症刺激会触发MUC5AC过度表达,导致黏液分泌亢进、小气道阻塞、黏液纤毛清除功能受损,进而引发呼吸功能障碍。因此,抑制MUC5AC过表达是治疗黏液阻塞性肺疾病的有效策略。
RNA干扰(RNAi)治疗为调控肺部蛋白表达提供了极具前景的手段,其可沉默几乎任意靶基因以实现治疗效果。然而,裸露siRNA体内稳定性差、细胞摄取效率低、内体逃逸受限,使其难以有效递送至靶部位。
纳米递送系统在多种治疗应用中展现出显著优势,性能优于传统制剂。对于siRNA递送,纳米载体平台具有三大核心优势:一是保护siRNA在循环和器官内免受核酸酶降解;二是可通过表面修饰实现组织或细胞特异性靶向;三是借助内体逃逸机制增强胞质递送效率。
脂质纳米粒(LNPs)是目前唯一获得临床批准的RNA递送载体,其安全性与有效性已得到充分验证。值得注意的是,首个获FDA批准的RNAi药物patisiran已成功用于治疗遗传性转甲状腺素蛋白介导的淀粉样变性。然而,黏液阻塞性肺疾病属于炎症性疾病,外界炎症刺激会进一步加重疾病进展。
遗憾的是,脂质纳米粒本身具有固有的免疫原性。局部给药后,LNPs会招募免疫细胞(如中性粒细胞、巨噬细胞)并促发促炎细胞因子释放(如IL
6、TNF
α),加剧炎症反应,表现为疼痛、肿胀、发热、乏力等典型症状。因此,降低LNPs诱发的炎症反应,对于其在黏液阻塞性肺疾病治疗中的应用至关重要。
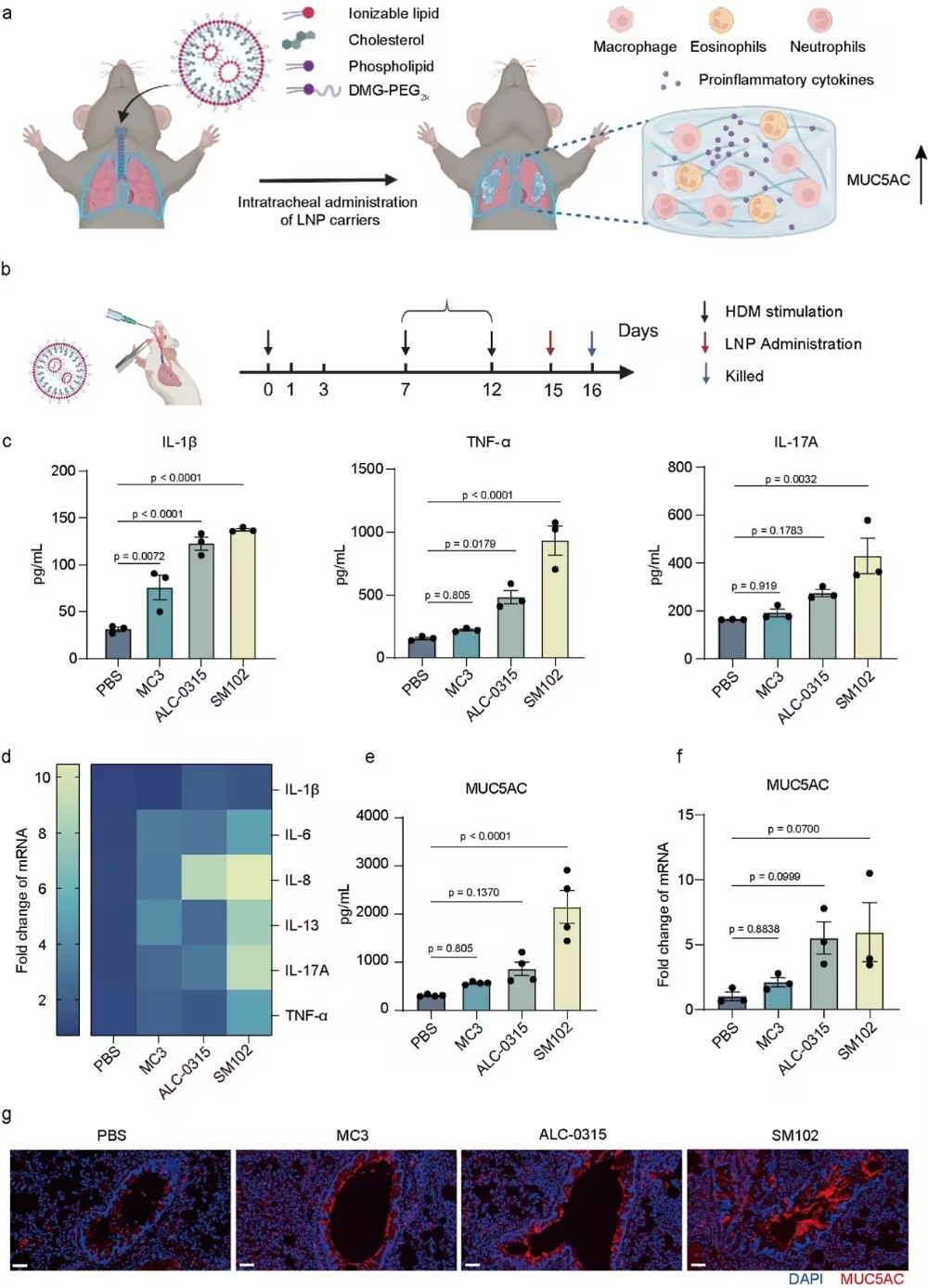
图1 LNP载体在哮喘小鼠气管内给药后诱导肺部炎症并加剧MUC5AC表达(摘自
ACS Nano
)
该研究发现,经气管给予市售LNP制剂会诱导促炎细胞因子释放,进而在基因与蛋白水平上调MUC5AC表达。为克服LNPs对MUC5AC沉默效率的限制,作者设计了低免疫原性LNPs,用于哮喘及其他黏液阻塞性肺疾病中的MUC5AC沉默。
该策略包括筛选五种可电离阳离子脂质,并将抗炎天然产物衍生物作为第五组分掺入LNPs中。同时,我们将制剂的氮磷比(N/P)从6:1降至3:1,以减少总脂质含量,在保持siRNA包封率高于85%及良好理化性质的前提下,提升LNPs的生物相容性。
通过系统筛选,确定了制剂1——一种熊果酸(UA)修饰的LNP,其在体内实现85%的蛋白敲低效率,优于整合素αvβ6配体修饰siRNA的69%。值得注意的是,即使以1 mg/kg siRNA剂量经气管滴注给药,制剂1仍表现出优异的生物安全性,体内分布研究证实其可高效将siRNA递送至杯状细胞。
在屋尘螨(HDM)诱导的哮喘小鼠模型中,制剂1展现出强大的治疗与预防效果,包括减少巨噬细胞、中性粒细胞和嗜酸性粒细胞浸润,降低IL
13与IL
17A水平,并缓解肺部气道阻塞。此外,在慢性阻塞性肺疾病患者来源的类器官模型中,制剂1可有效抑制MUC5AC表达。该研究开发了一种低炎症RNA递送平台,为高效沉默炎症相关基因、推动黏液阻塞性肺疾病治疗进展提供了具备临床转化潜力的策略。
参考消息:https://pubs.acs.org/doi/10.1021/acsnano.5c16693
