Biomaterials:康复大学陈刚团队设计工程化噬菌体纳米组装体稳定DC-T细胞免疫突触以实现高效流感疫苗接种
树突状细胞(DCs)对T细胞的激活需要形成稳定的免疫突触(IS)。
2026年3月6日,康复大学陈刚、南京中医药大学曹鹏、扬州大学郇长超共同通讯在
Biomaterials
上在线发表题为
Engineered bacteriophage nanoassemblies in vivo stabilize DC–T cell immune synapse for high-performance influenza vaccination
的研究论文。
该研究开发了一种通过在体内靶向调控DC-T细胞突触相互作用的疫苗策略。作者构建了噬菌体纳米组装体,将抗原编码序列递送至DC细胞质中,并在体内增强DC-T细胞免疫突触的稳定性,从而提升疫苗效果。
具体而言,作者将流感血凝素干基因插入噬菌体基因组,并将DC靶向肽融合至噬菌体侧壁。随后,噬菌体作为表面活性剂包裹疏水性颗粒,颗粒内部包载钠/质子泵抑制剂,以调控细胞间黏附分子1(ICAM-1)的膜定位,从而稳定免疫突触。尺寸可控的纳米组装体通过激活NF-κB、PI3K-AKT和RhoA-ROCK信号通路,抑制ICAM-1的内化。纳米组装体免疫可触发强烈的抗流感病毒T细胞和抗体应答,为感染小鼠提供完全保护,并诱导长期免疫记忆。
综上,研究结果证实,通过在体内靶向增强DCs与T细胞之间的免疫突触稳定性,可有效提升疫苗的保护效果。该噬菌体纳米组装体具有灵活性和通用性,可轻松改造用于开发针对其他病原体的多种疫苗制剂。

核酸疫苗作为前沿生物技术创新,在治疗和预防应用中展现出巨大潜力。然而,有效递送是实现其免疫效果的关键,而这在很大程度上依赖于递送平台的设计。
尽管近年来以脂质纳米颗粒递送mRNA疫苗为代表的非病毒载体备受关注,但仍存在一些不可避免的挑战限制其广泛应用,如肝外靶向和细胞质递送困难,甚至在接种后引发疼痛和炎症。用于核酸疫苗递送的真核病毒载体(尤其是腺病毒平台)也面临诸多挑战,包括致癌风险、遗传毒性等安全性问题。此外,核酸疫苗的生产、运输和储存条件严苛,迫切需要开发高效、安全、便捷的载体以推动其发展。
M13噬菌体是一种原核病毒纳米纤维,具有可修饰的基因组和可扩展的表面结构,已逐渐在核酸递送和肽展示方面展现出巨大潜力。其基因组具有高度可塑性和可操作性,通过基因工程不仅可使M13噬菌体成为核酸递送载体,还能在病毒表面展示特异性靶向基团或抗原。
此外,M13噬菌体基因组富含胞嘧啶-磷酸-鸟嘌呤(CpG)基序,使其具有佐剂效应。这种多功能性使得噬菌体作为递送系统时,既能作为载体递送疫苗,又能作为佐剂增强免疫应答,从而在疫苗开发中具有独特优势。与真核病毒不同,噬菌体(通常称为原核病毒)具有宿主特异性,仅能感染特定菌株的细菌。
因此,它们无法感染哺乳动物细胞,确保了其作为治疗剂时具有良好的安全性。此外,噬菌体成本低廉,可通过细菌在数小时内大规模生产,适合广泛应用。
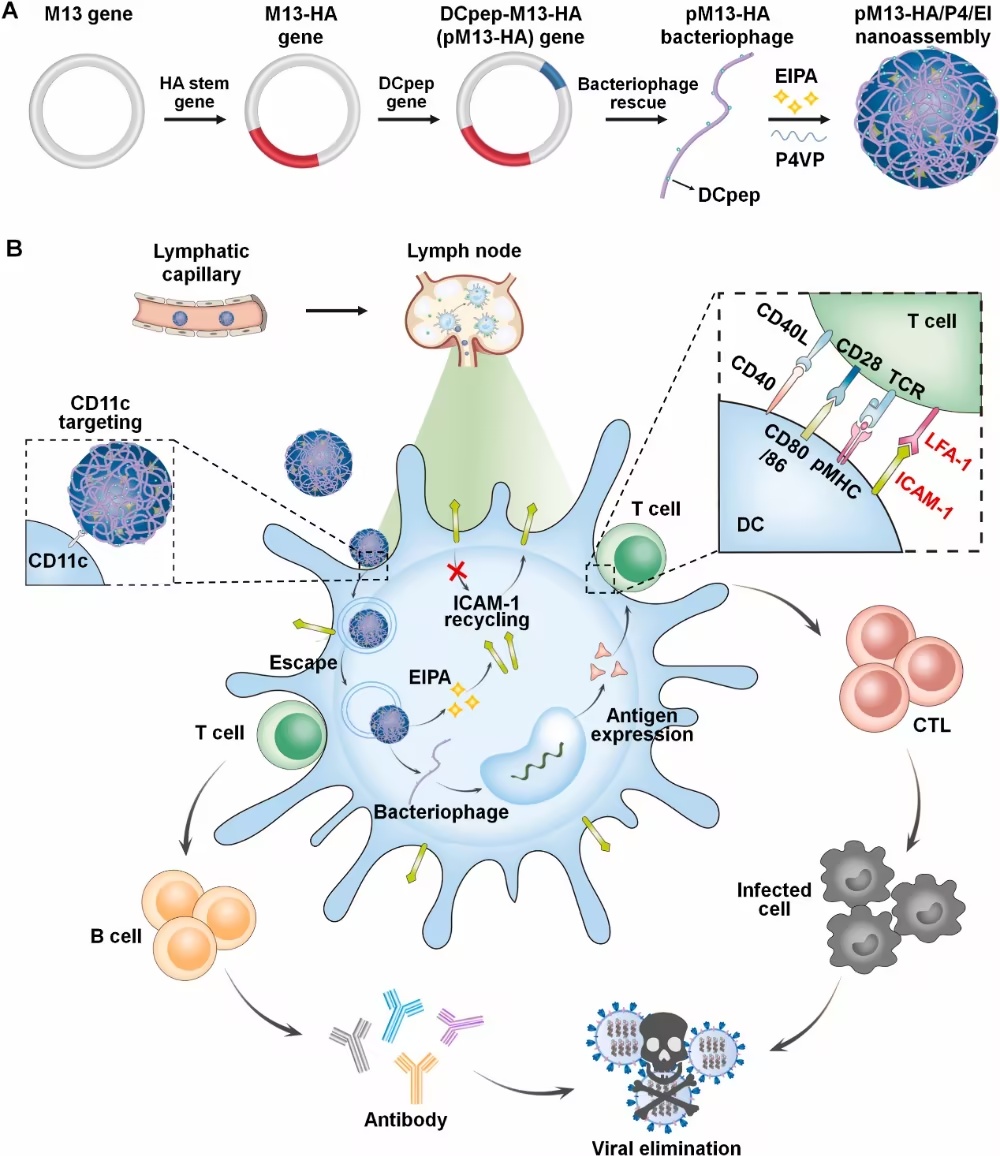
图1 基于M13噬菌体的纳米组装体的制备及作用机制示意图(摘自
Biomaterials
)
树突状细胞(DCs)作为最强大的抗原呈递细胞,在T细胞免疫应答的激活中发挥着关键作用,是疫苗递送的靶细胞。除了调控DC成熟和抗原呈递外,DC-T细胞相互作用也是提升疫苗效果的重要途径。已有研究表明,糖聚合物修饰的DCs可增强DCs与T细胞之间的黏附性,从而提高DC疫苗的效果。DCs与T细胞之间的结合强度直接决定抗原呈递效率及后续T细胞激活。
DCs表面的细胞间黏附分子1(ICAM-1)与T细胞表面的淋巴细胞功能相关抗原1(LFA-1)结合,在DC-T细胞界面形成免疫突触(IS),这一过程在DC-T细胞簇的聚集过程中发挥关键作用。在免疫突触内,TCR-肽-MHC复合物周围的ICAM-1/LFA-1结合可稳定DC-T细胞界面,促进T细胞活化。此外,ICAM-1会持续内化并循环回到免疫突触界面,改善ICAM-1的膜定位有助于稳定免疫突触稳定性,进而促进DC-T细胞相互作用。
在疫苗相关研究中,经氧化石墨烯纳米片修饰的DC疫苗可通过调控ICAM-1的膜定位增强免疫突触形成,从而提高疫苗效果。然而,尽管体外制备的DC疫苗已有诸多进展,但如何在体内靶向增强免疫突触稳定性以提升疫苗效果,相关研究仍较为匮乏。
该研究利用M13噬菌体,同时实现了核酸疫苗递送和DC-T细胞免疫突触稳定。首先,通过基因工程改造M13噬菌体,使其携带流感病毒血凝素(HA)干基因,并在侧壁展示DC靶向肽。随后,经改造的噬菌体与聚(4-乙烯基吡啶)(P4VP)自组装形成核-壳结构纳米组装体,并包载钠/质子泵抑制剂以增加ICAM-1的膜定位,从而有助于稳定免疫突触。
结果表明,噬菌体纳米组装体通过促进DC-T细胞免疫突触稳定,显著提高了DC抗原呈递效率和T细胞激活水平。通过多项体内实验,作者验证了噬菌体纳米组装体对流感病毒感染模型的有效保护作用。该研究为基于工程化噬菌体制剂,通过体内靶向增强免疫突触稳定性以提升疫苗效果提供了新途径。
参考消息:https://www.sciencedirect.com/science/article/pii/S0142961226001377?via%3Dihub
