Int J Mol Sci:宫颈小细胞癌类器官模型问世,HPV18整合驱动MYC激活揭示治疗新靶点

说起宫颈癌,大家往往想到的是发病率最高的鳞癌和腺癌。但在临床上,还有一种极其凶险的亚型——宫颈小细胞神经内分泌癌(SCNEC),虽然只占所有宫颈癌的2%至5%,但其早期转移率高达40%以上,五年生存率仅30%左右,远低于普通宫颈癌的65%以上。由于病例稀少,目前对这种肿瘤的研究十分有限,临床治疗也多依赖经验性用药,缺乏
精准
策略。近日,一项发表于
Int J Mol Sci
的研究为这一困境带来了转机。

来自日本岛根大学等机构的研究团队成功从一位41岁宫颈SCNEC患者活检组织中建立了类器官和球状体培养体系,并将其移植到
免疫
缺陷小鼠体内,构建了“患者肿瘤-类器官-异种移植瘤”三模型平台。这一平台不仅忠实再现了原始肿瘤的病理特征,还在基因组层面验证了模型的稳定性。
研究发现,类器官在培养中生长旺盛,冻存复苏后仍能保持形态和功能。病理染色显示,类器官和移植瘤完整保留了SCNEC的特征:细胞呈小圆形态、胞浆稀少,免疫组化显示CD56、突触素和神经元特异性烯醇化酶阳性,Ki-67增殖指数高达80%以上,而p53表达微弱,p16则呈现强阳性,提示与高危型HPV感染密切相关。
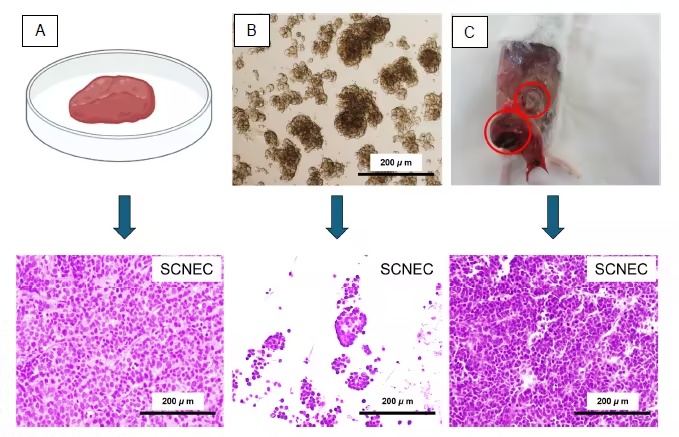
图1:SCNEC组织病理学特征在患者肿瘤、类器官及移植瘤中保持一致
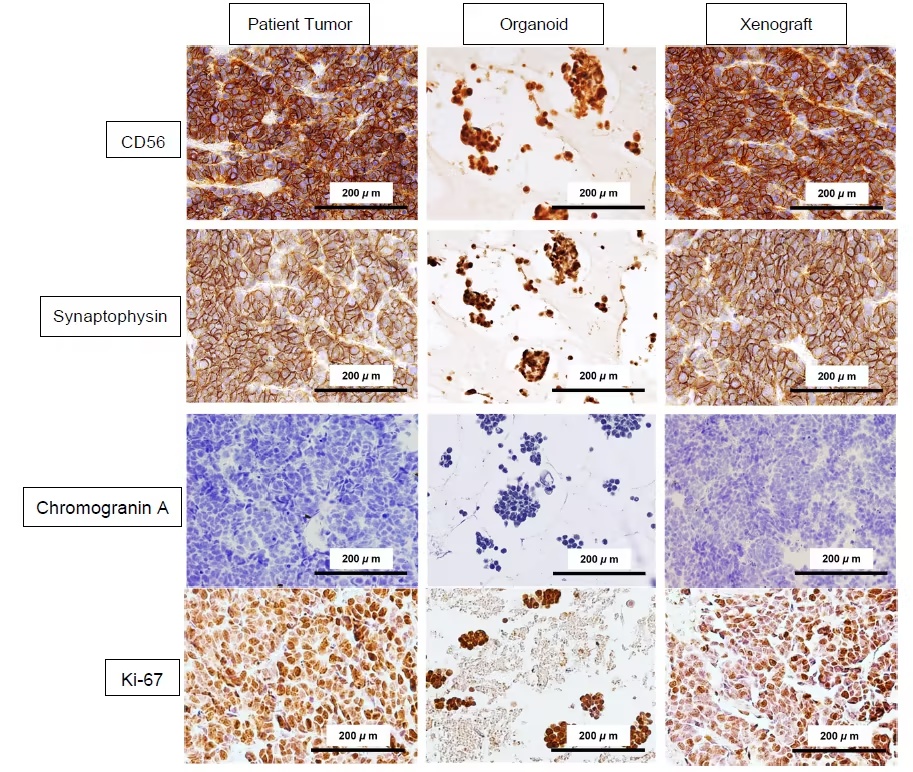
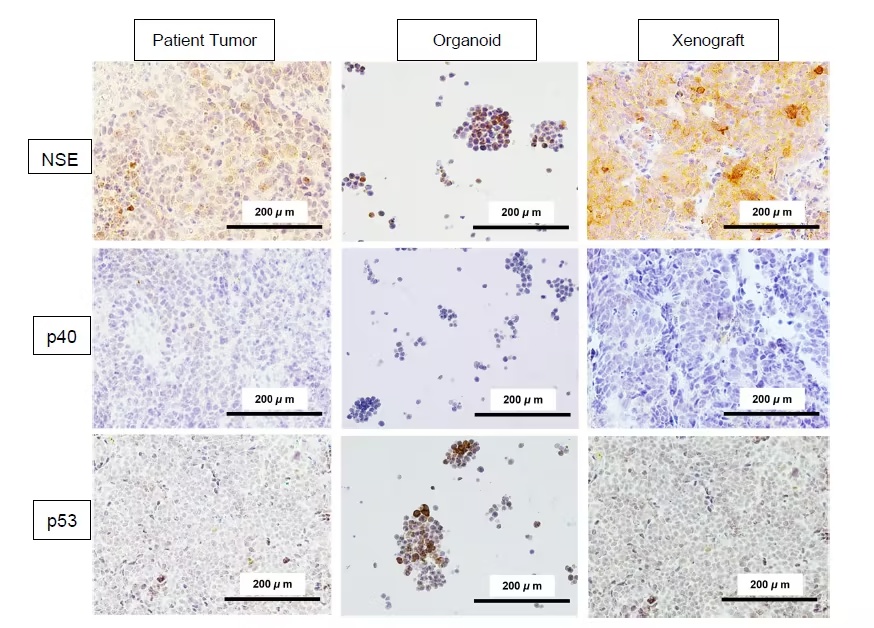
图2:免疫表型验证显示神经内分泌标志物在各模型中表达一致
全外显子组测序显示,三模型间存在26个共享的体细胞变异,包括PIK3CA基因的经典激活突变p.E542K,以及MYC、TERT等基因的拷贝数扩增,同时伴有TP53拷贝数缺失。这些变异在患者原始肿瘤、类器官和移植瘤中高度一致,证实了模型的基因组保真度。
在HPV状态方面,三模型均呈现p16强阳性,PCR检测确认HPV18阳性。进一步通过测序数据分析发现,HPV18基因组整合在8号染色体的8q24.21区域,邻近MYC基因。这一整合位点与HeLa细胞中的HPV18整合位点一致,提示病毒整合可能通过激活MYC表达促进肿瘤恶性进展。值得注意的是,移植瘤中还出现了一个额外的整合位点11q14.1,提示在体内扩增过程中可能发生了克隆演化。
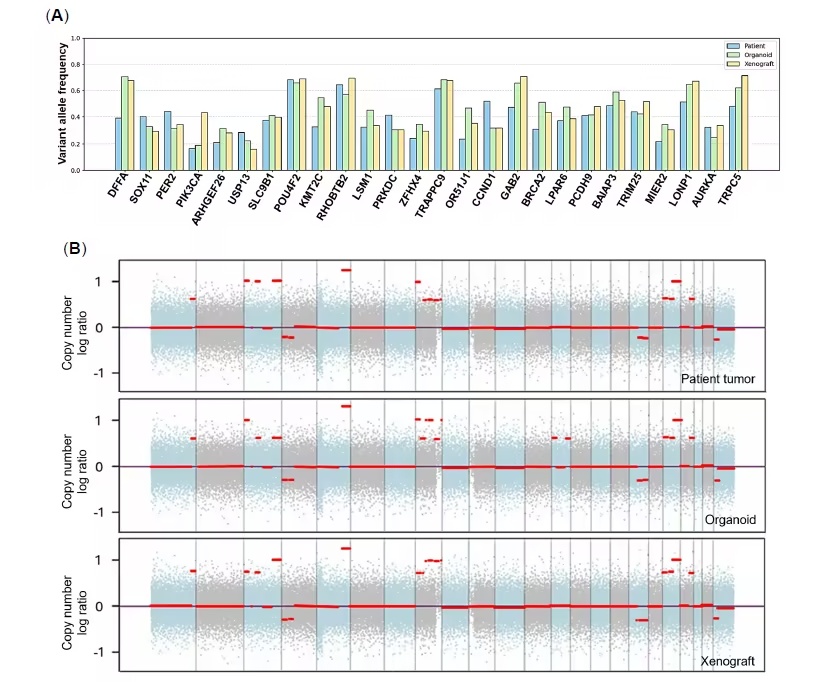
图3:全外显子测序显示三模型间体细胞变异及拷贝数变化高度一致
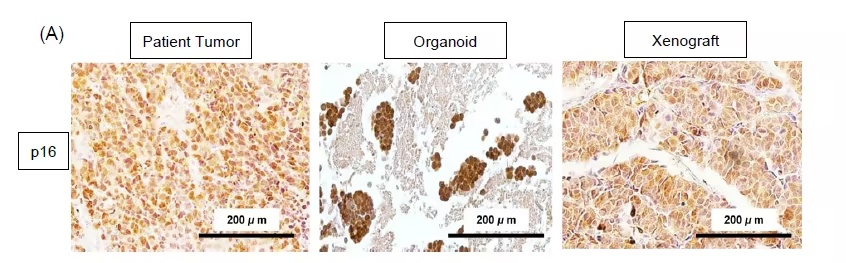
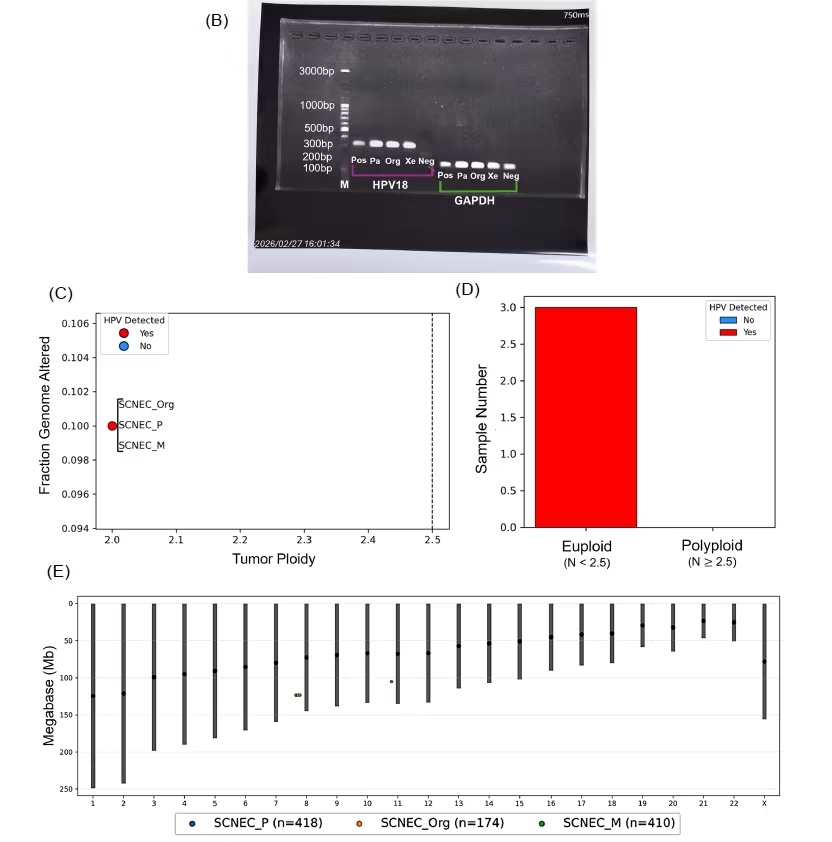
图4:HPV18整合及基因组稳定性在三模型中保持一致
在药物敏感性实验中,研究团队用紫杉醇、顺铂、
卡铂
、依托泊苷、奥拉帕利和依维莫司分别处理类器官和球状体。结果显示,作用72小时后,除依维莫司外,其余药物均表现出剂量依赖性的细胞活力抑制。其中紫杉醇的半数抑制浓度最低,约为0.34 μM,显示出较强的体外活性。
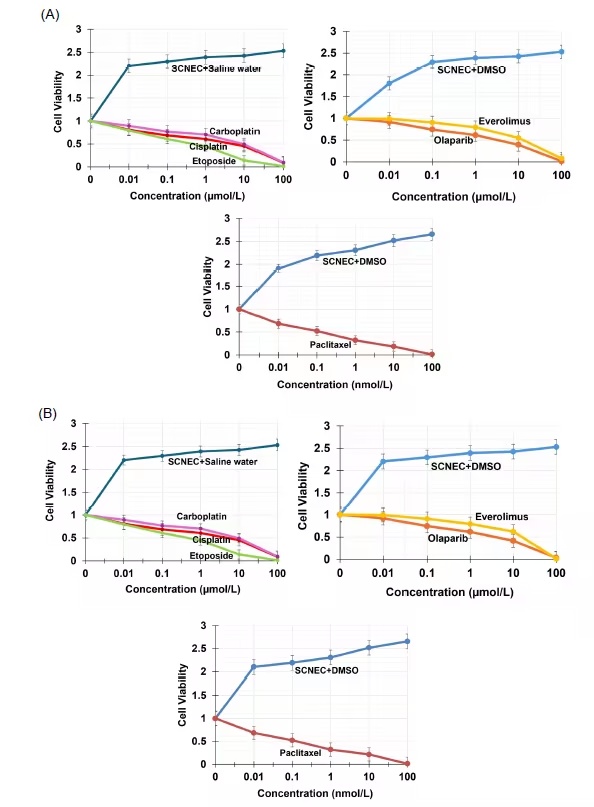
图5:类器官及球状体对临床常用药物呈现剂量依赖性反应
综上,该研究首次在宫颈SCNEC中建立了集患者原始肿瘤、类器官和移植瘤于一体的三模型平台,完整保留了HPV整合、PIK3CA突变、MYC扩增等关键分子事件,并成功用于药物敏感性评估。这一平台为研究这一罕见但高度恶性的肿瘤提供了可靠的实验工具,也为未来个体化治疗策略的探索奠定了基础。(
生物谷)
参考文献:
Sohel HI, Zahan UF, Ishikawa M, et al. Integrated Molecular and Functional Characterization of Cervical Small-Cell Neuroendocrine Carcinoma Using a 3D Organoid Model.
Int J Mol Sci
. 2026;27(5):2393. Published 2026 Mar 4. doi:10.3390/ijms27052393
