中国药科大学肖易倍、陆美玲Molecular Cell!!解析CRISPR-Cas9记忆形成的关键结构机制
CRISPR-Cas系统是原核生物中一种重要的适应性免疫机制,通过将外源DNA片段(称为前间隔序列)整合到宿主基因组中的CRISPR阵列,赋予细胞对特定病原体的记忆能力。在这一系统中,II-A型CRISPR-Cas9因其在基因组编辑中的广泛应用而备受关注,但其间隔序列获取的具体机制,尤其是Cas9蛋白如何参与这一过程,仍存在许多未解之谜。间隔序列获取是CRISPR免疫的第一步,涉及Cas1-Cas2整合酶复合物将外源DNA片段插入CRISPR阵列,但II-A型系统缺乏Cas4蛋白,而Cas1本身无法识别原间隔序列邻近基序(PAM),这导致PAM识别和间隔序列选择如何耦合的问题长期悬而未决。中国药科大学肖易倍教授团队与合作者的最新研究针对这一空白,通过结构生物学方法揭示了Cas9在II-A型系统中导向间隔序列获取的分子基础。这项研究不仅填补了CRISPR-Cas系统基础理论的关键漏洞,还为理解适应性免疫的进化提供了新视角,对开发更精准的基因编辑工具具有潜在意义。该成果以封面形式发表于《Molecular Cell》期刊,凸显了其重要性。
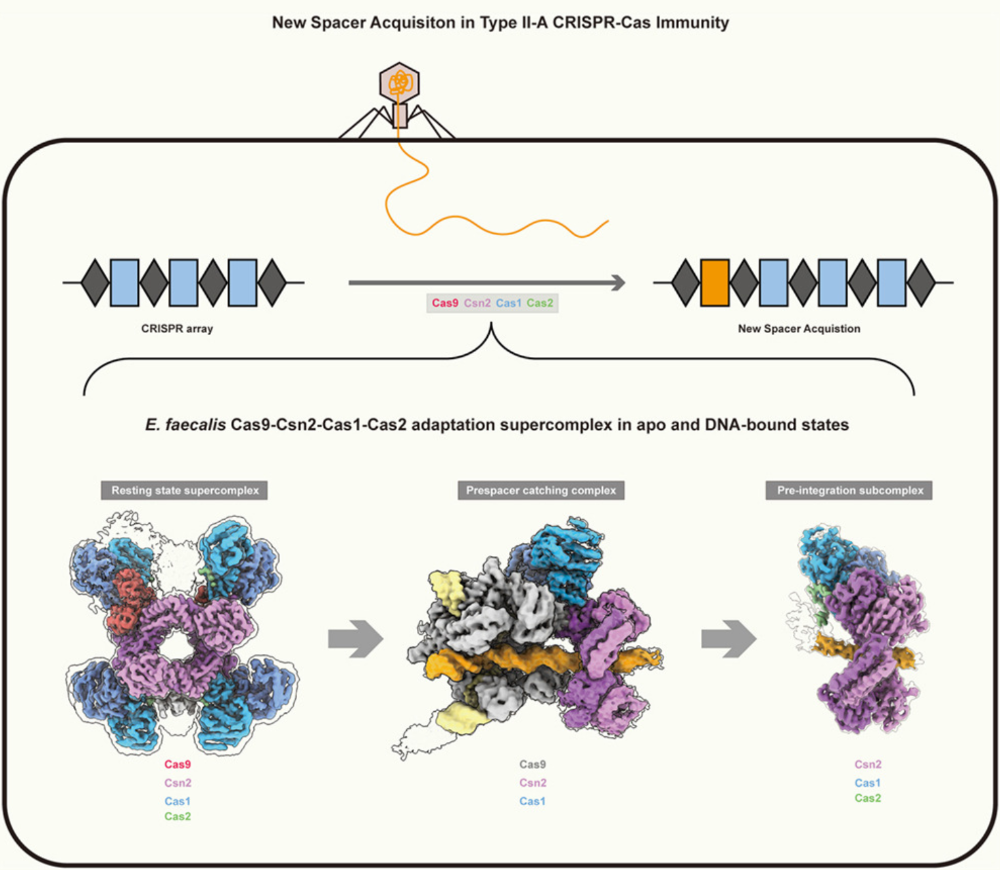
研究团队利用冷冻电镜技术解析了粪肠球菌来源的Cas9-Csn2-Cas1-Cas2超复合物在两种状态下的高分辨率结构:一是非结合状态的静息复合体(Cas9₂-Csn2₈-Cas1₈-Cas2₄),二是DNA结合状态的前间隔序列捕获复合体。结构分析表明,在DNA结合后,复合物发生构象变化,使DNA穿过Csn2蛋白的中央通道,从而允许Cas9沿DNA滑动并探查PAM序列。Cas9与Csn2共同界定了一段30碱基对的DNA区域,其长度与典型的前间隔序列匹配,确保了间隔序列选择的特异性。进一步实验显示,Cas9的解离会触发Csn2-Cas1-Cas2组装体的结构重排,暴露出PAM邻近的DNA区域,使得Cas1-Cas2整合酶能够结合该位点,启动后续的定向整合过程。这些发现首次在原子水平展示了Cas9如何与Csn2、Cas1-Cas2协同工作,将PAM识别与前间隔序列处理相耦合,从而保证间隔序列获取的保真性和效率,避免了自我靶向的风险。
该研究的发现具有重要的理论价值和应用潜力。从机制层面看,它阐明了II-A型CRISPR-Cas系统中Cas9的直接参与作用,解决了长期以来关于PAM识别如何引导间隔序列获取的争议,为CRISPR免疫的进化研究提供了结构基础。此外,这项成果可能推动基因组编辑技术的优化,例如通过模拟自然界的间隔序列获取机制,设计更高效、更特异的基因编辑工具。研究团队包括中国药科大学和新加坡国立大学的多位学者, work 得到了国家重点研发计划等项目支持,体现了国际合作的协同效应。未来,基于这一结构模型,可以进一步探索CRISPR-Cas系统在其他生物中的变体,或开发针对特定疾病的 therapeutic 应用。总体而言,这项研究不仅深化了对原核生物免疫机制的理解,也为生物技术领域带来了新的灵感。
信息来源:医学研究前沿




免责声明
“汇聚南药”公众号所转载文章来源于其他公众号平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请在留言栏及时告知,我们会在24小时内删除相关信息。
本平台不对转载文章的观点负责,文章所包含内容的准确性、可靠性或完整性提供任何明示暗示的保证。
喜欢的点个“看一看”和"喜欢"吧

不然微信推送规则改变,有可能每天都会错过我们哦~
