化妆品与皮肤科学 | 广东省面膜类化妆品生产企业GMP 检查缺陷分析及对策

引用本文



王焕,吴生齐∗,李晓莹,詹春燕,叶舜旻.广东省面膜类化妆品生产企业GMP检查缺陷分析及对策[J].中国食品药品监管.2026.02(265):136-142.
广东省面膜类化妆品生产企业GMP 检查缺陷分析及对策
Analysis of GMP Inspection Deficiencies and Countermeasures in Facial Mask Cosmetic Manufacturers in Guangdong Province
王焕
广东省药品监督管理局审评认证中心
WANG Huan
Evaluation and Certification Center, Guangdong Medical Products Administration
吴生齐∗
广东省药品监督管理局审评认证中心
WU Sheng-qi∗
Evaluation and Certification Center, Guangdong Medical Products Administration
李晓莹
广东省药品监督管理局审评认证中心
LI Xiao-ying
Evaluation and Certification Center, Guangdong Medical Products Administration
詹春燕
广东省药品监督管理局审评认证中心
ZHAN Chun-yan
Evaluation and Certification Center, Guangdong Medical Products Administration
叶舜旻
广东省药品监督管理局审评认证中心
YE Shun-min
Evaluation and Certification Center, Guangdong Medical Products Administration
摘 要Abstract
目的:分析广东省面膜类化妆品生产企业在生产质量管理规范(GMP)检查过程中发现的问题,并提出改进对策,为化妆品生产企业健全质量管理体系及药品监督管理部门制定更为有效的监管措施提供参考。方法:对2023 年1 月~2024 年6 月期间广东省面膜类化妆品生产企业GMP 检查过程中发现的缺陷进行统计,分析企业质量管理体系存在的不足,并提出针对性建议。结果:检查共发现不符合规定项目320 项次,其中关键项目不符合规定22 项次,其他重点项目不符合规定151 项次,一般项目不符合规定147 项次。企业生产质量管理体系被判定存在严重缺陷的占检查企业总数的26%。结论:面膜类化妆品生产企业在GMP 实施方面仍存在诸多问题,生产质量管理不规范,需进一步强化企业生产质量管理水平和能力提升,切实保障化妆品质量,确保公众用妆安全。
Objective:This study analyzes deficiencies identified during Good Manufacturing Practice GMP inspections of facial mask cosmetic manufacturers in Guangdong Province and proposes targeted improvement measures to support manufacturers in strengthening their quality management systems,while providing a scientific basis for regulatory authorities to optimize oversight strategies. Methods: A statistical analysis was conducted on deficiencies identified during GMP inspections of facial mask cosmetic manufacturers in Guangdong Province from January 2023 to June 2024. Weaknesses in quality management systems were examined,and recommendations for improvement were developed. Results:A total of 320 non-compliance items were recorded including 22 critical,151 major,and 147 general deficiencies. Among the inspected manufacturers 26% were found to have significant flaws in their quality management systems. Conclusion Facial mask cosmetic manufacturers continue to face considerable challenges in GMP compliance particularly in production quality management practices. Strengthening quality management standards and capabilities is essential to ensuring product quality and safeguarding consumer safety.
关键词Key words
面膜类化妆品;质量管理体系;化妆品GMP 检查;缺陷分析;监督检查
facial mask cosmetics;quality management system;cosmetic GMP inspection;deficiency analysis;regulatory inspection
基金项目



广东省药品监督管理局2023 年科技创新项目:广东省面膜类化妆品《化妆品生产质量管理规范》 现场检查指南(2023TDB51)

面膜类化妆品在我国逐渐成为日常护肤的常用产品,其使用人群持续扩大,使用频次不断增加。近年来,化妆品监管法规体系日益完善,特别是《化妆品生产质量管理规范》[1] ( 以下简称化妆品GMP) 于2022 年7 月1 日正式实施、《化妆品生产质量管理规范检查要点及判定原则》[2] ( 以下简称《检查要点》) 于2022 年10 月出台以来,化妆品监管能力和检查水平显著提升。同时,国家加大了对化妆品抽检的力度,面膜类化妆品相关的风险信息频频出现。
此前,山东省曾通过资料收集、问卷调查、现场调研和座谈交流等方式对省内面膜类化妆品生产企业的质量管理状况进行调查[3] 。广东省作为全国面膜类化妆品的生产大省, 相关企业数量多、产品覆盖广,具有更强的代表性和普遍性。基于此,对广东省面膜类化妆品生产企业的监督检查情况进行汇总和分析,有助于全面掌握当前行业存在的共性问题与薄弱环节。本文基于2023 年1 月 ~2024年6 月广东省药品监督管理局药品检查中心( 以下简称广东中心) 根据面膜类化妆品风险信息组织的化妆品GMP 检查数据,对发现的缺陷内容进行汇总分析,并提出改进措施,旨在为面膜类化妆品生产企业持续实施化妆品GMP 提供指导,同时为药品监督管理部门制定相关政策提供参考。
1 基本概况
2023 年1 月~2024 年6 月,广东中心依据《检查要点》对全省45 家( 次) 面膜类化妆品生产企业开展了监督检查。其中,11 家( 次) 质量管理体系存在严重缺陷,24 家( 次) 质量管理体系存在缺陷,7 家(次) 未发现质量管理体系存在缺陷,3 家(次) 因特殊原因未能开展现场检查。监督检查主要针对企业涉及的风险信息展开,风险信息类型包括不符合强制性国家标准和技术规范(如微生物限度超标和非法添加)、未按备案资料载明的技术要求进行生产、产品非法宣称,以及严重不良反应等。
2 结果统计
2.1 不符合规定项目汇总分类
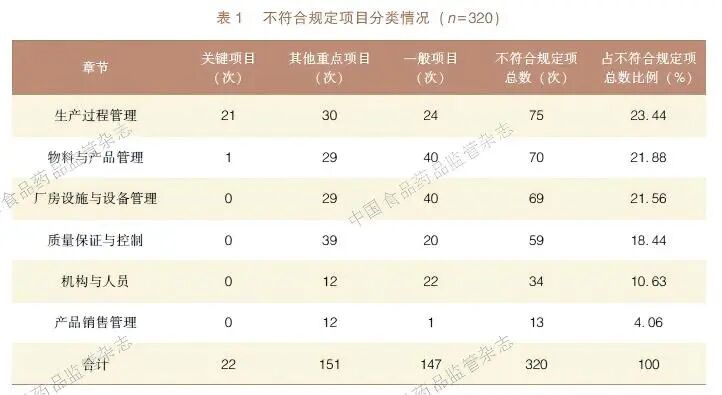
对45 家(次) 面膜类化妆品生产企业的监督检查结果进行汇总,共发现不符合规定项目320项次。其中,关键项目不符合规定22 项次,其他重点项目不符合规定151 项次,一般项目不符合规定147 项次。根据《检查要点》对不符合规定项进行分类,按涉及的章节统计,频次排名前四的章节分别为生产过程管理、物料与产品管理、厂房设施与设备管理、质量保证与控制。上述领域的不符合规定项相对集中,反映出企业在执行化妆品GMP 过程中普遍存在不足,具体见表1。
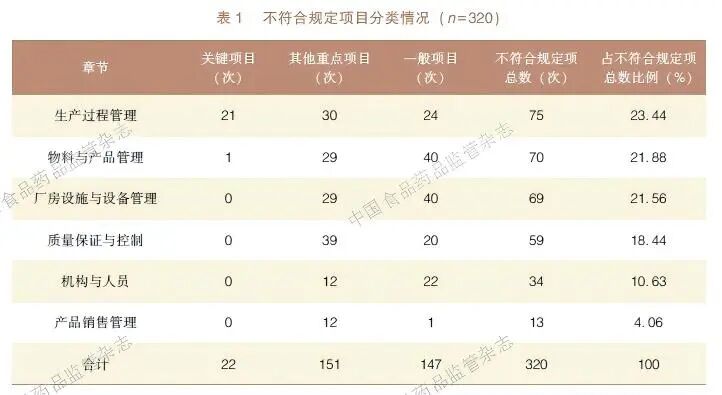
2.2 关键项目不符合规定情况
《检查要点》中关键项目共有3项,分别为49**、61**、74**。本研究共发现关键项目不符合规定22项次。其中,49**项不符合规定共计1次,占关键项目不符合规定项总数的4.55%;61**项不符合规定共计9次,占比40.91%;74**项不符合规定共计12次,占比54.55%。
2.3 其他重点项目不符合规定情况
监督检查中发现其他重点项目不符合规定项共计151项次。按照《检查要点》各章节进行分类,出现频次依次为质量保证与控制、生产过程管理、物料与产品管理、厂房设施与设备管理、机构与人员、产品销售管理,见表2。此外,按照涉及的具体检查条款出现频次排序,前十位依次为62*、68*、27*、47*、16*、30*、23*、50*、6*、76*,累计出现不符合规定项109次,详见表3。
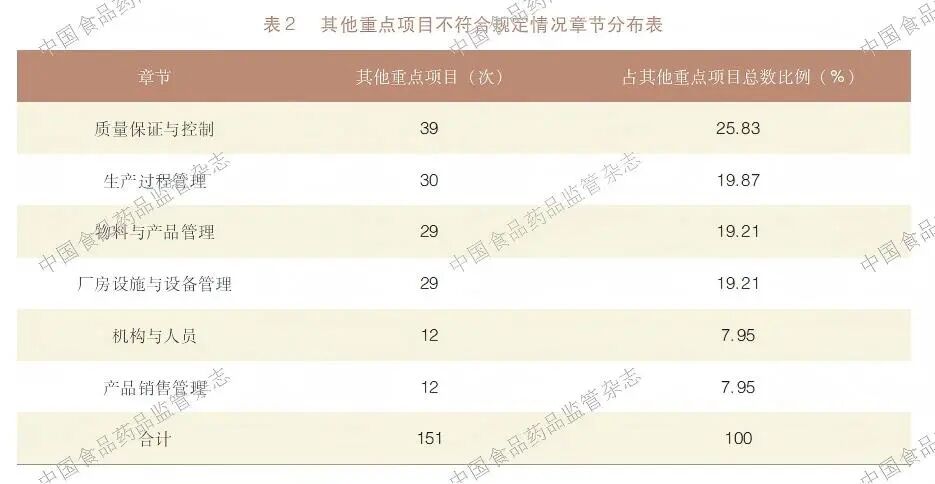
2.4 一般项目不符合规定情况
按照《检查要点》各章节进行分类,一般项目不符合规定项出现频次依次为厂房设施与设备管理、物料与产品管理、生产过程管理、机构与人员、质量保证与控制、产品销售管理,见表4。
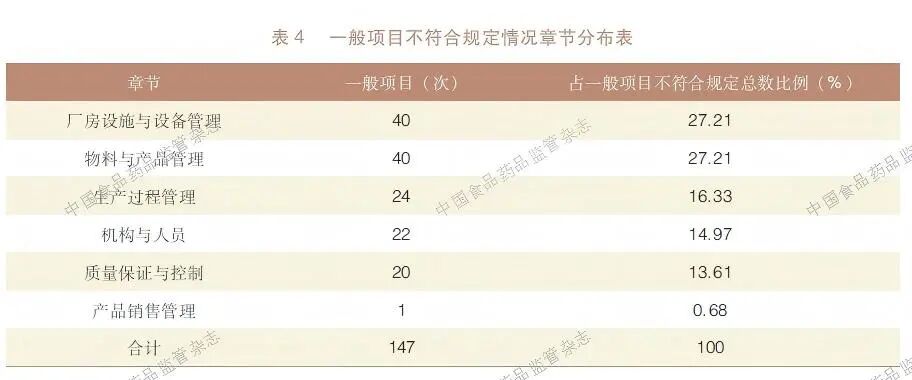
3 存在的主要问题
3.1 关键项目不符合规定问题
通过前文统计,关键项目74**项不符合规定的频次最高,主要有以下几类问题:产品批生产记录不完整,未经质量安全负责人审批即上市销售;未能提供产品的出厂检验报告,未经质量安全负责人审批即上市销售;企业未能提供已上市销售化妆品的产品放行文件。
关键项目中61**项不符合规定频次也较高,主要有以下几类问题:企业未建立生产工艺规程文件;企业未按照化妆品备案资料载明的生产工艺进行生产( 主要涉及配方、投料顺序和温度控制);企业未能在生产工艺规程中明确生产工艺参数及工艺过程的关键控制点。
关键项目49**项不符合规定数仅有1 次,现场检查发现企业使用外购的特殊化妆品半成品,但该企业未注册过任何特殊化妆品。
3.2 其他重点项目不符合规定问题
从表2 可以看出,各章节中其他重点项目不符合规定项的频次分布整体可为三个层次:第一层次为质量保证与控制,不符合规定项频次最高;第二层次包括生产过程管理、物料与产品管理以及厂房与设施设备管理,不符合规定项出现频次次之,三个章节之间不符合规定项频次无明显差异;第三层次为机构与人员及产品销售管理,不符合规定项频次相对较少。
3.2.1 生产过程管理
在生产过程管理相关条款中, 62**项和68**项不符合规定的频次均为15 次。
62*项不符合规定的情况包括:企业未能提供抽查产品的主要生产工艺验证方案、记录及报告;或者仅能提供部分验证文件,如只有验证方案,但缺少验证报告和记录等。
68*项不符合规定的情况包括:企业未能提供抽查产品的生产记录或提供的生产记录内容不完整;生产记录部分内容填写不完整,如生产指令未填写产品编号、客户名称、生产批号等内容;检验记录未填写检验日期;乳化记录未填写原料批号、投料时间、投料复核信息等。
3.2.2 质量保证与控制
在质量保证与控制相关条款中,27*项、16*项和23*项的不符合规定频次分别为12次、10次和9次。
27*项不符合规定有以下几类:企业留样数量不足,未达到出厂检验需求量的2倍;未按规定加贴留样标签,缺少留样信息;留样记录表上有记录,但是缺少实际留样产品。
16*项不符合规定常见问题包括:企业人员更改了记录,但更正人未签注日期及姓名;企业温湿度记录表填写与实际情况不一致,或部分生产期间温湿度记录缺失等。
23*项不符合规定有以下几类:企业未能提供产品需要检验的原料来料检验记录;未能提供已标示质量状态为合格的半成品的检验记录及报告;未能提供现场检查时正在灌装的半成品的检验记录及报告;未能提供仓库内存放产品或已销售产品的半成品检验记录及报告。
3.2.3 物料与产品管理
在物料与产品管理相关条款中,47*项不符合规定的频次为11次,50*项不符合规定的频次为9次。
47*项不符合规定常见问题包括:企业在库部分原料供应商不在合格物料供应商名录中;企业合格供应商名录中未记录物料名称、生产企业名称等内容;企业未能提供对供应商审核的资料,或对关键原料供应商进行重点审核的资料;企业未建立合格供应商目录等。
50*项不符合规定常见问题包括:企业未能提供原料到货后对其确认的相关记录;企业未建立物料验收相关制度规程,且未能提供生产用物料的验收记录;企业未建立部分物料的验收标准和验收方法;企业已标示合格的物料性状与验收标准不一致,且未能提供该物料的验收记录等。
3.2.4 其余章节
在厂房设施与设备管理章节中,30*项不符合规定的频次为10 次,常见问题包括:企业擅自改变功能间用途, 如更衣间、称量间和预进间堆放大量半成品;企业在原料仓( 一般区) 进行称料、配料, 未在符合要求的称料间( 准洁净区) 内进行;企业生产车间的安全门、拆包间与配料间之间的门可以随意开启, 存在物料、人员的交叉污染;企业称量间内存放大量原料等。
在机构与人员章节中,6*项不符合规定的频次为9 次,常见问题包括:质量安全负责人未负责产品质量安全问题的决策,质量安全相关文件未由质量安全负责人签发,而由他人代为签发;企业数批次产品上市销售,但无法提供质量安全负责人签发的放行审核文件;企业现场未能提供质量安全负责人定期向法定代表人报告质量管理体系运行情况的相关文件。
在产品销售管理章节中,76*项不符合规定的频次为9 次,常见问题包括:企业销售记录缺少备案编号、价格、购买者名称、使用期限、净含量等内容;企业未建立产品销售记录制度;企业未能提供已销售产品的销售记录。
3.3 一般项目不符合规定问题
从表4 可以看出,各章节中一般项目不符合规定项的频次分布情况整体可为三个层次:第一层次为厂房设施与设备管理、物料与产品管理,不符合规定频次最高;第二层次为生产过程管理、机构与人员、质量保证与控制,不符合规定频次次之,三个章节之间无明显差异;第三层次为产品销售管理,一般项目不符合规定项仅出现1 次。
3.3.1 厂房设施与设备管理
该章节存在的主要问题包括:生产设备缺少状态标识及清洁消毒标识,或标识不清晰、与设备实际状态不相符,如正在运行的设备状态标识为“检修” “待机” 等;关键衡器、量具、仪表和仪器未进行检定,如乳化车间真空乳化锅压力表、均质搅拌机压力表校准证书已过期,均质搅拌机、乳化间称量用的台称校准证书已过期等;未配备防虫防鼠设施或配备不足,如生产车间未配备防止昆虫、鼠和其他动物进入的设备设施,包材仓、成品仓库的可开启窗户未安装防虫防鼠设施,生产车间内直接连通外界的排气扇未安装防蚊虫设施;未能提供洁净区和准洁净区的环境监控计划,或未定期开展并留存监控记录;生产车间内温湿度记录表上记录的温度超过文件规定生产期间的温度标准。
3.3.2 物料与产品管理
该章节存在的主要问题包括:物料或产品未分类按批进行摆放,例如成品仓库产品未按照待检、合格、不合格等分批分类存放且未明确标示, 待发货产品放置在退货区,原料仓库与成品仓库共用一个区域且未分区存放,不合格品区域存放合格产品等;原料仓库部分物料未贴标识,或物料标识信息不完整,缺少生产企业名称、原料规格、使用期限等关键信息;企业未对关键原料进行留样。
3.3.3 生产过程管理
该章节存在的主要问题包括: 物料及半成品未全程清晰标示,如乳化车间内称量好的物料无任何标签标识,静置间、乳化间、管口间等区域发现多种物料没有任何标识,静置间、灌装间部分半成品未标明名称、生产日期及批号等,部分标签没有完整填写数量信息;清场操作执行不规范,如乳化车间乳化罐在清洁消毒后未标明有效期限,个别企业生产活动结束4 天后仍未对生产场地进行清场等。
3.3.4 机构与人员
该章节存在的主要问题包括:员工培训管理不规范,如未制定年度培训计划,或虽制定了培训计划但未严格执行,培训档案内容不完整,缺少对培训方式及考核情况的记录,未对新入职员工进行培训,培训计划设置不合理,缺少化妆品相关法律法规等关键内容;企业未按要求建立并执行进入生产车间卫生管理制度,如现场发现部分员工穿拖鞋进入膏霜、面膜灌装车间,未按要求穿戴专用工作鞋或一次性鞋套,灌装间存放创可贴、手机充电线等员工私人物品等。
3.3.5 质量保证与控制
该章节存在的主要问题为:企业未按要求建立并执行实验室管理制度,如现场发现电子天平(型号:AX-2000) 称盘表面残留大量油污,部分实验室仪器设备无状态标识且校准已过期等;企业未按要求进行留样,如现场检查时企业未能提供成品留样台账,或虽留样但未能提供按要求进行观察的记录等。
3.3.6 产品销售管理
该章节存在的问题是企业未按规定对不合格产品进行明确标识和隔离,未能提供相关处理记录。
4 分析与建议
通过检查结果和不符合规定项目可以看出,相关化妆品企业的生产质量管理体系建设和运行与化妆品GMP 要求存在一定差距,给化妆品生产质量安全带来了风险隐患。因此,亟需药品监督管理部门进一步加强监管,同时推动企业持续改进质量管理体系,确保化妆品生产的规范性和安全性。
4.1 强化监督检查,督促企业提升质量管理意识
近年来,化妆品监管法律体系不断完善,《检查要点》作为监督检查的重要依据, 对化妆品注册人、备案人及受托生产企业贯彻执行化妆品GMP 提供了具体指导[4] 。然而,检查结果显示,部分化妆品生产企业对此重视不足,未能及时根据《检查要点》完善自身质量管理体系。建议监管部门进一步加强监督检查,尤其应针对风险信息频发的面膜化妆品企业组织开展飞行检查和专项检查[5] , 对质量管理意识薄弱的企业,以及在检查过程中发现的违法违规线索依法严肃处理,在行业内形成具有震慑力的典型案例,从而强化企业的主体责任意识和质量管理意识,推动企业积极完善质量管理体系[6] 。
4.2 强化企业培训,提升企业员工质量管理素质
检查发现,企业普遍对员工培训重视不足,表现为缺少系统的年度培训计划、培训内容不全面、培训过程缺乏考核等,导致员工整体对化妆品GMP 和《检查要点》的要求不熟悉、对岗位职责和要求不了解、日常操作不熟练,甚至出现违规操作的情况,从而给化妆品生产带来风险隐患。建议企业应高度重视培训工作,认真组织全体员工学习直接关系企业质量管理体系构建的政策法规、岗位职责、产品专业知识及操作规范[7] 。尤其应加强对《检查要点》中关键项目和其他重点项目不符合规定情况相对集中的生产过程管理、质量保证与控制、物料与产品管理、厂房设施与设备管理等章节内容的培训,并通过培训效果评估和实操考核, 切实提升员工的实际操作能力,确保员工真正掌握质量管理要求[3] 。
4.3 强化贯彻落实, 提升企业质量管理水平
从不符合规定项目的具体内容来看,企业在落实化妆品GMP 和《检查要点》要求方面仍存在较大差距,尤其是在产品放行管理、按照注册或备案要求制定并执行生产工艺规程、生产记录的完善、验证管理以及物料管理[8,9]等方面问题较为突出。建议企业在加强培训的基础上,强化质量管理体系的贯彻落实,充分利用体系自查,重视监管部门日常检查和监督检查中发现的问题,不断健全质量管理体系,实现企业质量管理的正向循环与持续提升。
第一作者简介
王焕,广东省药品监督管理局审评认证中心,副主任药师。专业方向:化妆品GMP 检查研究
通讯作者简介
吴生齐,广东省药品监督管理局审评认证中心,主任药师。专业方向:化妆品GMP 检查、药品GMP 检查、药品注册研究
参考文献:略




编辑:李丹
审核:赵燕宜

