一针编程抗癌 T 细胞!Nature 重磅突破:体内精准编辑颠覆 CAR-T,血液瘤、实体瘤全拿下
CAR-T 细胞疗法被誉为癌症治疗领域的革命性突破,但这种个性化治疗的过程堪称一场 “细胞长征”:医生从患者体内提取免疫细胞,运送到专业实验室进行基因改造,再运回医院输回患者体内。整个过程耗时数周,花费高达数十万美元,让无数亟需治疗的患者望而却步。
如今,发表在
《Nature》
上的一项重磅研究彻底改变了这一现状,来自加州大学旧金山分校、伯克利分校、杜克大学等机构的科学家们,开发出一种能直接在患者体内 “编程” 抗癌 T 细胞的新方法,无需体外培养,仅需单次注射即可激活体内免疫战士,不仅解决了传统 CAR-T 的诸多痛点,更在血液瘤和实体瘤模型中均展现出强效疗效,有望彻底颠覆现有的治疗模式。

全球癌症统计数据显示,2020 年新增癌症病例约 1930 万,死亡病例近 1000 万。CAR-T 疗法在血液肿瘤领域展现出惊人疗效,某些难治性白血病的完全缓解率可达 80% 以上,但美国食品药品监督管理局目前已批准的七种 CAR-T 疗法,每剂价格在 40 万至 50 万美元之间,加上前期化疗和住院费用,总治疗成本往往突破百万美元。
更令人揪心的是,在长达数周的等待期间,部分患者的病情持续恶化,失去了治疗机会。同时,传统 CAR-T 多依赖慢病毒载体随机整合 DNA,可能导致基因插入错误位点,带来潜在癌变风险,且 CAR 在非 T 细胞中表达可能引发抗原阴性复发。这些现实困境,使得 CAR-T 疗法成为全球性的医疗资源可及性难题,而这项新研究的核心突破,正是通过精巧设计的双载体系统,一举解决了体内基因改造的三大核心痛点:靶向特异性、整合精准性和递送有效性。
研究团队设计的双载体系统,堪称 “精准编辑 + 安全整合” 的典范。第一个载体是包膜递送载体(EDV),核心任务是携带 CRISPR-Cas9 基因编辑工具(Cas9 核糖核蛋白复合物)精准抵达 T 细胞。为实现特异性靶向,团队对 EDV 进行了双重改造:表面融合抗 CD3 单链可变片段(scFv),使其仅能识别并结合 T 细胞表面的 CD3 分子;同时突变了囊膜蛋白 VSVG 的关键位点, 消融了对低密度脂蛋白受体(LDLR)的亲和力,彻底避免对造血干细胞、巨噬细胞、肿瘤细胞等其他细胞造成误编辑。更巧妙的是,CD3 靶向设计不仅能精准递送 Cas9 工具,还能激活 T 细胞,增加细胞周期进程——因为同源定向修复(HDR)依赖细胞分裂,这一设计为基因整合创造了有利条件,大幅提升了编辑效率。
第二个载体是经定向进化改造的腺相关病毒(AAV-hT7),负责携带编码 CAR 的 DNA 供体模板(HDRT)。传统 AAV6 在体内易被血清预存中和抗体清除,且对 T 细胞靶向性不足,研究团队通过三轮血清环境下的定向进化筛选,获得了 AAV-hT7 变体:它能抵抗人体预存中和抗体,在含血清条件下的 T 细胞转导效率较 AAV6 显著提升。基因组-wide CRISPR 筛选证实,其主要通过结合 T 细胞表面的 CD7 受体实现高效摄取,进一步强化了 T 细胞特异性。
值得注意的是,CAR 供体模板不含启动子,需通过 HDR 精准整合到 T 细胞特异性的 T 细胞受体 α 恒定链(TRAC)基因位点,才能借助内源性 TRAC 启动子实现 CAR 的稳定、生理性表达——这一设计既保证了 CAR 仅在 T 细胞中表达,避免了非靶向细胞编辑的风险,又能同时敲除内源性 TCR,为后续开发通用型 CAR-T 奠定基础,减少移植物抗宿主病(GvHD)风险。
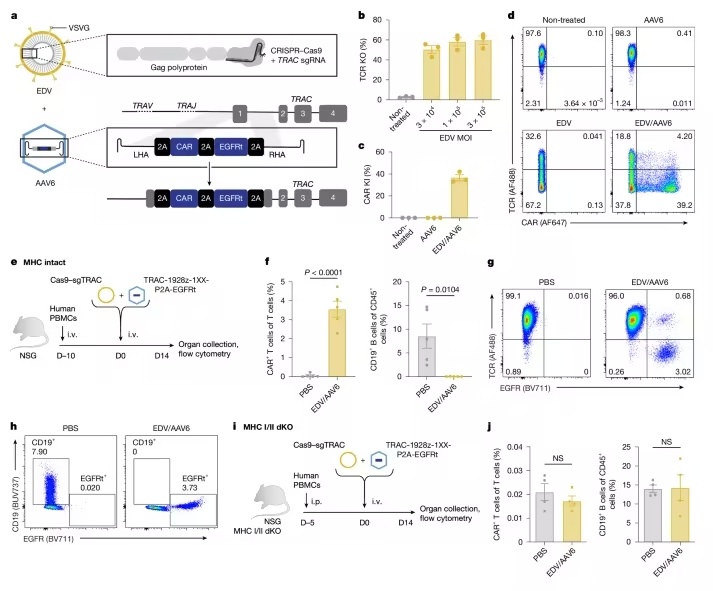
Cas9-EDV与HDRT-AAV的共递送在体外和体内生成TRAC-CAR T细胞
在人源化免疫系统的小鼠实验中,这套双载体系统展现出惊人效果。针对侵袭性 B 细胞急性淋巴细胞白血病(B-ALL)的实验显示,单次注射后,18/20 只小鼠实现完全缓解,骨髓和脾脏中的 NALM6 白血病细胞被彻底清除,改造后的 CAR-T 细胞占人源 CD45⁺细胞比例最高可达 40%。
更令人振奋的是,该方法对多发性骨髓瘤也表现出强效疗效——8/8 只模型小鼠均实现肿瘤完全控制,35 天后再次接种 OPM2 骨髓瘤细胞,3/4 的小鼠仍能有效抵御肿瘤复发,证实体内生成的 CAR-T 细胞具备长期持久性。针对实体瘤的挑战同样取得突破,在 MES-SA 肉瘤模型中,团队设计了靶向 B7H3 抗原的 CAR,结果 5/6 只小鼠达到完全缓解,打破了 CAR-T 疗法在实体瘤领域疗效不佳的 “魔咒”。
更重要的是,体内生成的 TRAC-CAR T 细胞展现出超越体外制造细胞的独特优势:流式分析显示,其 CD4⁺/CD8⁺亚群比例均衡,Ki-67⁺增殖细胞比例显著高于体外培养细胞,同时保留了 27.4% 的 TCF1⁺祖细胞样亚群——这种表型与更强的抗肿瘤持久性和复发抵抗能力密切相关。对比实验进一步证实,与慢病毒介导的体内 CAR-T 生成相比,TRAC 位点整合的 CAR-T 细胞扩张速度更快(第 2 周扩张倍数是慢病毒组的 21-50 倍),CAR 表达更均一(无高低表达差异),肿瘤控制效果更优,完全缓解率达到 100%,而慢病毒组最高仅为 17%。此外,血清细胞因子检测显示,小鼠体内未出现明显细胞因子风暴,安全性表现良好。
为验证系统的通用性,团队还测试了不同靶点的 CAR 构建:针对 CD19 的 CAR 用于 B 细胞恶性肿瘤,针对 BCMA 的 CAR 用于多发性骨髓瘤,针对 B7H3 的 CAR 用于实体肉瘤,均取得了显著疗效,证实该平台可灵活适配不同癌症类型。同时,TCR 克隆性分析显示,体内生成的 CAR-T 细胞克隆多样性虽低于体外制造产品,但符合体内工程化的特征,且未出现单一克隆过度扩张的情况,降低了潜在的恶性转化风险。
这项研究的突破性意义,不仅在于 CAR-T 疗法的革新,更在于为整个细胞与基因治疗领域开辟了全新路径。传统方法依赖病毒随机整合 DNA,存在插入突变风险,而新方法通过双载体系统和 TRAC 位点精准设计,确保改造仅发生在 T 细胞,且基因准确插入预定位置,大幅提升了安全性。体内原位编辑避免了体外培养导致的细胞干性丧失,保留了 T 细胞的天然增殖和归巢能力,疗效更优。同时,该系统无需复杂的体外培养设备,有望大幅降低治疗成本,解决 “细胞长征” 带来的时间和经济负担。
对于全球无数等待 CAR-T 疗法的患者而言,这项技术的潜在意义不言而喻。如果成功转化到临床应用,患者可能只需一针注射,即可在体内完成免疫细胞的改造,省去数周等待时间和数十万费用,彻底打破 CAR-T 疗法的价格壁垒和可及性限制。更重要的是,该技术有望让 CAR-T 疗法走出顶级癌症中心,进入社区医院,真正实现医疗资源的普惠化。
当然,这项技术距离临床应用仍有需要攻克的难关:需扩大样本规模开展人体临床试验,评估长期安全性和有效性;需进一步优化载体递送效率,确保在人体中达到治疗所需的 CAR-T 细胞比例;同时,需解决抗 AAV 抗体产生可能影响重复给药的问题。但研究者表示,该系统在小鼠体内的安全性和疗效已得到充分验证,随着技术的不断完善,未来有望实现 “一针抗癌” 的终极目标,让 CAR-T 疗法真正走向民主化,为全球癌症患者带来更可及、更高效、更安全的治疗新选择。(
生物谷)
参考文献:
Nyberg, W.A., Bernard, PL., Ngo, W. et al.
In vivo site-specific engineering to reprogram T cells
. Nature (2026). doi:10.1038/s41586-026-10235-x
