Science:王育才/朱书/蒋为团队揭示肠道细菌影响载体体内递送效率,为提高药物递送效率带来全新思路


撰文丨王聪
编辑丨王多鱼
排版丨水成文
为了发挥药效,药物和疫苗需要避免降解以抵达体内预定靶点,并将脱靶毒性降至最低。近年来,研究人员开发了多种体内递送系统(In vivo delivery system,IDS),包括合成 IDS(例如聚合物纳米颗粒、脂质体、LNP 等)和病毒 IDS(包括慢病毒、腺病毒、AAV 以及溶瘤病毒等),这些递送系统旨在保护和运输治疗药物,然而,它们临床应用因递送效率低而受阻,尤其容易被免疫系统迅速清除,而对递送系统本身进行的改进,不足以解决这一问题。

体内递送系统(In vivo delivery system,IDS)对于临床应用生物利用度低或存在剂量限制性全身毒性的治疗剂至关重要。以聚合物纳米颗粒和病毒载体为代表的体内递送系统的发展,推动了包括体细胞基因组编辑、mRNA 疗法和靶向癌症疗法在内的多种治疗范式的快速发展。然而,一个主要且持续存在的局限性仍然存在:它们会被机体的清除系统非选择性清除,这极大地降低了向靶器官/组织的递送效率。
在所有器官中,肝脏是 IDS 清除的主要场所,其中肝脏驻留的库普弗细胞(KC)是主要的清除细胞,能够捕获大部分给药剂量。目前,减少肝脏 IDS 清除的策略主要依赖于抗污表面修饰、材料重新设计、KC 饱和以及清除受体阻断。尽管这些方法已取得部分成功,但在通用性、安全性、肝脏选择性和临床转化性方面,仍有很大的改进空间。
一直以来,研究人员在材料和工程优化方面付出了大量努力,但对于肝脏如何维持其高水平的清除体内递送系统(In vivo delivery system,IDS)的能力,却关注甚少。因此,确定调控库普弗细胞(KC)与 IDS 相互作用的核心信号通路,将有助于开发适用于多种 IDS 的全新递送增强策略。
鉴于肠道微生物群与肝脏之间存在密切的相互作用,研究团队推测,可能存在一条肠-肝信号轴,以增强库普弗细胞在稳态下对包括 IDS 在内的外来物质的吞噬作用。
研究团队证实,清除肠道微生物群或阻断细菌感应受体,可显著降低肝脏清除率,并提高多种体内递送系统(IDS)的递送效率(无论递送系统的自身化学成分或其递送何种物质)。这一效果转化为基于 IDS 的疗法(包括体细胞基因组编辑、精准癌症治疗)的显著疗效提升。
递送效率的增强,归因于库普弗细胞(KC)的功能失活,并伴有其形态、分子表型和吞噬活性的明显改变。研究团队进一步确定了革兰氏阴性菌是该信号轴的主要驱动因素,但它们并非通过细菌来源产物直接作用于库普弗细胞。相反,肠道细菌调控肠上皮细胞的色氨酸代谢,而上皮细胞来源的血清素成为连接肠道与库普弗细胞介导的 IDS 清除的关键信使。血清素通过库普弗细胞上的特定受体进行信号转导,触发细胞骨架重塑,并上调吞噬相关基因的表达,从而广泛增强库普弗细胞对多种 IDS 的摄取。
在治疗方面,通过限制饮食中血清素生成来源或阻断相关血清素受体实现的短暂血清素信号中断,即可广泛提高体内递送系统(IDS)的递送效率,且这一短暂的干预窗口足以在多种临床相关的基于 IDS 的疗法中实现显著的治疗效益——使化疗和溶瘤病毒疗法的效果提高了 3 倍多,使体细胞基因编辑和 mRNA 疗法的效果提高了 5-15 倍。
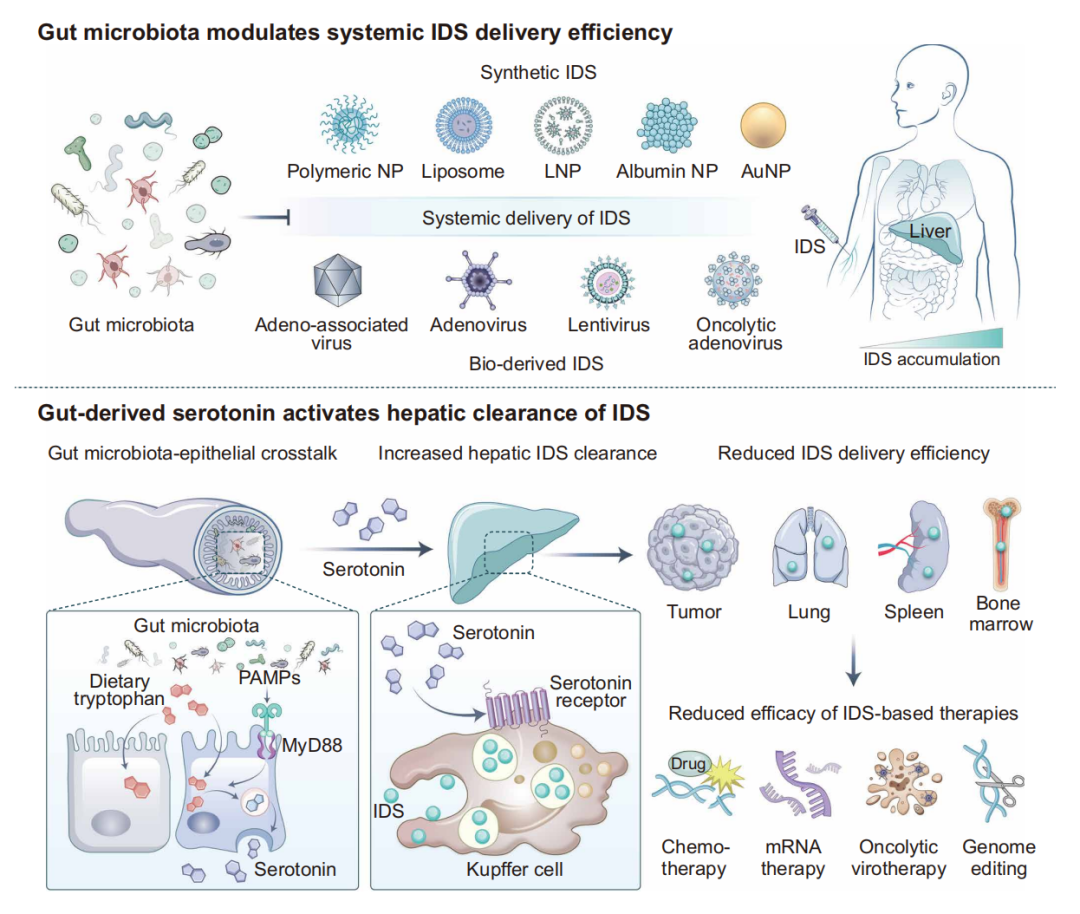 肠-肝免疫轴限制了基于 IDS 的疗法
肠-肝免疫轴限制了基于 IDS 的疗法
总的来说,这项研究确定了肠道共生菌驱动的肠-肝免疫轴是调控体内递送系统(IDS)清除和全身递送效率的主要因素,表明了长期存在的药物递送障碍可以通过调控内源性生物途径来解决。从转化医学角度来看,靶向色氨酸代谢或血清素信号转导的策略为提高 IDS 效率提供了一种广泛适用的方法,通过减少肝脏的快速清除或肝毒性,对基因治疗、mRNA 疗法以及精准癌症治疗具有良好的应用前景。
论文链接:
https://www.science.org/doi/10.1126/science.adu7686




点在看,传递你的品味




