急性髓系白血病(AML)的治疗格局正在经历一场深刻的范式转变。过去几十年间,以“7+3”方案(阿糖胞苷联合蒽环类药物)为基础的强化疗 followed by 异基因造血干细胞移植(allo-HSCT)一直是治疗的金标准。然而,对于携带特定高危分子特征的患者群体,尤其是赖氨酸甲基转移酶2A重排(KMT2Ar)和核磷蛋白1突变(NPM1m)的AML患者,传统疗法往往难以实现持久的疾病控制,复发率高且预后不佳。随着对白血病发生机制理解的深入,靶向治疗时代应运而生。继FLT3抑制剂和IDH1/2抑制剂之后,阻断Menin-KMT2A蛋白相互作用成为了近年来最具突破性的治疗策略。2024年11月,首款Menin抑制剂Revumenib获得加速批准,标志着这一类药物的正式登场。然而,单药治疗虽能诱导缓解,却面临分化综合征(DS)、心脏毒性(QTc延长)以及获得性耐药等挑战。当前,临床研究的焦点已迅速从单药转向联合治疗。多项早期临床试验数据显示,Menin抑制剂与强化疗或去甲基化药物(HMA)及维奈克拉(Venetoclax)组成的“三联疗法”,在初治和复发/难治(R/R)患者中均展现出令人瞩目的疗效,总缓解率(ORR)显著提升,微小残留病灶(MRD)阴性率大幅提高。本文基于最新权威综述,深入探讨Menin抑制剂三联疗法的疗效突破、安全性管理策略以及针对耐药机制的应对之道,旨在为临床医生提供科学、客观的决策参考。一、机制溯源:为何Menin成为关键靶点?
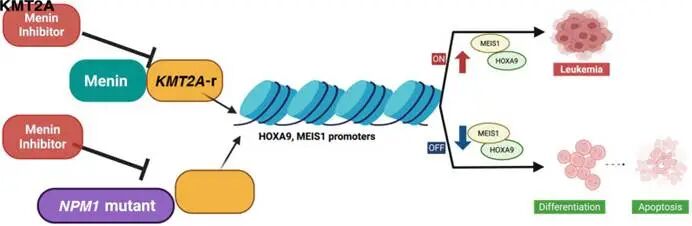
要理解Menin抑制剂的疗效,首先需明确其作用机制。尽管KMT2Ar和NPM1m AML的遗传起源不同,但两者在致病机制上存在惊人的共性:它们都高度依赖Menin蛋白来维持异常的HOX-MEIS转录程序。Menin是由MEN1基因编码的染色质支架蛋白。在KMT2Ar白血病中,Menin直接结合所有KMT2A融合蛋白N端的保守基序,将复合物锚定在HOX基因位点,并招募DOT1L等组蛋白甲基转移酶,从而维持HOXA9、HOXA10和MEIS1等高表达。这些转录因子是维持白血病干细胞自我更新和阻断分化的关键。而在NPM1m AML中,突变的NPM1蛋白易位至细胞核,与野生型KMT2A复合物及Menin相互作用,同样驱动这一致癌轴。Menin抑制剂通过强效破坏Menin与KMT2A复合物之间的蛋白 - 蛋白相互作用,迫使复合物从染色质上解离,沉默HOX-MEIS转录程序。这一过程导致H3K79甲基化水平下降,增强子重编程,最终恢复髓系细胞的分化能力,诱导细胞周期停滞和凋亡。由于该结合口袋在所有KMT2A融合变体中高度保守,且在正常造血祖细胞中非必需,因此这类药物具有广泛的基因型覆盖率和良好的治疗指数。图1.Menin抑制剂在伴NPM1突变及KMT2A重排AML中的作用机制示意图
二、单药治疗的奠基与局限:从Revumenib到新一代药物
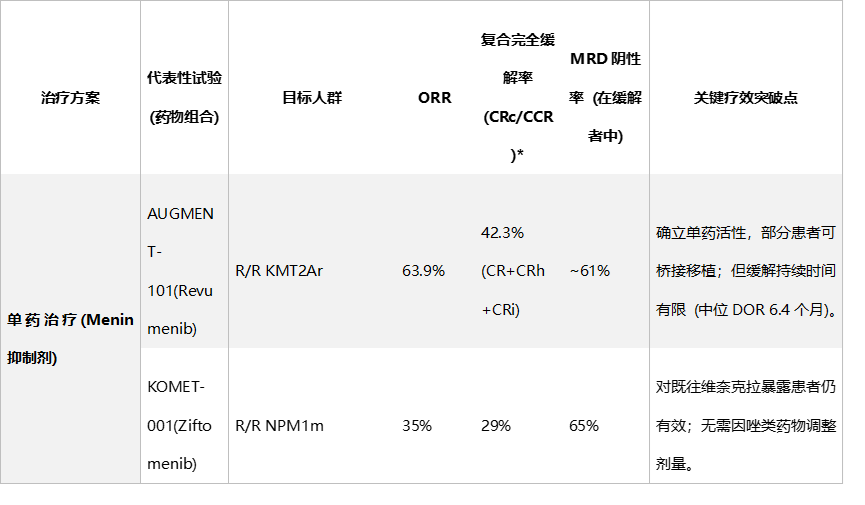
作为先行者,Revumenib在AUGMENT-101研究中确立了其地位。在重度预治的R/R KMT2Ar患者中,其复合完全缓解率(CCR)达到22%,总缓解率(ORR)高达63%,且61%的缓解者实现了MRD阴性。更重要的是,约40%的缓解者成功桥接了allo-HSCT,为治愈带来了希望。在NPM1m患者中,Revumenib也展现了类似的活性(ORR 47%)。随后,Ziftomenib、Enzomenib、Bleximenib等新一代药物相继问世。Ziftomenib在NPM1m患者中显示出33%的ORR,且无需因联用唑类抗真菌药而调整剂量,亦无显著的QTc延长风险。Enzomenib则凭借优异的药代动力学特征,在KMT2Ar和NPM1m患者中分别取得了65.2%和59%的ORR,且分化综合征发生率较低。Bleximenib和共价结合抑制剂BMF-219更是被设计用于克服潜在的耐药突变。然而,单药治疗的局限性也日益显现。首先,缓解深度和持续时间仍有限,中位缓解持续时间(DOR)多在4-7个月之间,难以长期控制疾病。其次,特异性毒性不容忽视。分化综合征(DS)作为“脱靶”效应,发生率在10%-20%之间,严重时可危及生命。此外,Revumenib特有的QTc间期延长问题限制了其在部分心脏病患者中的应用。最为严峻的是,约39%的Revumenib复发患者出现了MEN1基因的获得性突变,导致靶点结合能力下降,引发耐药。表1. Menin抑制剂三联疗法 vs. 单药治疗对比
三、三联疗法的崛起:疗效的深度突破
鉴于单药治疗的瓶颈,研究者迅速启动了Menin抑制剂与现有标准疗法联合的探索。目前的“三联疗法”主要指Menin抑制剂联合“维奈克拉+去甲基化药物(Ven/HMA)”或联合“强化疗(7+3)”。3.1在新诊断(ND)患者中的惊艳表现
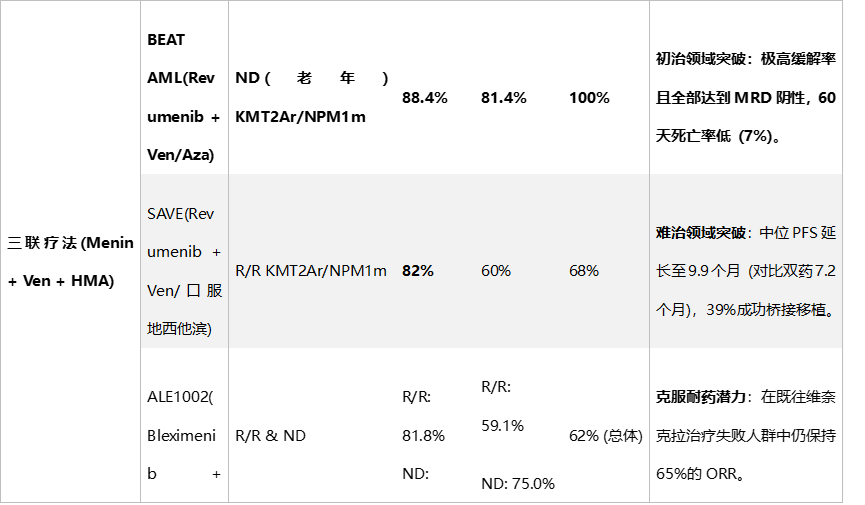
对于初治患者,三联疗法似乎正在重新定义缓解标准。在BEAT AML联盟的研究中,Revumenib联合Ven/Aza治疗老年ND患者,CR率高达67%,CCR达69.3%,且所有缓解者均实现MRD阴性。更为震撼的是KOMET-007试验的数据:Ziftomenib联合“7+3”方案治疗ND KMT2Ar或NPM1m患者,CR率达到了惊人的100%,MRD阴性率高达86%。Bleximenib联合“7+3”在ND患者中也取得了86%的CCR。这些数据强烈提示,Menin抑制剂有望成为此类患者的一线标准治疗。3.2在复发/难治(R/R)患者中的挽救价值
对于既往治疗失败的患者,三联疗法同样展现了强大的挽救能力。SAVE试验评估了全口服方案(Revumenib+口服地西他滨/Cedazuridine+维奈克拉),在R/R患者中ORR高达82%,中位无进展生存期(PFS)延长至9.9个月,显著优于历史对照。值得注意的是,即便是在既往接受过维奈克拉治疗的患者中,Ziftomenib和Bleximenib的三联方案仍保持了50%-65%的ORR,证明了其克服BCL-2耐药潜力的可能性。3.3 MRD阴性与移植桥接
三联疗法最核心的优势在于深度的MRD清除。多项研究显示,三联方案下MRD阴性率普遍超过60%-80%,远高于单药治疗。深度的分子学缓解不仅延长了生存期,更为更多患者创造了接受allo-HSCT的机会,这是目前唯一可能治愈AML的手段。四、安全性管理:差异化特征与应对策略
随着给药强度的增加,三联疗法的安全性管理变得尤为关键。总体而言,毒性可控,但需精细化管理。4.1分化综合征(DS)的预防与处理
DS是Menin抑制剂类的标志性毒性,源于白血病细胞的快速分化。在三联疗法中,DS发生率略有上升(约15%-25%),但严重(≥3级)事件比例并未显著增加。关键在于早期识别(如不明原因发热、体重增加、呼吸困难)和及时干预。目前的标准策略包括预防性使用地塞米松、出现症状时立即暂停给药并加大激素剂量。Enzomenib等新一代药物显示出更低的DS发生率,可能与其药代动力学特性有关。4.2心脏毒性的分子特异性
QTc间期延长是Revumenib的主要限制因素,在任何级别的发生率可达25%-64%。这要求临床必须常规进行心电图监测和电解质管理,并避免联用其他延长QTc的药物。相比之下,Ziftomenib、Bleximenib和Enzomenib在临床试验中未显示出显著的QTc延长风险,这为有心脏基础疾病的患者提供了更安全的选择。这表明心脏毒性是分子特异性的,而非类效应。4.3血液学毒性的叠加效应
当Menin抑制剂与Ven/HMA或强化疗联用时,骨髓抑制不可避免。在三联方案中,3-4级中性粒细胞减少和血小板减少的发生率可高达70%-80%。管理策略包括预防性使用抗生素、生长因子支持,以及灵活调整维奈克拉的给药天数(如从28天减至21天或14天)。值得庆幸的是,多数患者的血象可在疗程间歇期恢复,且未观察到长期的骨髓衰竭风险。五、耐药机制解析与未来应对
尽管三联疗法疗效显著,但耐药仍是悬在头顶的达摩克利斯之剑。目前的耐药机制主要分为两类:5.1靶点内耐药(On-target)
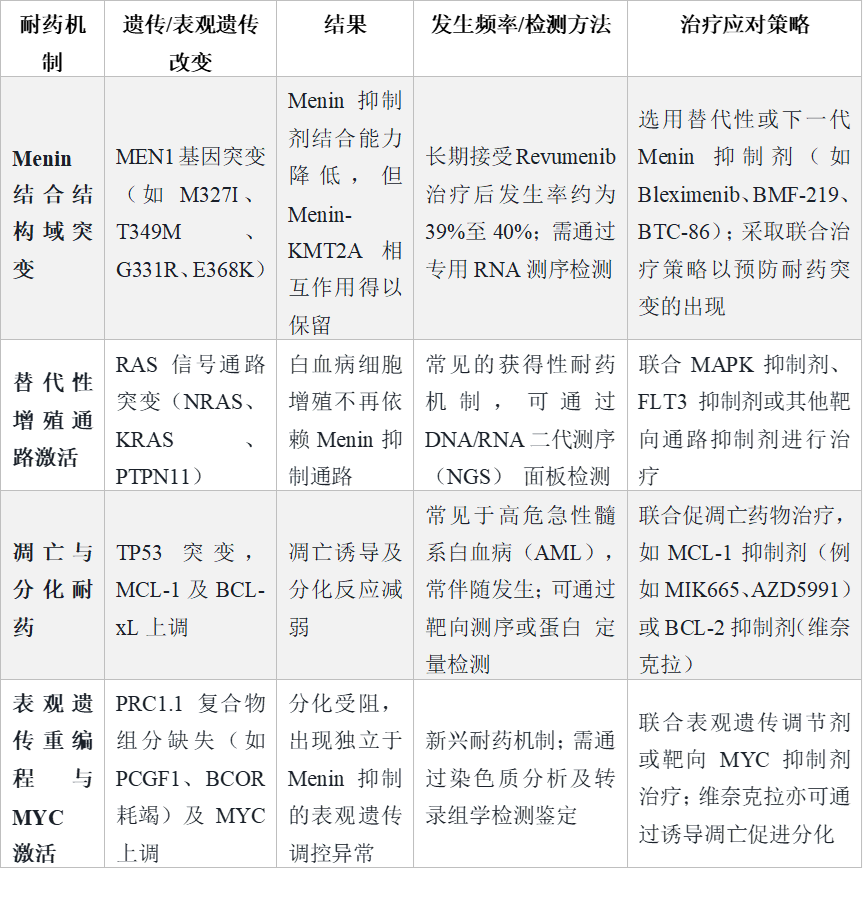
最主要的是MEN1基因的点突变(如M327I, G331R, T349M),这些突变改变了Menin蛋白的结合口袋,降低了药物亲和力,但保留了其与KMT2A的结合功能。这在Revumenib治疗后尤为常见(约39%)。应对策略: 开发下一代抑制剂。例如,Bleximenib和共价结合抑制剂BMF-219被设计为能结合突变后的Menin蛋白或结合不同的口袋,临床前数据已显示其对突变株有效。此外,轮换使用不同结构的Menin抑制剂也可能是一种策略。表2. Menin抑制剂耐药机制及治疗应对策略
5.2靶点外耐药(Off-target)
包括RAS通路突变(NRAS, KRAS, PTPN11)激活替代增殖信号,TP53突变导致凋亡受阻,以及PRC1.1复合物缺失引起的表观遗传重编程。应对策略: 联合靶向治疗。针对RAS突变,可联合MAPK抑制剂或FLT3抑制剂;针对凋亡受阻,可联合MCL-1抑制剂;针对表观遗传逃逸,可联合DOT1L抑制剂或BRD4抑制剂。这种“双靶向”甚至“多靶向”策略可能是未来的主流方向。此外,动态监测至关重要。在治疗过程中及复发时,利用高灵敏度的NGS技术检测MEN1突变及其他克隆演变,将为后续治疗方案的选择提供关键依据。六、结语
总的来说,Menin抑制剂三联疗法标志着KMT2Ar/NPM1m突变AML治疗迈入精准联合新纪元。相较于单药,该策略在初治及复发难治人群中显著提升了缓解深度与MRD阴性率,并有效桥接造血干细胞移植。尽管面临分化综合征、QTc延长及MEN1突变耐药等挑战,但通过新一代药物优化、毒性精细化管理及基于分子机制的联合阻断策略,临床获益有望进一步扩大。随着多项III期试验推进,三联方案有望确立为一线标准,最终改善高危AML患者的长期生存预后。[1] Perner F, Gadrey JY, Armstrong SA, Kühn MWM. Targeting the Menin-KMT2A interaction in leukemia: Lessons learned and future directions. Int J Cancer. 2026 Jan 15;158(2):342-356. doi: 10.1002/ijc.35332.[2] Chen T, Kim G, Rahimi Y, Kamdar M, Fernandez-Hernandez E, Woan K, Tam EL, Yaghmour G. Clinical Integration of Menin Inhibitors in AML: Evolving Data and Therapeutic Perspectives. Oncol Res. 2026 Feb 24;34(3):4. doi: 10.32604/or.2025.072443.[3] Thakur RK, Wang ES. The promise of menin inhibitors: from approval to triplet regimens. Hematology Am Soc Hematol Educ Program. 2025 Dec 5;2025(1):599-606. doi: 10.1182/hematology.2025000755.