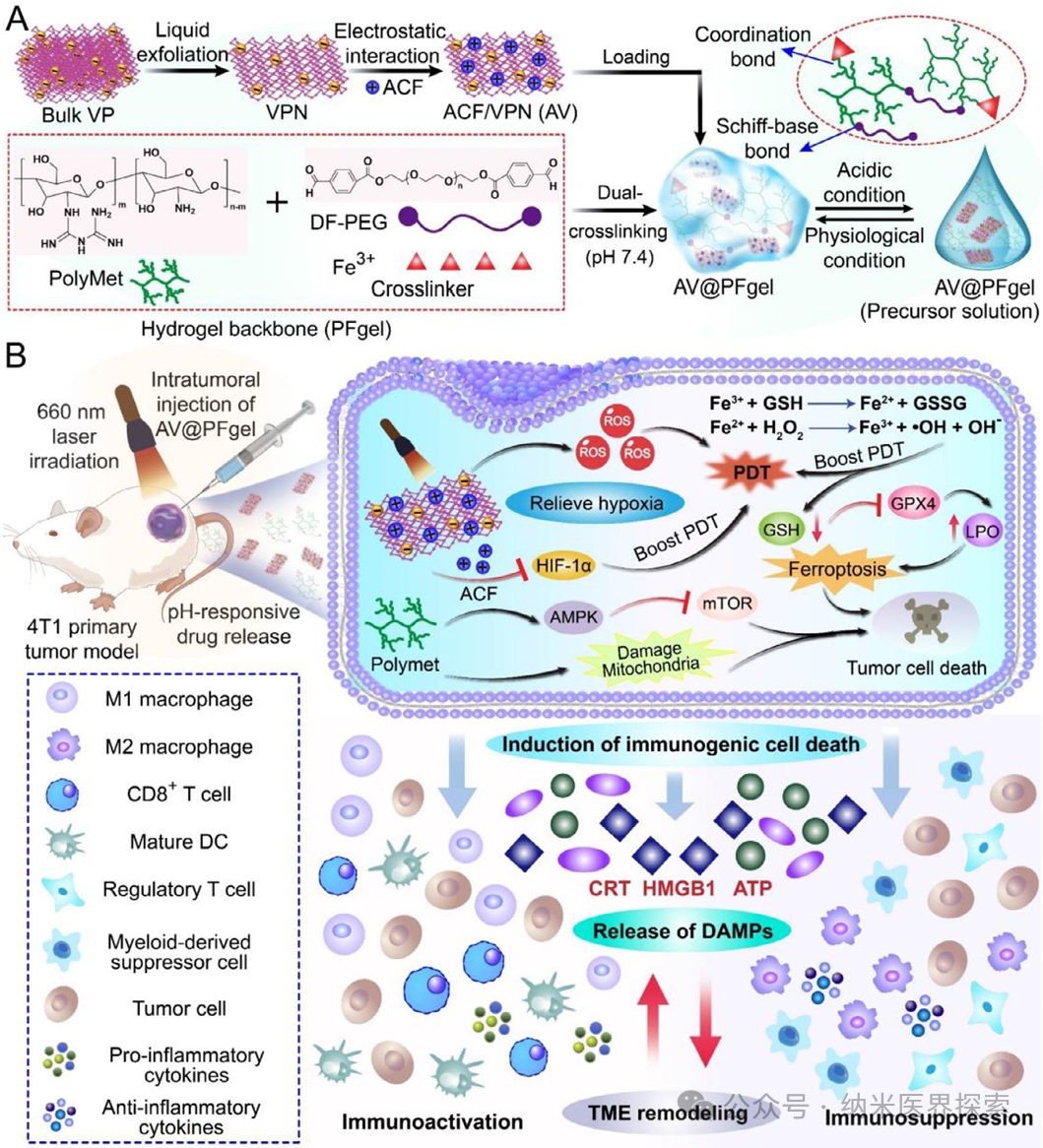
实体瘤缺氧一直是光动力治疗的老大难问题,还会引发免疫抑制、促进转移。这篇文章设计开发了一款可注射免疫水凝胶 AV@PFgel,把紫磷光动力、铁死亡、缺氧缓解和 HIF‑1α 抑制整合在一起。凝胶在肿瘤酸性环境下响应释药,激光照射后协同杀伤肿瘤、激活免疫,对原位和转移性三阴性乳腺癌都有很好的抑制效果,还能建立长期免疫记忆。
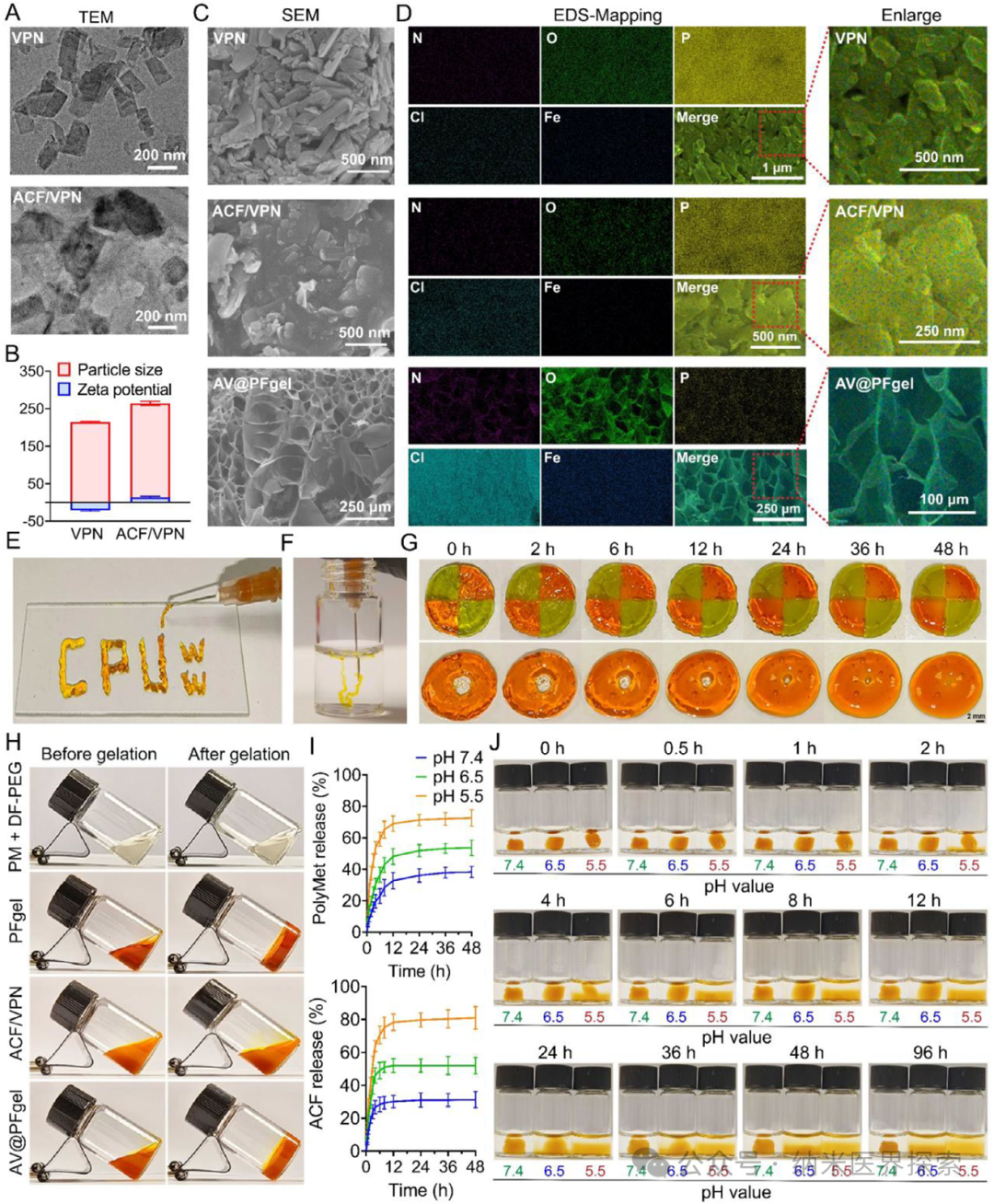
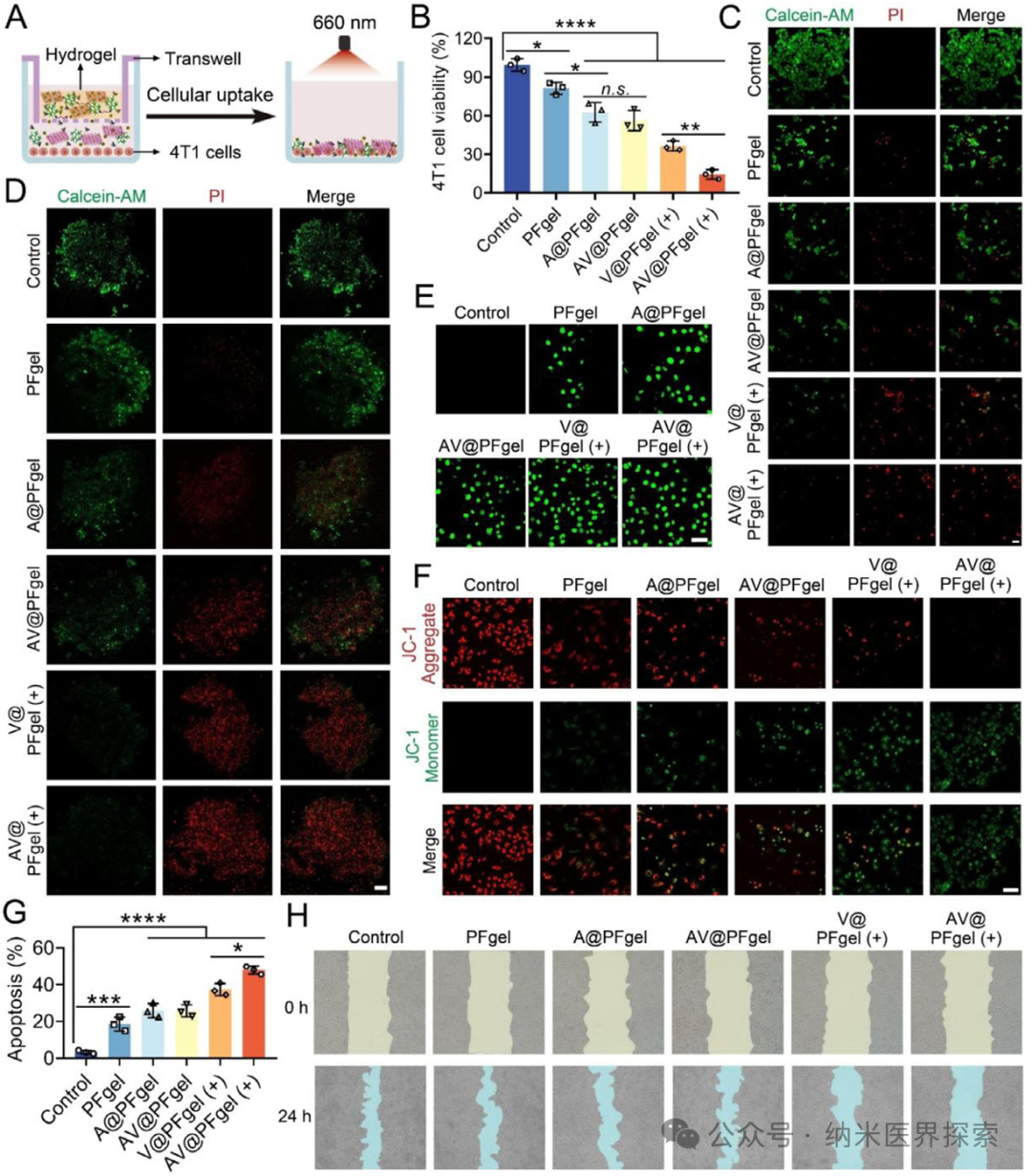
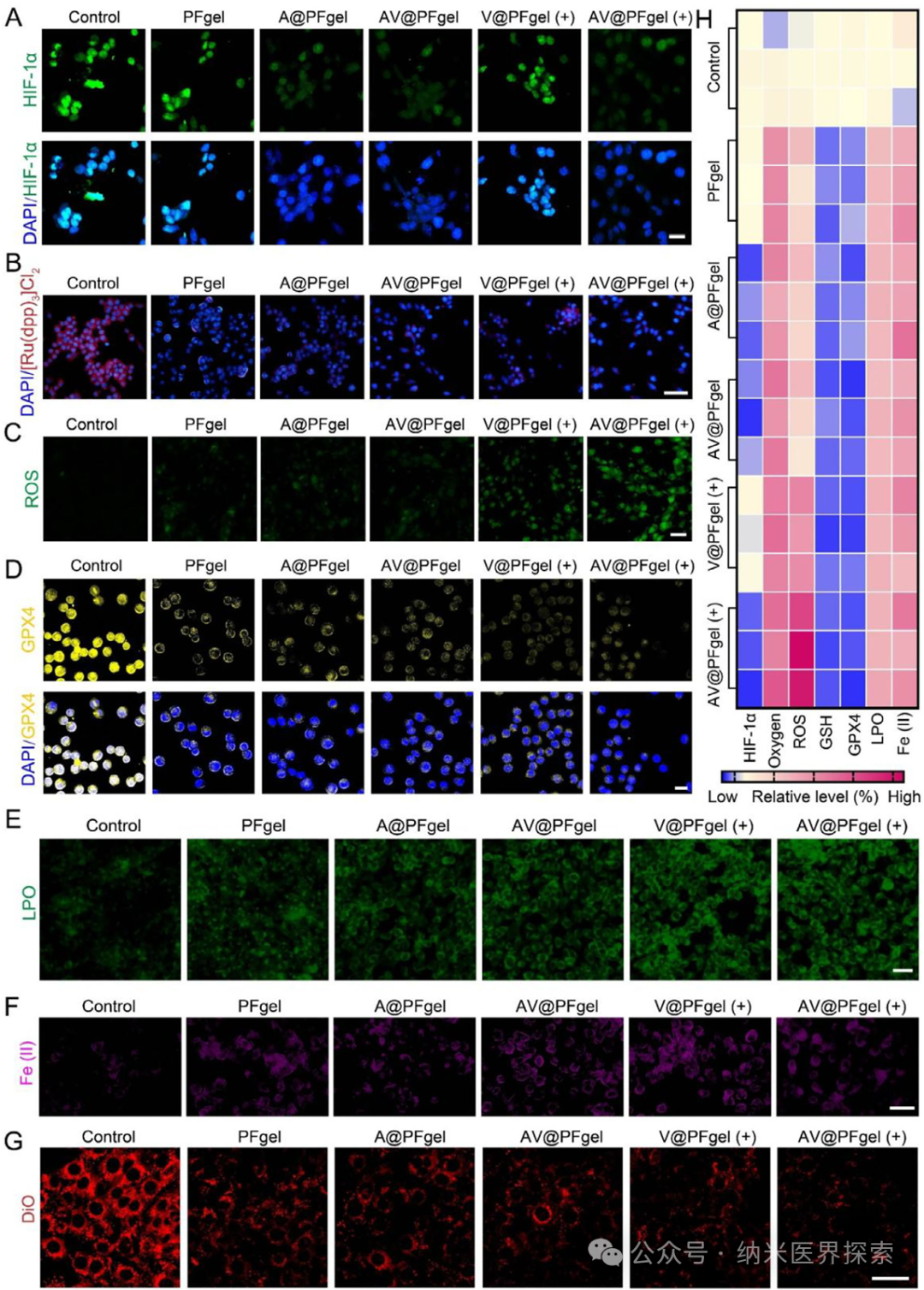
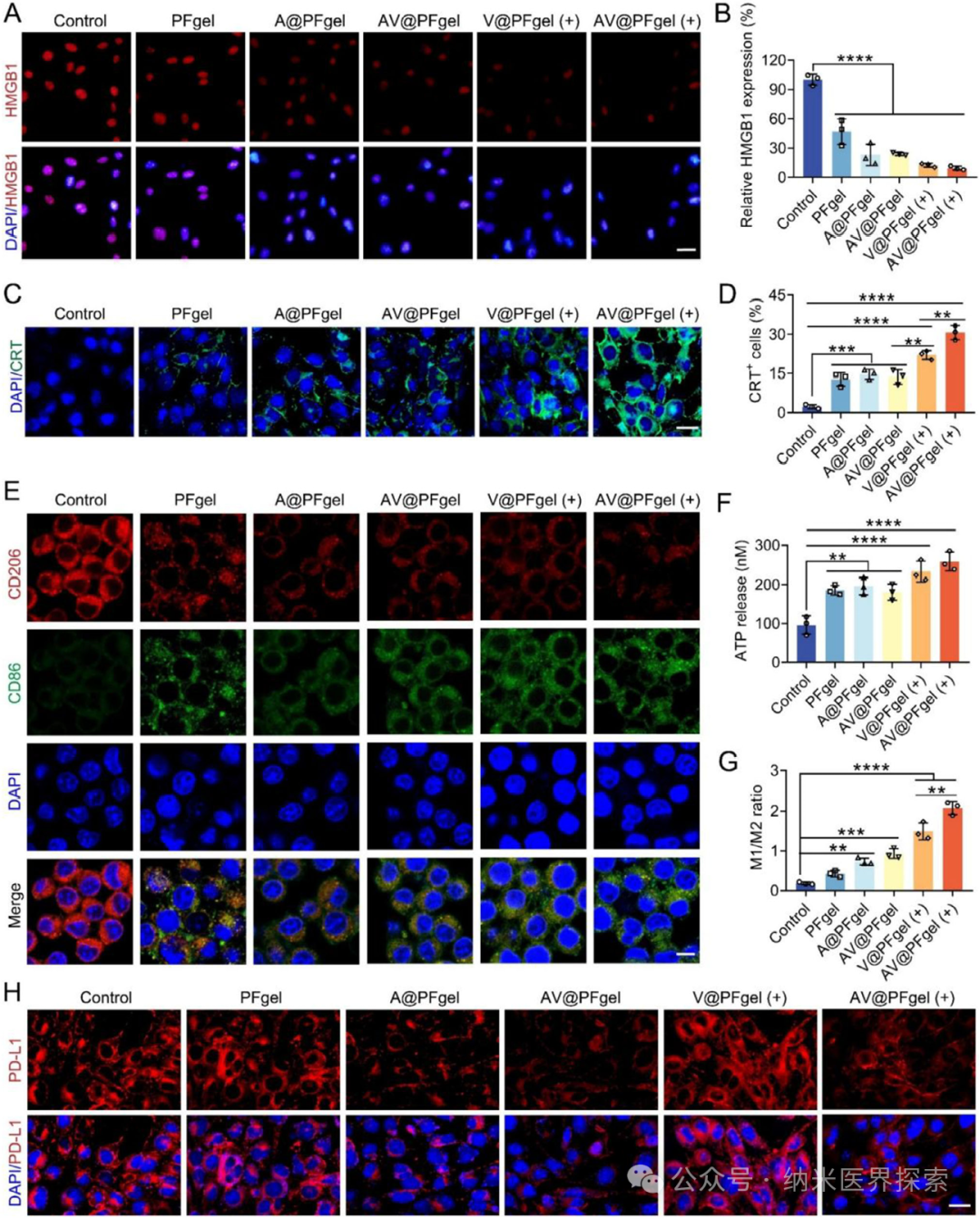
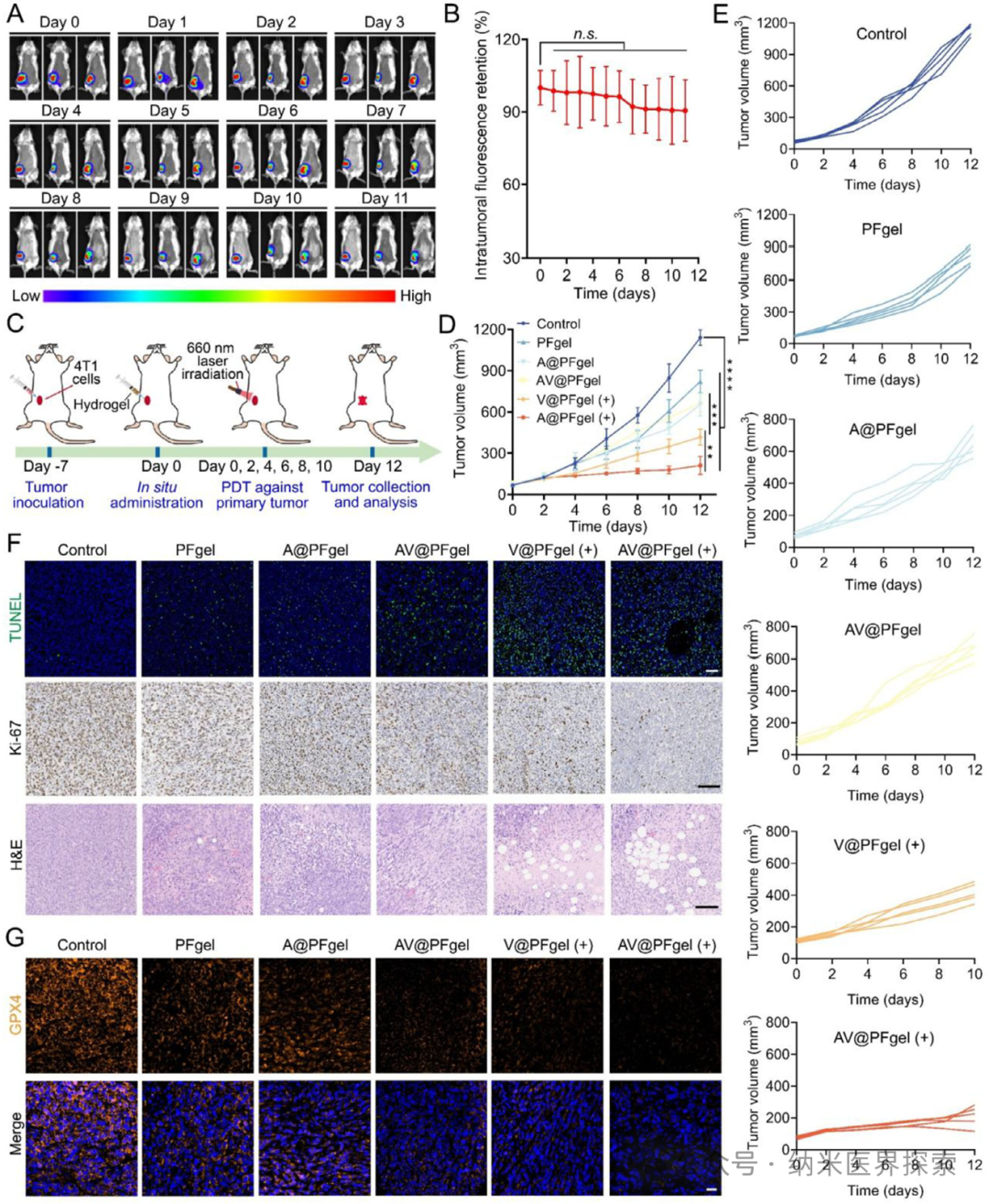
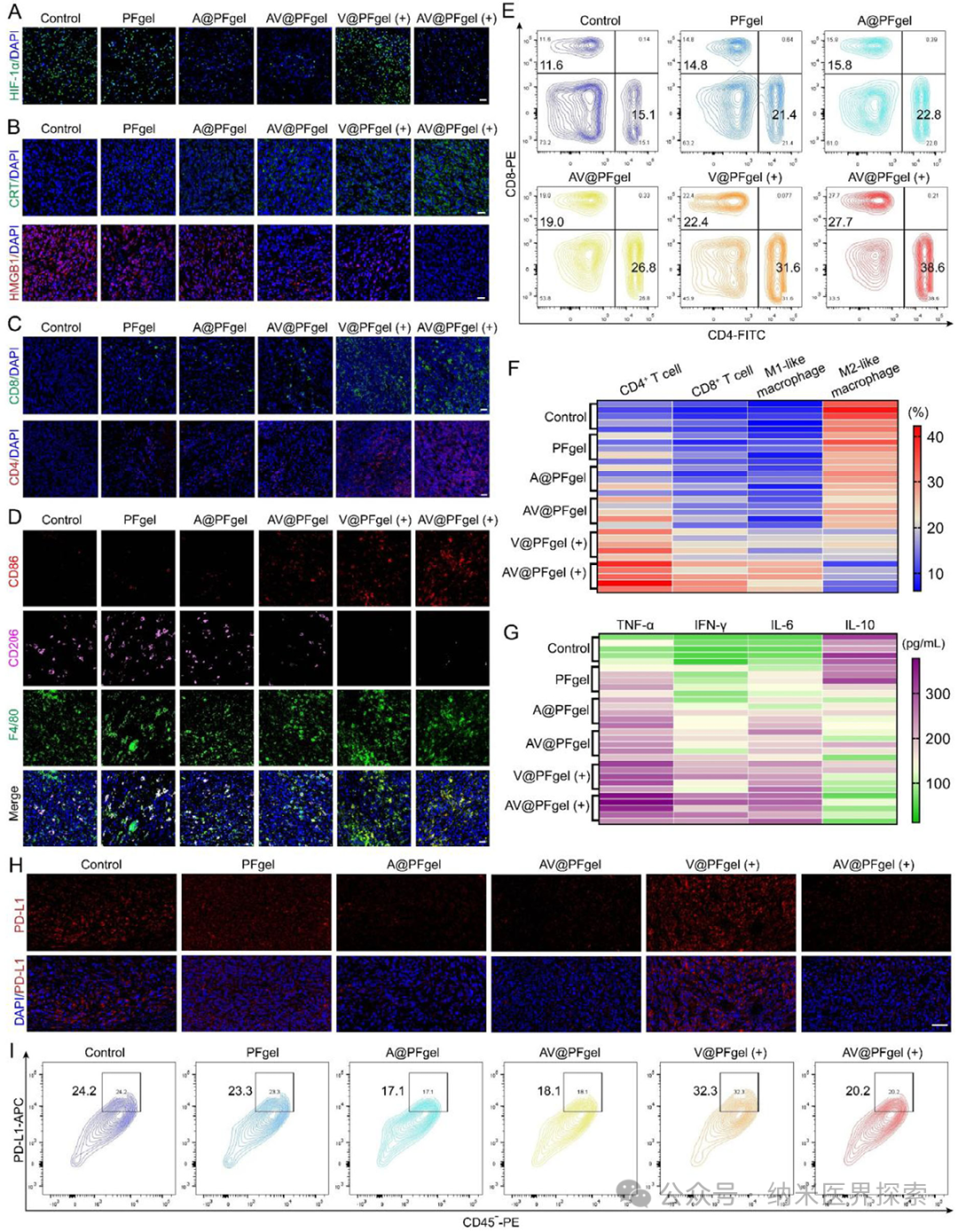
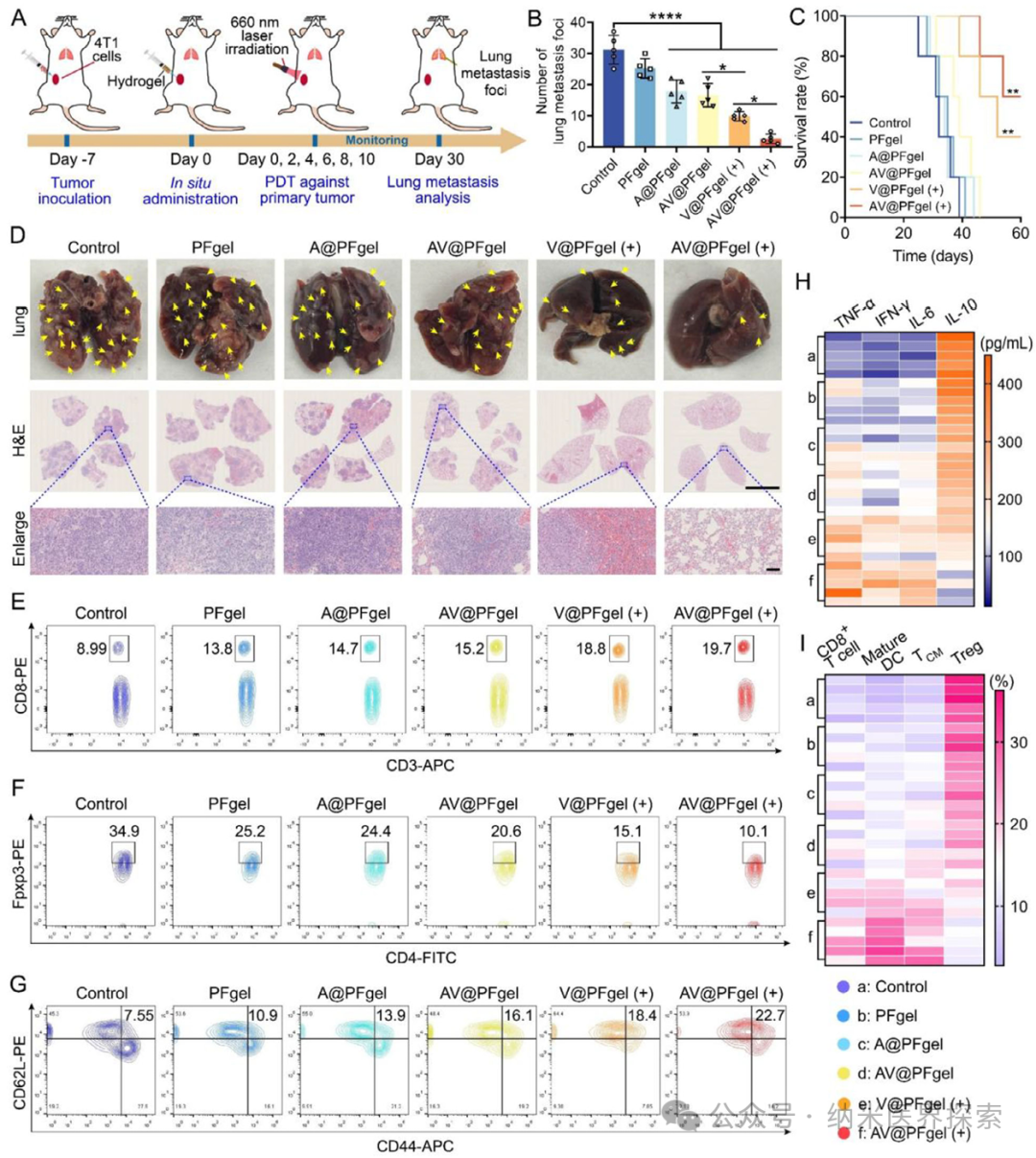
1️⃣ 首次将紫磷纳米片光动力治疗、铁死亡诱导、缺氧缓解、HIF-1α 抑制四大功能整合到单一可注射水凝胶体系,实现多机制协同抗癌2️⃣ 构建了双交联 pH 响应型水凝胶,在肿瘤酸性微环境精准降解,实现药物与活性成分的控释,兼顾注射性与自修复性3️⃣ 利用铁离子芬顿反应原位产氧,从根源解决光动力治疗的缺氧瓶颈,同时触发铁死亡,形成治疗正反馈4️⃣ 水凝胶载体兼具药物递送与免疫调控双重作用,重塑肿瘤免疫微环境,激活持久局部与全身抗肿瘤免疫5️⃣ 单次瘤内注射联合激光照射即可同时抑制原位肿瘤与肺转移,并建立长期免疫记忆,提升难治性三阴性乳腺癌治疗效果实体瘤普遍存在缺氧微环境,这不仅会促进肿瘤侵袭、转移和免疫逃逸,还会严重依赖氧气的光动力治疗效果大打折扣。缺氧会上调 HIF-1α,进一步诱导 PD-L1 高表达、招募调节性 T 细胞和肿瘤相关巨噬细胞,让肿瘤变成 “免疫沙漠”。光动力治疗本身还会消耗氧气,加重缺氧,形成恶性循环。铁死亡作为铁依赖性程序性死亡,能克服肿瘤凋亡耐药,还可触发免疫原性细胞死亡,但单独使用铁死亡或光动力都难以兼顾局部杀伤与全身免疫激活。传统递送体系合成复杂、生物相容性差、靶向性不足,无法实现缺氧缓解、铁死亡、光动力与免疫治疗的协同,临床转化难度大。三阴性乳腺癌易转移、预后差,现有疗法难以同时控制原位瘤与远处转移,急需一体化多功能治疗平台。作者设计开发了AV@PFgel 免疫工程化水凝胶,以聚二甲双胍为骨架,通过 Fe³+ 配位键与席夫碱双交联构建,负载阿克拉霉素 / 紫磷纳米片复合物。该水凝胶可注射、自修复,在肿瘤弱酸性环境下响应降解,缓慢释放聚二甲双胍、Fe³+ 和阿克拉霉素 / 紫磷纳米片。紫磷纳米片在 660 nm 激光下作为光敏剂产生活性氧,直接杀伤肿瘤并诱发免疫原性细胞死亡;Fe³+ 被还原为 Fe²+,通过芬顿反应分解肿瘤内 H₂O₂产氧、缓解缺氧,同时引发铁死亡,加剧脂质过氧化与细胞膜破裂;阿克拉霉素抑制 HIF-1α,阻断缺氧相关免疫抑制通路,下调 PD-L1。三者协同将肿瘤微环境重编程为免疫激活状态,激活 CD8+T 细胞、促肿瘤巨噬细胞极化,抑制调节性 T 细胞,实现对三阴性乳腺癌原位瘤与肺转移的高效抑制,同时建立长期免疫记忆。AV@PFgel 的制备流程及其结合光动力治疗(PDT)的抗肿瘤作用机制示意图作者首先通过液相剥离制备紫磷纳米片,静电吸附负载阿克拉霉素得到阿克拉霉素 / 紫磷复合物;再合成聚二甲双胍,与 Fe³+ 形成配位复合物,再与双苯甲醛 PEG 通过席夫碱反应构建双交联水凝胶,最终制得 AV@PFgel。对材料的形貌、粒径、电位、光谱、流变学性能、pH 响应降解与药物释放行为进行系统表征,验证水凝胶的注射性、自修复性与酸响应特性。Figure 1、AV@PFgel 的制备与表征。(A)紫磷纳米片(VPN)与阿克拉霉素 / 紫磷纳米片复合物(ACF/VPN)的透射电镜图;(B)VPN 与 ACF/VPN 的粒径及 Zeta 电位(n=3);(C)VPN、ACF/VPN 与 AV@PFgel 的扫描电镜图;(D)VPN、ACF/VPN 与 AV@PFgel 的能谱面扫;通过(E)在载玻片上书写字母、(F)用注射器挤出至 PBS 溶液(pH 7.4)中,评估 AV@PFgel 的可注射性;(G)AV@PFgel 的自修复性能表征;(H)AV@PFgel 凝胶化前后的溶胶 - 凝胶转变测试;(I)不同 pH 条件下 48 小时内聚二甲双胍(PolyMet)与阿克拉霉素(ACF)的累积释放曲线(n=3);(J)不同 pH 条件下 96 小时内 AV@PFgel 在 PBS 溶液中的状态观察。作者以 4T1 三阴性乳腺癌细胞为模型,检测材料细胞摄取、细胞毒性、凋亡、迁移侵袭能力;检测细胞内 HIF-1α、氧含量、活性氧、谷胱甘肽、GPX4、脂质过氧化物、Fe²+ 水平,验证缺氧缓解、光动力效应与铁死亡通路激活;检测免疫原性细胞死亡标志物、树突状细胞成熟、巨噬细胞极化及 PD-L1 表达,评估体外免疫激活效果。Figure 2、体外抗肿瘤活性。(A)采用 Transwell 共培养体系评估水凝胶制剂体外治疗效果的处理方法示意图;(B)不同处理 24 小时后 4T1 细胞的存活率(n=3);(C)不同处理 24 小时后钙黄绿素 - AM/PI 双染的 4T1 细胞(标尺:50 μm);(D)不同处理 24 小时后钙黄绿素 - AM/PI 双染的 4T1 肿瘤球(标尺:200 μm);(E)不同处理 24 小时后 4T1 细胞的 TUNEL 染色(标尺:50 μm)及(G)定量分析(n=3);(F)采用 JC-1 探针评估不同处理 24 小时后 4T1 细胞的线粒体功能(标尺:100 μm);(H)不同处理 24 小时后 4T1 细胞划痕愈合的照片。采用单因素方差分析及 Tukey 事后检验进行统计学分析,*p<0.05,**p<0.01,***p<0.001,****p<0.0001,n.s. 表示无统计学差异。作者构建了 4T1 原位乳腺癌小鼠模型,瘤内单次注射 AV@PFgel,联合 660 nm 激光照射,监测肿瘤生长、小鼠体重与生存期;检测肿瘤组织凋亡、增殖、缺氧、铁死亡、免疫细胞浸润与细胞因子水平;构建转移模型,观察肺转移灶数量,评估系统免疫激活与免疫记忆形成,同时验证材料体内生物相容性与降解性。Figure 3、体外抗肿瘤作用机制。(A)不同处理 24 小时后 4T1 细胞的 HIF-1α 免疫荧光染色(标尺:20 μm);(B)采用 [Ru (dpp)₃] Cl₂探针检测不同处理 24 小时后 4T1 细胞内氧含量(标尺:50 μm);(C)采用 DCFH-DA 探针检测不同处理 24 小时后 4T1 细胞内活性氧(ROS)水平(标尺:20 μm);(D)不同处理 24 小时后 4T1 细胞中 GPX4 的免疫荧光染色(标尺:20 μm);(E)采用 BODIPY⁵⁸¹/⁵⁹¹-C11 荧光探针检测不同处理 24 小时后 4T1 细胞内脂质过氧化物(LPO)水平(标尺:20 μm);(F)采用 FerroOrange 探针检测不同处理 24 小时后 4T1 细胞内 Fe²⁺含量(标尺:20 μm);(G)采用 DIO 染色观察不同处理 24 小时后 4T1 细胞膜完整性(标尺:20 μm);(H)不同处理 24 小时后 4T1 细胞内各生物标志物相对水平的热图分析(n=3)。Figure 4、体外免疫激活作用。(A)不同处理 24 小时后 4T1 细胞的 HMGB1 免疫荧光染色(标尺:20 μm)及(B)定量分析(n=3);(C)不同处理 24 小时后 4T1 细胞的 CRT 免疫荧光染色(标尺:20 μm)及(D)流式细胞术对 CRT 阳性细胞的定量分析(n=3);(E)不同处理 24 小时后 M2 型 RAW264.7 细胞中 CD86 与 CD206 的免疫荧光染色(标尺:20 μm)及(G)M1/M2 巨噬细胞比例的定量分析(n=3);(F)不同处理 24 小时后 4T1 细胞的胞外 ATP 释放量(n=3);(H)不同处理 24 小时后 4T1 细胞的 PD-L1 免疫荧光染色(标尺:20 μm)。采用单因素方差分析及 Tukey 事后检验进行统计学分析,**p<0.01,***p<0.001,****p<0.0001。Figure 5、体内瘤内滞留性能与抗肿瘤活性。(A)瘤内注射 Cy5 标记的水凝胶后,4T1 原位荷瘤小鼠的活体荧光成像及(B)肿瘤部位 Cy5 荧光强度随时间的定量分析(n=3);(C)体内抗肿瘤效果评估的治疗方案示意图;(D)不同处理期间 4T1 原位荷瘤小鼠的平均肿瘤生长曲线及(E)个体肿瘤生长曲线(n=5);(F)不同处理后 4T1 肿瘤组织切片的 TUNEL 染色(标尺:50 μm)、Ki-67 免疫组化(标尺:100 μm)与 H&E 染色(标尺:100 μm);(G)不同处理后 4T1 肿瘤组织切片中 GPX4 的免疫荧光染色(标尺:20 μm)。采用单因素方差分析及 Tukey 事后检验进行统计学分析,**p<0.01,***p<0.001,****p<0.0001,n.s. 表示无统计学差异。Figure 6、体内抗肿瘤机制与局部免疫激活。(A)不同处理后 4T1 原位肿瘤组织中 HIF-1α 的免疫荧光染色(标尺:20 μm);(B)不同处理后 4T1 原位肿瘤组织中 CRT 与 HMGB1 的免疫荧光染色(标尺:20 μm);(C)不同处理后 4T1 原位肿瘤组织中 CD8⁺ T 细胞与 CD4⁺ T 细胞的免疫荧光染色(标尺:20 μm);(D)不同处理后 4T1 原位肿瘤组织中肿瘤相关巨噬细胞(TAMs)的免疫荧光染色(标尺:20 μm);(E)不同处理后 4T1 原位肿瘤组织中 CD8⁺ T 细胞与 CD4⁺ T 细胞的流式代表性图;(F)流式细胞术分析不同处理后 4T1 原位肿瘤组织中各类免疫细胞占比的热图(n=5);(G)不同处理后 4T1 原位肿瘤组织中各类细胞因子水平的热图(n=5);(H)不同处理后 4T1 原位肿瘤组织中 PD-L1 表达的免疫荧光染色(标尺:50 μm);(I)不同处理后 4T1 原位肿瘤组织中 CD45⁺PD-L1⁺肿瘤细胞的流式代表性图。Figure 7、体内抗转移作用与全身免疫激活。(A)抗转移效果评估的治疗方案示意图;(B)不同处理后第 30 天肺转移结节数量的定量分析(n=5);(C)不同处理组小鼠 60 天内的生存率(n=5);(D)不同处理后小鼠肺组织的照片与组织学分析(上方标尺:5 mm,下方标尺:100 μm);不同处理后小鼠脾脏中(E)CD3⁺CD8⁺ T 细胞、(F)CD4⁺Foxp3⁺调节性 T 细胞、(G)CD44⁺CD62L⁺中枢记忆 T 细胞的流式代表性图;(H)不同处理后小鼠血清中各类细胞因子水平的热图(n=5);(I)不同处理后小鼠脾脏中各类免疫细胞占比的热图(n=5)。采用单因素方差分析及 Tukey 事后检验进行统计学分析,生存率采用 Kaplan-Meier 曲线与对数秩检验分析,*p<0.05,**p<0.01,****p<0.0001。本研究针对实体瘤缺氧导致光动力治疗失效、免疫抑制微环境难以逆转、三阴性乳腺癌易转移耐药等临床痛点,构建了一种集缺氧缓解、铁死亡、光动力治疗、免疫调控于一体的多功能免疫工程化水凝胶 AV@PFgel。该水凝胶以聚二甲双胍为骨架,经 Fe³+ 与席夫碱双交联而成,具备良好注射性、自修复性与肿瘤酸性微环境响应降解能力,可实现活性成分的瘤内长效控释。在激光照射下,紫磷纳米片高效产生活性氧执行光动力杀伤;Fe³+ 通过芬顿反应原位产氧缓解缺氧,同时触发铁死亡;阿克拉霉素抑制 HIF-1α,解除缺氧相关免疫抑制。多重机制协同触发肿瘤免疫原性细胞死亡,重塑肿瘤微环境,促进 CD8 + 细胞毒性 T 细胞浸润、肿瘤相关巨噬细胞向 M1 型极化,降低 PD-L1 与调节性 T 细胞水平。体内实验显示,单次瘤内注射联合激光照射可显著抑制原位三阴性乳腺癌生长,减少肺转移灶,延长小鼠生存期,并建立长期抗肿瘤免疫记忆。该水凝胶体系生物相容性好、降解安全,无需多次给药,操作简便,为缺氧实体瘤尤其是转移性三阴性乳腺癌提供了一种高效、可转化的一体化免疫治疗新策略,也为多功能纳米水凝胶在肿瘤协同治疗中的应用提供了新思路。
参考文献:
Cong Fu,Yuanyuan Cao,Yijun Mei,Qiaqia Xiao,Jingyi Hu,Zhencheng Gao,Xueyu Gao,Yi Hou,Fei Zhang,Guangda Zhu,Chao Zhang,Yue Yin,Hening Liu,Ruiyue Chen,Jinying Zhang,Xin Han,Yujun Song,Wei Wang,Lu Tang;
Immune-Engineered Hydrogels Combat Orthotopic and Metastatic Cancer via Hypoxia-Relieved Photodynamic Therapy and Ferroptotic Cell Death;
AdvancedFunctionalMaterials,2026;0:e29034;
https://doi.org/10.1002/adfm.202529034
信息来源:纳米医界探索



“汇聚南药”公众号所转载文章来源于其他公众号平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请在留言栏及时告知,我们会在24小时内删除相关信息。
本平台不对转载文章的观点负责,文章所包含内容的准确性、可靠性或完整性提供任何明示暗示的保证。