2026孤儿药报告解读:五款创新疗法如何改写罕见病治疗格局
发布时间:2026-03-23来源:药事纵横
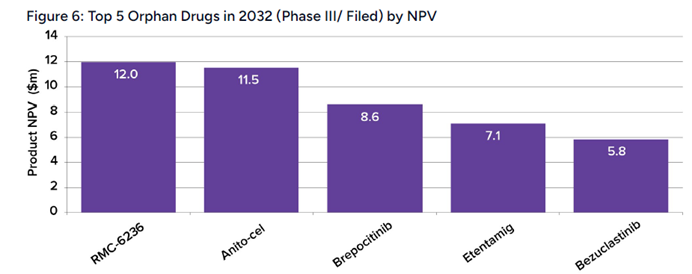
近日,行业权威机构Evaluate发布《2026年孤儿药报告》(2026 Orphan Drug Report),报告明确指出,尽管全球医药市场环境复杂多变,但孤儿药领域仍保持稳健增长态势,成为医药创新最具活力的赛道之一。报告重点梳理了5款值得关注的在研孤儿药,涵盖RAS抑制剂、CAR-T细胞疗法、双重激酶抑制剂、双特异性抗体等多个前沿领域,这些疗法凭借独特的作用机制、优异的临床数据,有望打破现有治疗瓶颈,改写罕见病及难治性肿瘤的治疗格局。一、RAS抑制剂破局胰腺癌,靶向治疗迎来“关键一跃”
在2026年孤儿药报告列出的重点疗法中,Revolution Medicines公司的Daraxonrasib(RMC-6236)尤为引人注目。作为一款口服选择性RAS抑制剂,该药凭借靶向激活状态RAS蛋白的技术突破,打破了RAS突变肿瘤“难靶向、疗效差”的困境,尤其在胰腺导管腺癌(PDAC)治疗中展现出强劲潜力,成为RAS靶向治疗领域的“关键一跃”。Daraxonrasib的核心技术突破,在于其独特的作用机制——能够精准靶向与GTP结合、处于激活状态的突变型及野生型RAS蛋白。长期以来,RAS突变被认为是“不可成药”靶点,核心原因在于RAS蛋白表面缺乏明确的小分子结合位点,且其与GTP的结合亲和力极强,传统抑制剂难以竞争结合。而Daraxonrasib通过结构优化,实现了对激活态RAS蛋白的特异性结合,能够有效抑制RAS蛋白的信号传导,阻断肿瘤细胞的增殖与存活,从根源上发挥抗肿瘤作用。2025年6月,该药获美国FDA授予突破性疗法认定,用于治疗既往接受治疗、携带KRAS G12突变的转移性胰腺导管腺癌患者,彰显了其临床价值。胰腺导管腺癌(PDAC)是一种恶性程度极高的罕见肿瘤,也是RAS突变的高发领域,其中KRAS G12突变占比极高,患者预后极差,5年生存率不足10%,一线治疗手段有限,临床需求极为迫切。Daraxonrasib在早期临床试验中展现出的优异数据,为PDAC患者带来了新的希望。2025年公布的临床试验结果显示,无论是单药治疗还是联合化疗,该药在一线转移性PDAC患者中均表现出积极疗效。在单药治疗队列中,Daraxonrasib每日一次300 mg给药,40例患者总体耐受性良好;在具有足够随访时长的38例患者中,客观缓解率(ORR)达47%,疾病控制率(DCR)达89%,中位随访时间为9.3个月,多数患者在数据截止时仍在接受治疗,展现出持久的疗效。更值得关注的是其联合治疗方案,Daraxonrasib每日一次200 mg联合吉西他滨和白蛋白紫杉醇(GnP)标准化疗,在40例RAS突变患者中总体安全性良好;在31例随访充分的患者中,ORR达到55%,DCR为90%,中位随访时间为6.9个月,缓解率较单药治疗进一步提升,体现出显著的协同效应。Daraxonrasib的研发进展,不仅为PDAC患者提供了全新的治疗选择,更对KRAS突变型肿瘤的治疗格局产生深远影响。此前,KRAS突变肿瘤的治疗多依赖化疗、免疫治疗等非特异性手段,疗效有限,而Daraxonrasib作为口服RAS抑制剂,实现了对KRAS突变的精准靶向,且联合化疗能够进一步提升疗效,有望成为KRAS突变型PDAC的一线标准治疗方案。目前,该药正在多项3期临床试验中用于治疗PDAC,同时其用于治疗非小细胞肺癌(NSCLC)的3期临床试验也在推进中,未来有望覆盖更多RAS突变型肿瘤,推动靶向治疗进入“RAS可及”的新时代。二、CAR-T再进阶,anito-cel如何实现疗效与安全性的“双赢”
CAR-T细胞疗法自问世以来,彻底改变了多发性骨髓瘤(MM)等血液系统罕见病的治疗格局,但传统CAR-T疗法往往面临疗效与安全性难以平衡的困境——要么缓解率不足,要么易引发严重免疫毒性。而吉利德科学/Arcellx联合开发的Anitocabtagene autoleucel(anito-cel),通过创新的结构设计,实现了疗效与安全性的“双赢”,成为2026年孤儿药报告中的焦点CAR-T疗法。anito-cel的核心优势,在于其采用了Arcellx开发的创新紧凑结合结构域——D-Domain。与传统CAR-T细胞的结合结构域相比,D-Domain体积更小、稳定性更强,能够在避免持续信号传导的情况下,实现较高水平的嵌合抗原受体(CAR)表达;同时,其被设计为可快速从B细胞成熟抗原(BCMA)靶点解离,这一独特特征能够有效避免CAR-T细胞的过度激活,减少细胞因子释放综合征(CRS)、神经毒性等严重免疫毒性的发生,同时保证对多发性骨髓瘤细胞的有效清除,实现“疗效最大化、毒性最小化”。优异的结构设计,转化为了突出的临床疗效。在2025年12月美国血液学会(ASH)年会上公布的关键性2期临床试验iMMagine-1数据显示,中位随访时间为15.9个月时,接受anito-cel治疗的复发/难治性多发性骨髓瘤患者,总缓解率(ORR)高达96%,完全缓解/严格完全缓解率(CR/sCR)达74%,这一缓解率显著高于现有CAR-T疗法。更重要的是,该药展现出良好的长期生存获益,患者24个月无进展生存率(PFS)为61.7%,24个月总生存率(OS)为83.0%,在复发/难治性MM患者中表现出卓越的持久疗效。anito-cel的巨大潜力,也吸引了吉利德科学的重金布局。2026年2月,吉利德科学宣布将斥资约78亿美元收购Arcellx公司,核心目的便是将anito-cel纳入自身肿瘤管线,强化其在多发性骨髓瘤治疗领域的竞争力。目前,FDA已受理anito-cel的生物制品许可申请(BLA),用于治疗复发/难治性MM,若顺利获批,将成为一款兼具高疗效与高安全性的CAR-T疗法,改写复发/难治性MM的治疗格局。从行业竞争来看,anito-cel的优势在于其差异化的结构设计的带来的安全性优势——相较于现有CAR-T疗法,其免疫毒性发生率更低,患者耐受性更好,更适合用于多线治疗失败的复发/难治性MM患者。随着吉利德科学的收购与推广,anito-cel有望快速抢占市场份额,同时推动CAR-T疗法的技术升级,引领血液系统罕见病治疗向“高效、安全”的方向发展。三、TYK2/JAK1双重抑制,brepocitinib能否终结皮肌炎“无药可用”困境
皮肌炎(DM)是一种罕见的自身免疫性疾病,以皮肤和肌肉炎症为主要特征,患者常表现为肌肉无力、皮肤红斑、关节疼痛等症状,严重时可累及内脏器官,甚至危及生命。长期以来,皮肌炎缺乏针对性的靶向治疗药物,临床治疗主要依赖糖皮质激素、免疫抑制剂等非特异性手段,疗效有限且不良反应较多,患者面临“无药可用”的困境。而Priovant Therapeutics公司的Brepocitinib,作为一款选择性TYK2和JAK1双重抑制剂,有望终结这一困境,成为首个获批用于治疗皮肌炎的靶向疗法。Brepocitinib的核心作用机制,在于其能够双重抑制TYK2和JAK1激酶,进而阻断与自身免疫相关的多重关键细胞因子的信号传导,包括I型IFN、II型IFN、IL-6、IL-12和IL-23等。这些细胞因子在皮肌炎的发病机制中发挥关键作用,过度激活会导致皮肤和肌肉的异常炎症反应。通过双重抑制TYK2/JAK1,brepocitinib能够从源头抑制炎症反应,缓解患者症状,且相较于单一JAK抑制剂,其作用更广泛、更精准,能够减少单一靶点抑制带来的不良反应。该药的3期VALOR临床试验数据,充分印证了其在皮肌炎治疗中的优异疗效。VALOR是一项全球多中心3期临床试验,241例皮肌炎患者按1:1:1比例随机分配至brepocitinib 30 mg组、15 mg组或安慰剂组。研究结果显示,30 mg剂量组在第52周时,主要终点肌炎总改善评分(TIS)相较安慰剂达到统计学显著且具有临床意义的改善——TIS作为涵盖6项疾病活动指标的综合终点,能够全面评估患者的皮肤、肌肉受累情况,其改善意味着患者整体病情的缓解。更值得关注的是,brepocitinib的治疗获益具有“快速、持久”的特点,最早在第4周即已显现,且在整个为期一年的双盲治疗期间持续保持。除主要终点外,30 mg剂量组在全部9项关键次要终点上同样优于安慰剂,包括皮肤受累、肌肉受累及糖皮质激素减量等指标,其中超过三分之二接受30 mg治疗的患者达到TIS40标准(即TIS≥40分),这一改善幅度为最小临床重要差异的两倍;更有超过一半患者在达到TIS40的同时,将类固醇依赖剂量降低至每日≤2.5 mg,有效减少了长期使用糖皮质激素带来的不良反应。目前,美国FDA已受理brepocitinib用于治疗皮肌炎的新药申请(NDA),并授予优先审评资格,若顺利获批,将成为首个获批用于治疗皮肌炎的靶向疗法,彻底填补该领域的治疗空白。此外,brepocitinib的适应症布局正在持续拓展,目前还在3期临床试验中用于治疗非感染性葡萄膜炎(NIU),治疗皮肤结节病的2期临床试验也在进行中,未来有望覆盖更多自身免疫性罕见病,成为自身免疫领域的“重磅疗法”。四、双特异性抗体再发力,etentamig组合疗法重塑MM治疗边界
双特异性抗体作为近年来的研发热点,凭借其能够同时结合两个靶点、精准杀伤肿瘤细胞的优势,在多发性骨髓瘤(MM)等罕见血液肿瘤治疗中展现出巨大潜力。艾伯维公司的Etentamig,作为一款靶向BCMA和CD3的双特异性T细胞衔接器,通过与泊马度胺和地塞米松(POM+DEX)的联合策略,在多线治疗失败的复发/难治性MM患者中展现出显著疗效,有望重塑MM的治疗边界。Etentamig的作用机制具有高度特异性:其一端结合多发性骨髓瘤细胞表面的BCMA抗原,另一端结合T细胞表面的CD3分子,通过“桥梁作用”将T细胞招募至肿瘤细胞周围,激活T细胞的杀伤功能,从而特异性清除MM细胞。与传统抗体药物相比,双特异性T细胞衔接器能够直接激活内源性T细胞,无需体外培养,给药更便捷,且对肿瘤细胞的杀伤效率更高,尤其适合用于复发/难治性患者。考虑到复发/难治性MM患者多经过多线治疗,肿瘤细胞易产生耐药性,艾伯维采用了“etentamig+POM+DEX”的联合治疗策略,通过机制协同提升疗效。2025年12月ASH年会上公布的1b期临床试验结果显示,该联合疗法在既往接受过多种治疗(至少3线既往治疗)的复发/难治性MM患者中表现出显著疗效:来自剂量递增阶段(n=82)的初步数据显示,中位随访时间为23个月时,联合治疗的总缓解率(ORR)达81%,达到非常好部分缓解或更佳(≥VGPR)的患者比例为72%,在多线治疗失败的患者群体中,这一数据尤为亮眼。更重要的是,该联合疗法展现出持久的缓解趋势,截至数据分析时,缓解持续时间(DoR)尚未达到,意味着多数患者能够长期获益,有效延长了患者的生存期。此外,该联合疗法的安全性良好,未出现不可耐受的严重不良反应,患者耐受性较好,适合长期治疗。艾伯维预计在2026年获得etentamig组合疗法治疗复发/难治性MM患者的3期临床试验结果,并计划在2027年递交该疗法的监管申请。若顺利获批,etentamig组合疗法将为多线治疗失败的复发/难治性MM患者提供全新的治疗选择,打破现有治疗瓶颈,重塑MM的治疗格局。从市场潜力来看,复发/难治性MM患者群体庞大,且现有治疗手段有限,etentamig组合疗法凭借优异的疗效,有望成为该领域的核心治疗方案,具备广阔的市场前景。五、从SM到GIST,bezuclastinib如何打通KIT突变“双通道”
系统性肥大细胞增多症(SM)和胃肠道间质瘤(GIST)均为与KIT基因突变相关的罕见疾病,其中KIT D816V突变是SM的关键驱动因素,而KIT第17外显子突变也常见于晚期GIST患者。长期以来,针对这些突变的靶向治疗药物有限,患者疗效不佳、生存期较短。Cogent Biosciences公司的Bezuclastinib,作为一种选择性酪氨酸激酶抑制剂(TKI),能够强效抑制KIT D816V及第17外显子的其他突变,成功打通SM与GIST治疗的“双通道”,成为该领域的突破性疗法。Bezuclastinib的核心优势在于其高度的选择性——专门针对KIT D816V突变以及KIT第17外显子的其他突变,对正常细胞的KIT激酶影响较小,因此不良反应发生率更低,患者耐受性更好。与传统TKI药物相比,bezuclastinib对KIT突变的抑制活性更强,能够更精准地阻断肿瘤细胞的信号传导,从而实现更好的治疗效果。在系统性肥大细胞增多症(SM)领域,bezuclastinib已取得重要突破。Cogent Biosciences已于2025年12月向美国FDA递交新药申请,寻求批准bezuclastinib用于治疗非进展期系统性肥大细胞增多症,为这类患者提供了针对性的靶向治疗选择。而在胃肠道间质瘤(GIST)领域,该药的表现更为亮眼:2026年1月,bezuclastinib获得FDA授予的突破性疗法认定,与sunitinib联用,治疗既往接受过imatinib治疗的GIST患者。这一突破性疗法认定的授予,主要基于PEAK试验的研究结果。该试验在主要终点无进展生存期(PFS)方面显示出显著且具有高度统计学意义的临床获益:与当前标准治疗相比,bezuclastinib联合治疗组的疾病进展或死亡风险降低了50%(HR=0.50,95% CI:0.39–0.65);经盲法独立中心评估(BICR)判定,联合治疗组的中位无进展生存期为16.5个月,而活性对照组仅为9.2个月,疗效提升显著,为既往接受过imatinib治疗的GIST患者带来了新的希望。Bezuclastinib的研发进展,不仅填补了SM与GIST领域KIT第17外显子突变靶向治疗的空白,更体现了精准治疗时代下“突变导向”的治疗理念。Cogent Biosciences公司表示,预计在2026年4月完成递交bezuclastinib用于治疗GIST的NDA,若顺利获批,将成为首个专门针对KIT第17外显子突变的靶向疗法,打通SM与GIST治疗的“双通道”,为两类罕见病患者提供精准、高效的治疗选择,推动相关领域的治疗进入“精准靶向”新时代。五款在研疗法,五个不同的技术路径,却共同指向同一个方向——为罕见病患者带来更具针对性、更安全的治疗选择。在政策鼓励、技术突破与资本加持的多重推动下,孤儿药正从“边缘”走向“主流”。未来,我们有理由相信,更多曾被忽视的疾病将迎来属于它们的“高光时刻”。[1] Evaluate Releases 2026 Orphan Drug Report. Retrieved March 13, 2026, from[2] Orphan Drugs Outlook 2032: Sales, Pipeline & Policy for Rare Diseases. Retrieved March 13, 2026, from[3] AbbVie to Feature New Data at ASH 2025 Showcasing Continued Advances Across Novel Treatment Modalities in Multiple Blood Cancers. Retrieved March 13, 2026, from[4] Cogent Biosciences Highlights Additional Data with Six Bezuclastinib Posters from SUMMIT Trial at 2026 AAAAI Annual Meeting. Retrieved March 13, 2026, from[5] Cogent Biosciences to Initiate New Drug Application (NDA) Submission for Bezuclastinib Under Real-Time Oncology Review (RTOR). Retrieved March 13, 2026, from
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。