再注册工艺验证不合格、违反GMP逾期不改正,两药企被罚!

近日,江苏药监局发布对江苏涟水制药有限公司的行政处罚书,该公司为产品再注册及工艺再验证按计划生产了涉案双氯芬酸钾片(未上市销售),后经检验溶出度不合格,判定其违反了《中华人民共和国药品管理法》第九十八条第三款第七项之规定。判处没收劣药双氯芬酸钾片17862盒,没收违法所得没收非法财物的金额:2.6793万元,如下:
再注册工艺验证不合格
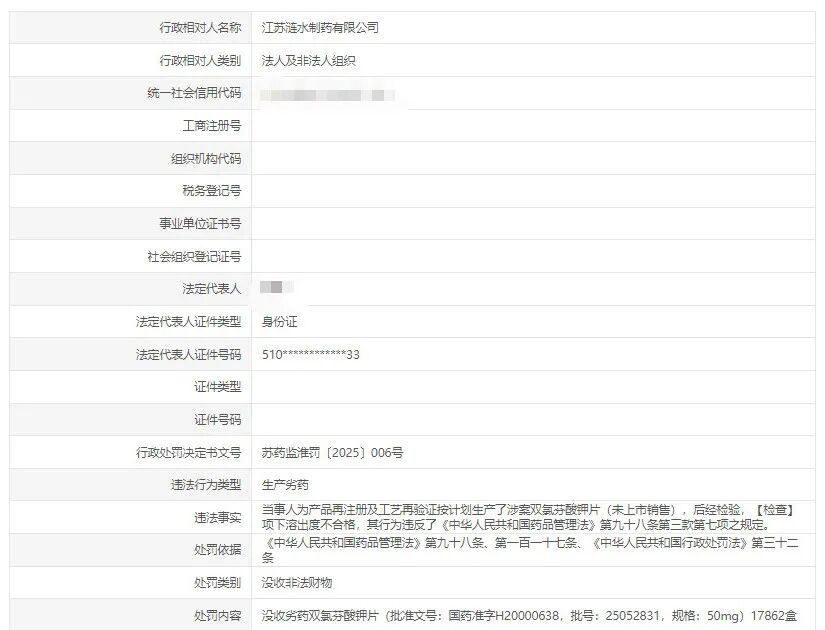
行政相对人名称:江苏涟水制药有限公司
行政处罚决定书文号:苏药监淮罚〔2025〕006号
违法行为类型:生产劣药
违法事实:当事人为产品再注册及工艺再验证按计划生产了涉案双氯芬酸钾片(未上市销售),后经检验,【检查】项下溶出度不合格,其行为违反了《中华人民共和国药品管理法》第九十八条第三款第七项之规定。
处罚依据:《中华人民共和国药品管理法》第九十八条、第一百一十七条、《中华人民共和国行政处罚法》第三十二条
处罚类别:没收非法财物
处罚内容:没收劣药双氯芬酸钾片(批准文号:国药准字H20000638,批号:25052831,规格:50mg)17862盒
没收违法所得没收非法财物的金额(万元):2.6793

违反GMP逾期不改正
2026年03月23日,河北药监局发布了对河北胡氏宇博药业有限公司的处罚通告,该公司因违反GMP且逾期不改正被罚款35万,如下:
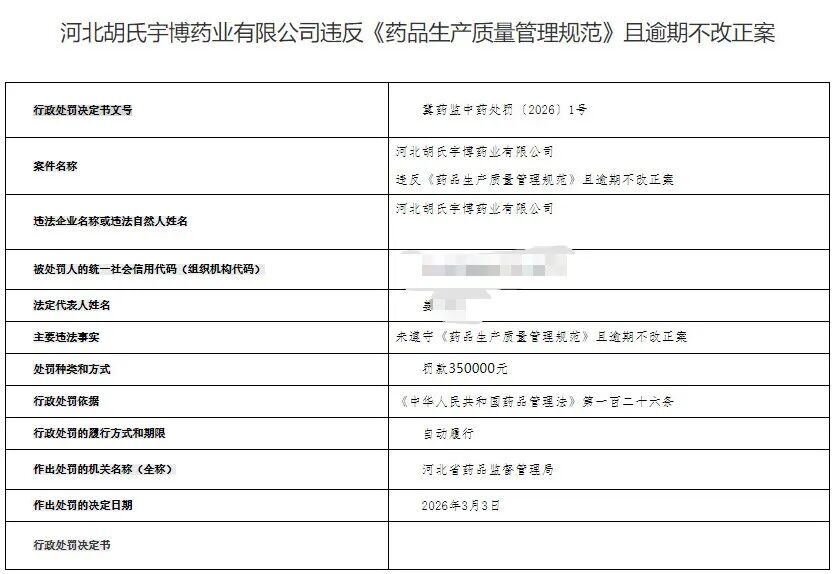
行政处罚决定书文号:冀药监中药处罚〔2026〕1号
案件名称:河北胡氏宇博药业有限公司违反《药品生产质量管理规范》且逾期不改正案
违法企业名称或违法自然人姓名:河北胡氏宇博药业有限公司
主要违法事实:未遵守《药品生产质量管理规范》且逾期不改正案
处罚种类和方式:罚款350000元
行政处罚依据:《中华人民共和国药品管理法》第一百二十六条

【点这里,进入医药数据库,搜索下载原文】

药学检测服务推荐
一、化药检测服务
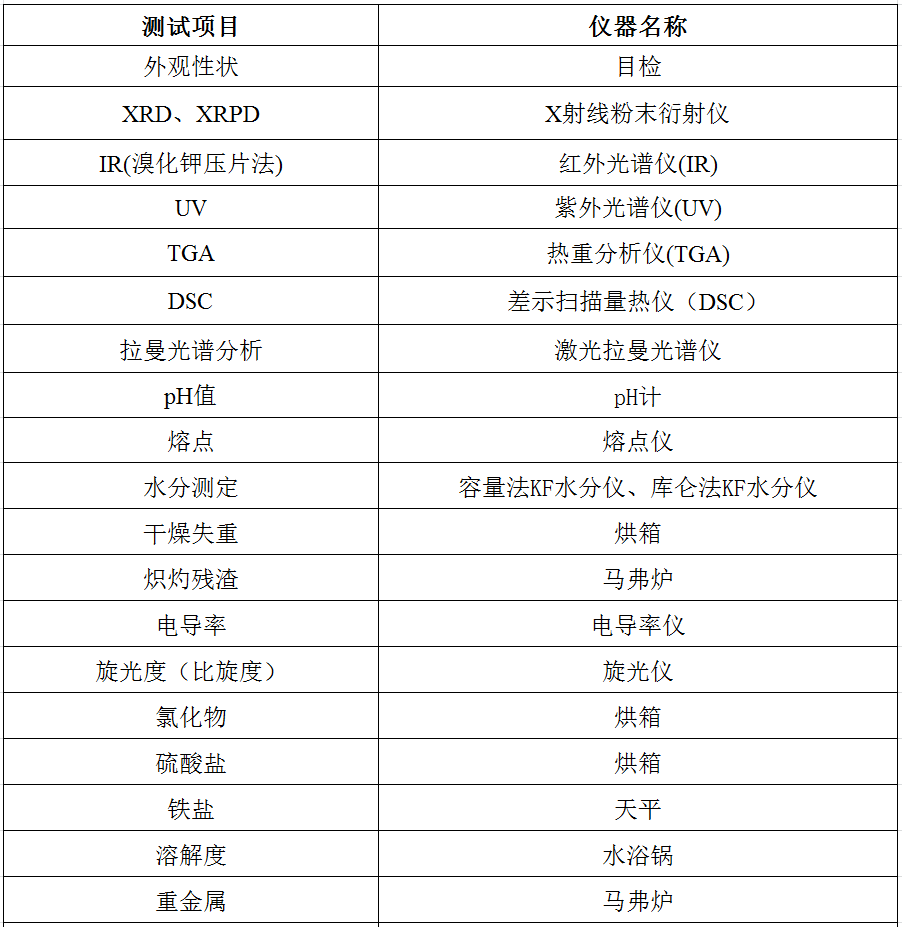



二、化药质量研究服务
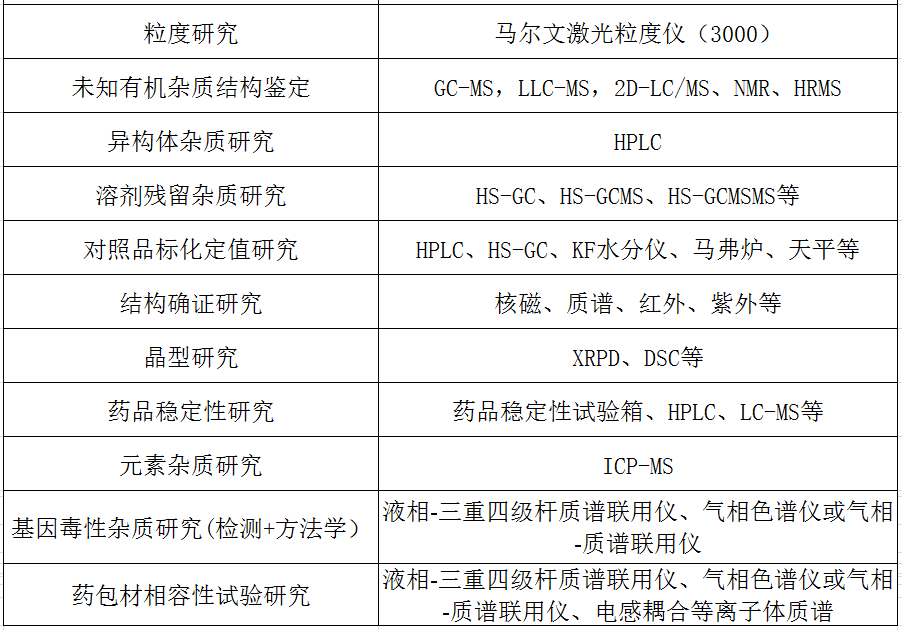

三、生物药检测服务

四、生物药质量研究服务
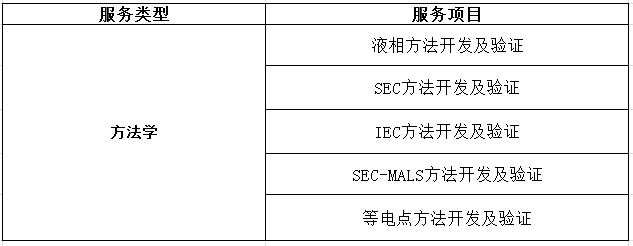
五、药品毒理安全性评价服务

六、药品包装材料理化检测
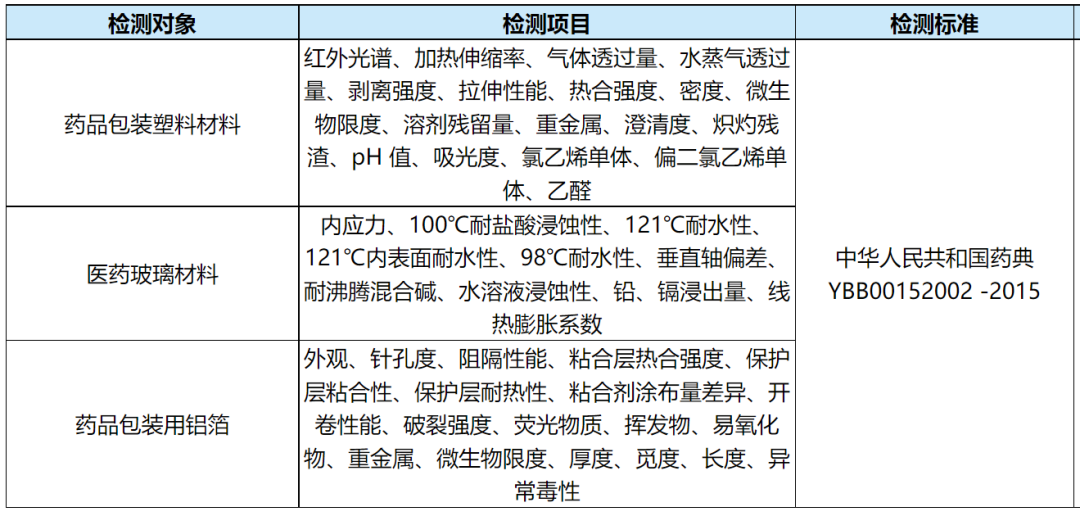
实验室资质:CMA、CNAS
实验室所在地:上海、苏州、青岛、广州、福州
联系我们:151-9002-7486/181-0068-0718(微信同号)


文章来源:GMP办公室,本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的单位、媒体或个人可与我们联系(274190388@qq.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。


