诺和诺德被FDA重罚,这件事你看懂了吗?
2026年3月5日,FDA向诺和诺德发出一封警告信。
如果你只是扫了一眼新闻标题,大概会觉得:哦,又是药企被罚,没啥稀奇。
但如果你真的这么想,你就错过了这条新闻里最致命的东西。
这次罚的,不是生产质量,不是数据造假,而是药物警戒(PV)体系的系统性崩塌。
换句话说,诺和诺德不是“做错了什么”,而是“整个安全监测的脑子坏掉了”。
01 你以为的合规,和真正的合规,差了十万八千里
很多人以为药企的合规就是“按规定办事”。但诺和诺德的案例告诉你:你的“规定”本身,可能就是违法的。
FDA的警告信里翻出了一条致命证据:诺和诺德的内部SOP Q014048明确规定——如果报告人自己认为事件与药物“无关”,就可以直接拒绝上报。

什么意思?一个患者吃了你的药,中风了,瘫痪了。患者自己说“我觉得可能和药没关系”。诺和诺德的人一看,行,你说没关系,那我就不报了。
完美闭环。
但FDA的法规是怎么写的?21 CFR 314.80写得清清楚楚:只要满足四要素——可识别患者、报告人、产品、事件——无论因果关系如何,都必须上报。
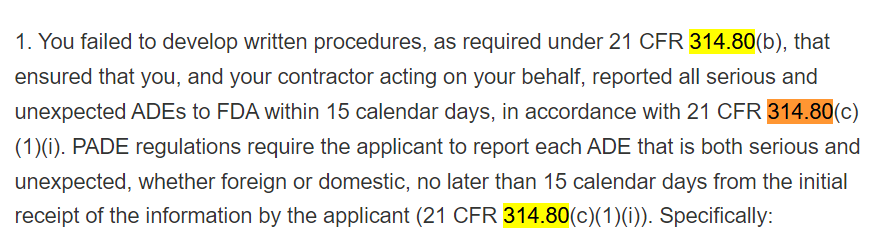
诺和诺德用自己的逻辑,替FDA做了决定。这不是失误,这是“系统性违规”。
02 你以为的整改,和真正的整改,中间隔着一堵墙
收到FDA的483表之后,诺和诺德做了什么?他们提交了7次整改更新。
7次。
每次都是“我们改了,我们优化了,我们培训了”。每次都被FDA驳回:不充分、不彻底、无效。
为什么?因为诺和诺德一直在做“表面整改”——改文件、换外包商、删条款。但FDA要的是“系统能力”:你的IT能不能自动抓取所有严重事件?你的外包呼叫中心有没有人盯着?你的员工还敢不敢因为“感觉无关”就扔报告?
答案是没有。FDA的检查员在现场发现:大量案件在系统里长期处于“待审查”状态,形同虚设;外包公司的关键通话录音被随意丢弃;一起自杀死亡案件,企业压根没启动任何调查。
这不是技术问题,这是管理层面的底线失守。
03 你以为的风险,和真正的风险,差了5000起诉讼
有读者可能会问:不就是晚报几份报告吗?有那么严重吗?
我告诉你有多严重。
截至2026年3月,已有超过5000名患者对诺和诺德提起诉讼。诉讼内容是什么?指控该公司低估了GLP-1药物的健康风险。也就是说,患者认为:如果你们早把真实的不良反应数据报告给FDA,我就不会吃这个药,或者至少知道风险再决定。

一位代理数千起案件的律师在接受采访时说了一句非常重的话:“除了阿片类药物时代,我没见过这么严重的违规。”
而FDA的警告信里还有一句更狠的:“基于检查结果和你的回复,我们严重怀疑这种违规行为是否覆盖了你的全部产品线。”
什么意思?你现在看到的5个案例,可能只是冰山一角。那些没被翻出来的、没被患者起诉的、还没被FDA查到的,还有多少?
04 你以为的并购,和真正的并购,是福是祸?
2024年,诺和诺德花了165亿美元收购Catalent。当时所有分析师的评价都是:解决了产能瓶颈,补上了供应链短板。
结果呢?接手之后才发现,这哪是“产能”,这是个“雷”。
2025年6月到7月,FDA对布卢明顿工厂的检查发现:无菌生产环境中存在猫毛和人类毛发。
你没看错。猫毛。(cat and human hair in vial stoppers, along with pest infestations in classified areas)

这家工厂还为Regeneron和Scholar Rock代工生产药品。结果呢?Scholar Rock的SMA新药因为这家工厂的问题,直接被FDA拒批。Regeneron的Eylea HD审批也被迫延期。
这就是165亿美元买来的“资产”。当你以为自己在扩张的时候,合规的窟窿已经大到吞掉整个业务。
05 写在最后
诺和诺德这一跤,摔出了整个行业的痛点。
第一,PV不是“成本”,是“生命线”。 你可以在市场部烧钱,可以在研发部烧钱,但如果你在药物警戒上省钱,FDA会让你把之前赚的钱,连本带利吐出来。
第二,外包不是“免责金牌”。 诺和诺德的呼叫中心外包了,SOP写错了,结果呢?FDA罚的还是诺和诺德。你的外包商犯的错,就是你的错。
第三,并购不是“买保险”。 165亿美元买来的工厂,如果合规有问题,就是165亿美元买的负债。尽职调查的时候,少查一个环节,上市后就是一年的噩梦。
《药物安全与药物警戒》这本书里有一句话,我印象很深:“药物警戒的本质不是报告,而是责任。”
诺和诺德用7次被驳回的整改方案,证明了这句话的含金量。
你以为的合规,是“该报的都报了”。真正的合规,是“连‘感觉无关’的报告都不会被扔掉”。
你以为的整改,是“发个声明、改个SOP”。真正的整改,是“从IT系统到外包管控,从人员培训到文化建设,全线重构”。
医药产业这个圈子,从来不缺故事,缺的是能看透故事的人。
这本书,我建议你翻一翻。不是为了应付检查,是为了不让自己的公司,成为下一个被FDA“公开处刑”的案例。
(本文提及的《药物安全与药物警戒》,是理解全球药品监管逻辑的入门必读。你不需要成为PV专家,但你需要知道:为什么你的同行,正在把这本书翻烂。)

