海思科两款重磅1类新药,拟纳入突破性治疗!

三月春意正浓,海思科在创新药研发赛道上迎来了爆发式收获。3月27日,据CDE官网公示,海思科子公司西藏海思科制药申报的1类新药HSK39004吸入粉雾剂拟纳入突破性治疗品种,用于慢性阻塞性肺疾病(COPD)的维持治疗。
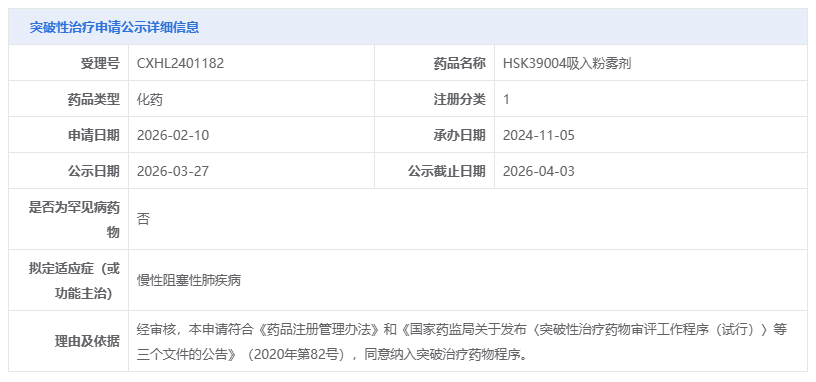
截图来源:CDE官网
而就在短短两周前(3月13日),公司另一款自主研发的1类新药HSK31679片也被正式纳入突破性治疗名单,适应症为代谢功能障碍相关性脂肪性肝炎(MASH)。
01
双轮驱动,差异化布局呼吸系统与肝病领域
此次备受瞩目的HSK39004是一款PDE3/4双重抑制剂,拥有吸入混悬液、吸入粉雾剂两种剂型。不同于单一靶点药物,HSK39004通过抑制PDE3和PDE4产生协同效应,既能扩张支气管,又能减少炎症因子释放,从而全面改善COPD患者的气流受限和气道炎症。
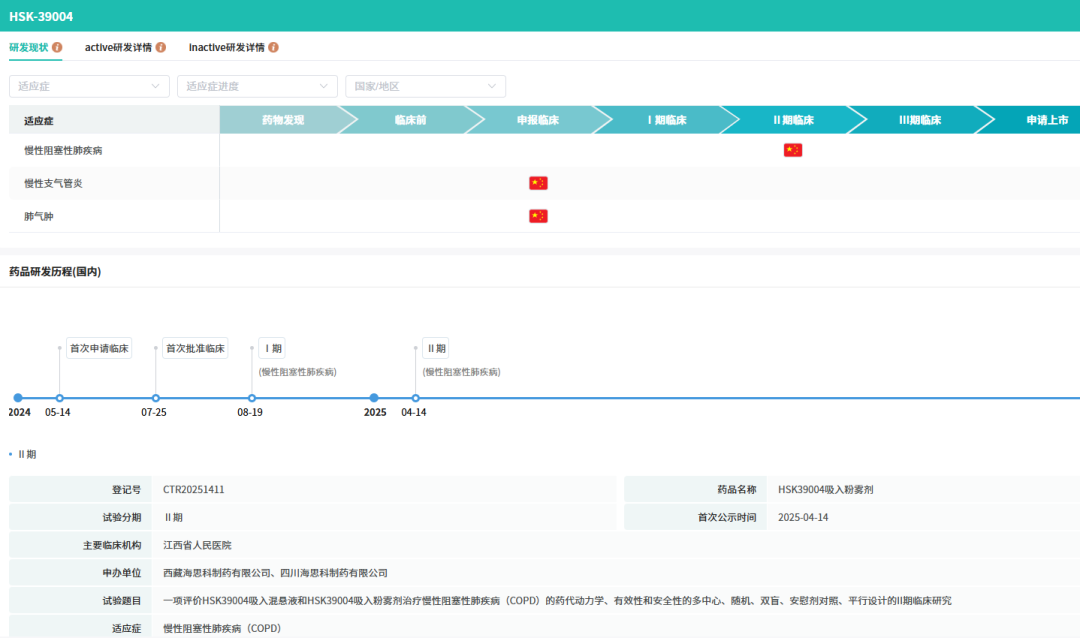
目前,该药物已在中国启动II期临床试验。值得关注的是,早在2026年1月,海思科便以此款药物进行了“NewCo”模式出海,授权美国AirNexis Therapeutics公司在除大中华区以外的全球范围内开发、生产和商业化HSK39004的独家权利,交易潜在金额超10亿美元。摩熵医药数据库显示,目前全球仅有一款PDE3/4抑制剂获批上市,海思科HSK39004在全球研发进度中位列第三,极具市场竞争力。
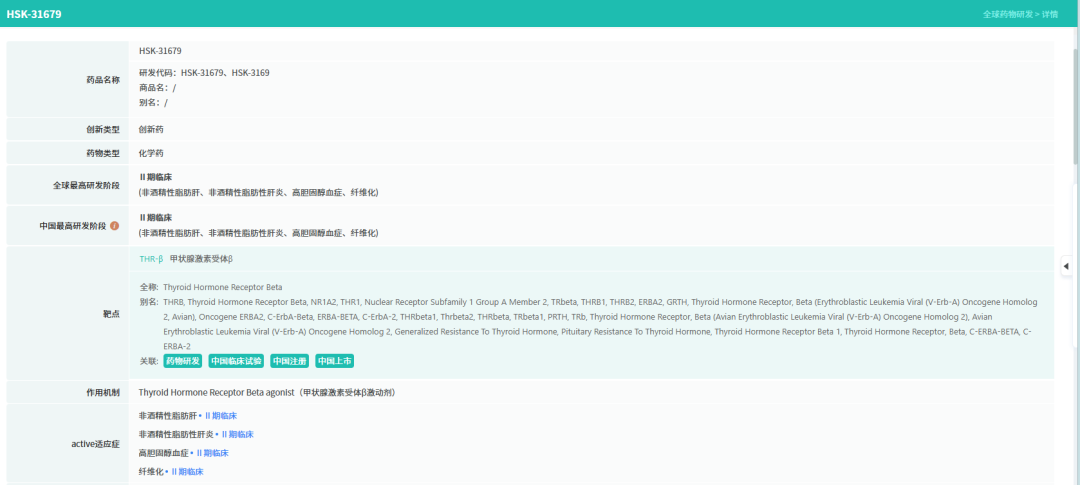
另一款入选药物HSK31679则是国内首个获得突破性治疗认定的甲状腺激素β受体(THR-β)激动剂。甲状腺激素β受体在肝脏中高表达,调控脂代谢相关的多个关键基因。HSK31679通过高选择性激活该受体,调节胆固醇和脂肪酸代谢,从而降低肝脏脂肪含量、改善炎症和纤维化。此次认定基于其在国内MASH患者中完成的II期临床积极数据:连续治疗52周后,患者在肝脏脂肪减少、炎症改善等组织病理学终点上表现优异,且安全性良好。若顺利获批,HSK31679将成为我国首个MASH治疗药物,填补该领域的临床空白。
02
MASH百亿市场,海思科加速布局
根据Frost & Sullivan预测,2030年中国及全球的MASH患病人数将分别达到0.56亿人和4.9亿人。庞大的患者基数催生了巨大的药物市场,2030年中国及全球的MASLD/MASH药物市场规模将分别达到355亿人民币和322亿美元。在中国,随着生活方式的改变,MASH患者群体已超数千万,但长期以来缺乏针对性的治疗药物,临床需求极度迫切。
目前,全球MASH赛道竞争日趋白热化,除THR-β激动剂外,FXR激动剂、GLP-1受体激动剂等靶点也在同步推进。然而,截至目前,国内尚无一款针对MASH病因治疗的创新药获批上市。海思科HSK31679作为国内首个纳入突破性疗法的THR-β激动剂,有望在后续审评中获得优先通道,加速上市进程,为数以千万计的MASH患者带来新的治疗希望。
03
厚积薄发,海思科创新转型步入收获期
此次两款重磅新药接连获得监管认可,不仅是海思科研发实力的集中体现,也标志着其创新转型正式步入收获期。据摩熵医药数据库统计,截至目前,海思科已有超30款1类新药获批临床,累计有4款1类新药成功上市,且均为化学药。
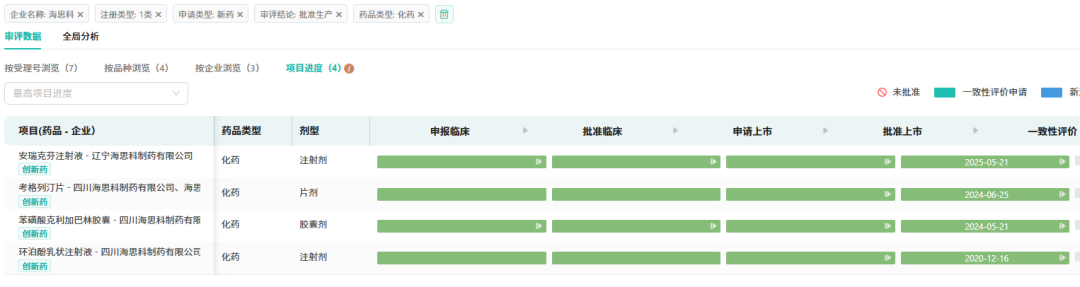
在其丰富的管线储备中,除了上述两款药物外,HSK39297片已于2026年1月首次提交上市申请,这是一款高效的选择性补体B因子(FB)抑制剂;而HSK31858片作为口服强效高选择性DPP1抑制剂,也已在2024年启动了III期临床。
从“仿创结合”到“自主创新”,海思科正以其扎实的研发积累和精准的战略眼光,在国产创新药的黄金时代加速前行。随着这些潜在“重磅炸弹”的陆续推进,海思科在国内外医药市场的影响力与竞争力,有望迈上一个全新的台阶。
END
本文为原创文章,转载请留言获取授权
近期更多摩熵咨询热门报告
识别下方二维码领取

联系我们,体验摩熵医药更多专业服务 | ||||
会议 合作 | 报告 定制 | 数据库 咨询 | 数据 定制 | 媒体 合作 |