【周末杂谈】先进技术并未改进审批的质和量
值得关注AI应用效果的人参考的、深知审批关键环节和企业实际需求的评论
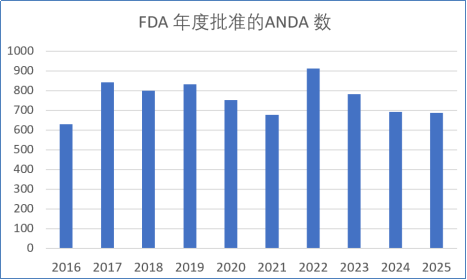
无论是专业技术性应用,如基于问题的审评(QbR)、质量源于设计(QbD)、知识辅助评估和结构化申请(KASA),还是信息技术(IT)和知识工程(KE)应用,如eCTD、机器学习、大语言模型(后两者可用时髦的词AI来统称),道理上都应有助于企业提高申报的质量及FDA提高审评的效率。但结果似乎并非如此,如下图显示。新冠疫情已过去四年多,大模型横空出世也已过去三年半了。新技术的应用固然可喜,但若不能影响审批结果,就只剩下劳民伤财了。
导致事与愿违的原因很多,其中之一是缺乏技术人员与审评人员间的交流合作,及对于对方领域的认知。技术人员容易高估技术的作用,低估深入了解审评工作的重要性。审评人员,受媒体热捧和冷嘲、及自身缺乏对技术的深入了解,难以客观地判断技术的影响,导致有些人或过多地依赖于技术人员,或过于轻视新技术。
到头来,技术应服务于审评。技术人员理应更加深入了解审评工作、认知影响效率的瓶颈环节:那些对提高ANDA批准数有直接影响的环节,而不是仅让管理变得形式上更系统化和现代化。
这就需要对审评业务有深刻认知的人来指点。最近,一位这样的人(Bob Pollock)在其博客上发表了一些评论。文章的主题虽不是技术和AI应用,但对那些关注如何做好AI应用的人,也许会有借鉴作用。现将其评论摘录和翻译如下。
我们仍然会看到多轮完全回应函(CRL)、中期回应函(IR)和学科审评函(DRL),其中提出了之前几轮审评中未涉及的新问题。这令业界感到沮丧,也凸显了ANDA“首次完整审评”(first-time complete review)的概念并非如人们所吹捧的那样完美。诚然,企业对CRL的回复可能会引发需要进一步澄清或回应的情况,但在第二轮或第三轮审评中突然出现的新缺陷问题必须得到解决,因为这些问题持续阻碍着监管机构在前两轮审评中批准仿制药的能力。除非“完整审评”真正做到完整审评,否则我认为一轮或二轮审评的批准数量短期内不会增加。
ANDA 审评由团队中多位审评员合作完成。由于审评人员众多且背景各异,企业会收到来自不同审评人员的不同问题。因此,即使企业认真地对之前收到的缺陷进行分类,并在新的申请中加以解决,他们仍然可能会收到不同的问题,尤其是在新审评人员接手他们的申请时。这并非一个新问题,而且在《仿制药法》实施31年后,似乎仍然没有简单的解决办法。
发函给企业前需经主管审核。表面上看,提出的缺陷可能合理(如拟议的CRL、IR或DRL中所述),但主管并非总有时间回溯到 ANDA 原始文件中查看导致缺陷的细节,因此,该信函可能在主管未能充分审查缺陷的情况下就发给企业。有些情况下,缺陷本身就不合理,或者审评人员漏看了申请中已有的相关信息。
人们可能认为随着AI技术的进步,及政府大力宣传其在加快药品审批方面的应用,标准的eCTD格式应能带来更便捷、更全面、更高效的审评。但我认为,目前的审评流程以与AI的融入程度还不够。我想有时候我需要发泄一下,而今天正好是个可以让我释放压力的日子。如果你在审评中也遇到过同样的问题,或者我只是像AI那样有时会产生幻觉,请告诉我!
识林®版权所有,未经许可不得转载

【关于识林-常见问题与解答】

