CDE上线“注册服务平台”,提供药品申报“全导航”!

3月30日,CDE宣布上线注册服务平台,可全链条展现药品注册申报流程,包含注册申请前的提前介入,临床试验申请、临床试验期间变更、上市许可申请的全程指导,上市后变更申请以及再注册申请的精准导航等。如下:


一、注册指导,全程导航
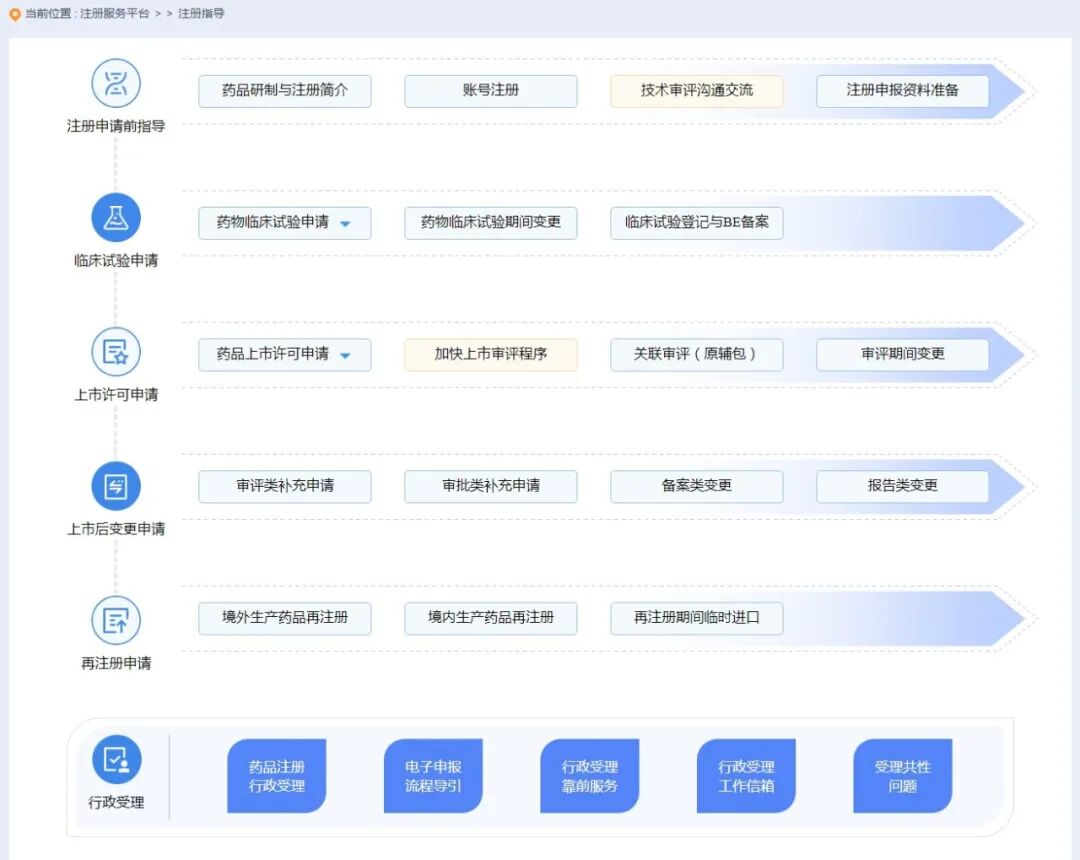
为全链条展现药品注册申报流程,增设“注册指导”栏目,包含注册申请前的提前介入,临床试验申请、临床试验期间变更、上市许可申请的全程指导,上市后变更申请以及再注册申请的精准导航。
“注册申请前指导”子栏目,展示“药品研制与注册简介”、“账号注册”、“技术审评沟通交流”、“注册申报资料准备”等注册申请前的准备环节,为充分研究、合理申报提供指导。
“临床试验申请”、“上市许可申请”、“上市后变更申请”、“再注册申请”子栏目,对药品上市前、后各注册申请涉及到的主要环节,如行政受理、加快上市、核查检验、补充资料、异议解决、行政审批及证书领取等,逐一展示相关要求、具体流程以及政策依据,为注册申报中的关键节点提供导航。
“行政受理”子栏目,介绍行政受理环节办事须知、电子申报流程、靠前服务、共性问题等内容;并设置“行政受理工作信箱”,充分听取和收集业界对优化受理工作、服务提升、培训需求等意见与建议,以便持续优化受理服务工作。
二、公众服务,合理引导
为响应公众需求,引导社会公众更好地了解药品审评工作,增设“公众服务”栏目,包含“药品注册简介”——介绍中药、化学药品、生物制品注册分类,以及药学、药理毒理和药物临床试验相关研究内容;“药品批准信息”——汇总国家药监局公开的药品批准信息、创新药品名录,以及中心网页公开的上市药品信息,方便公众查阅。
“注册服务平台”上线后将保持动态更新,持续优化。如在使用过程中遇到问题或有改进建议,可通过“行政受理工作信箱”提出。
国家药品监督管理局药品审评中心
2026年3月30日

【点这里,进入医药数据库,搜索下载原文】

药学检测服务推荐
一、化药检测服务
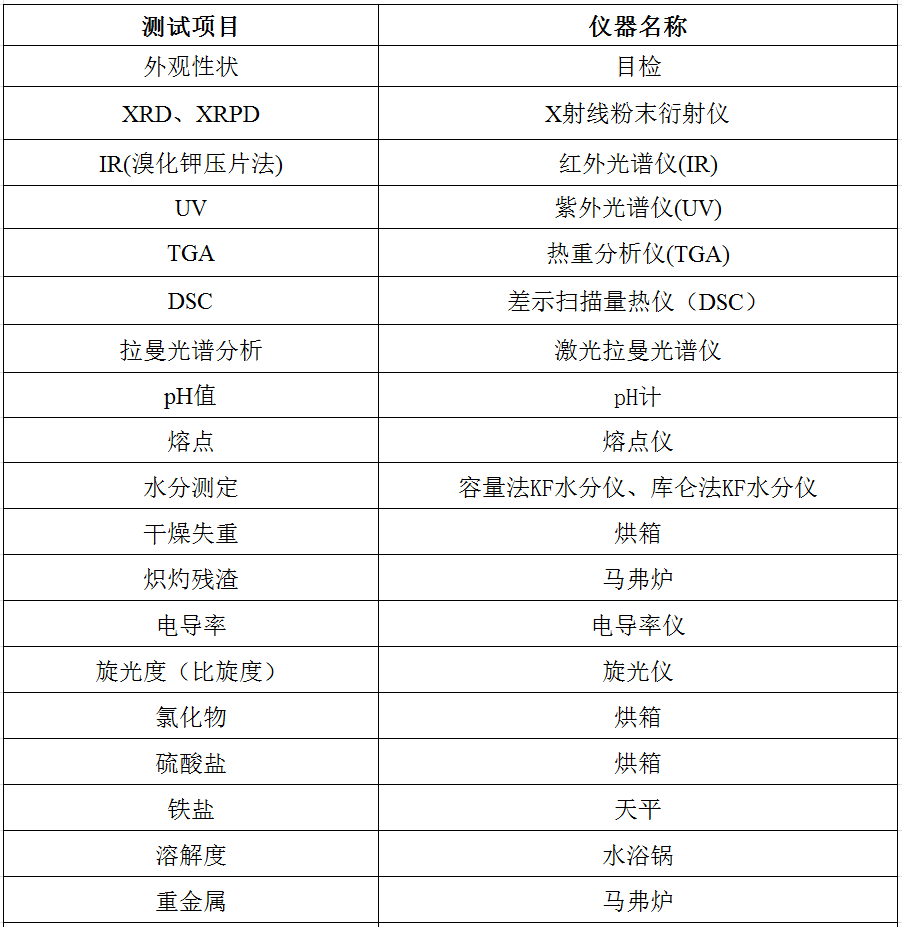



二、化药质量研究服务
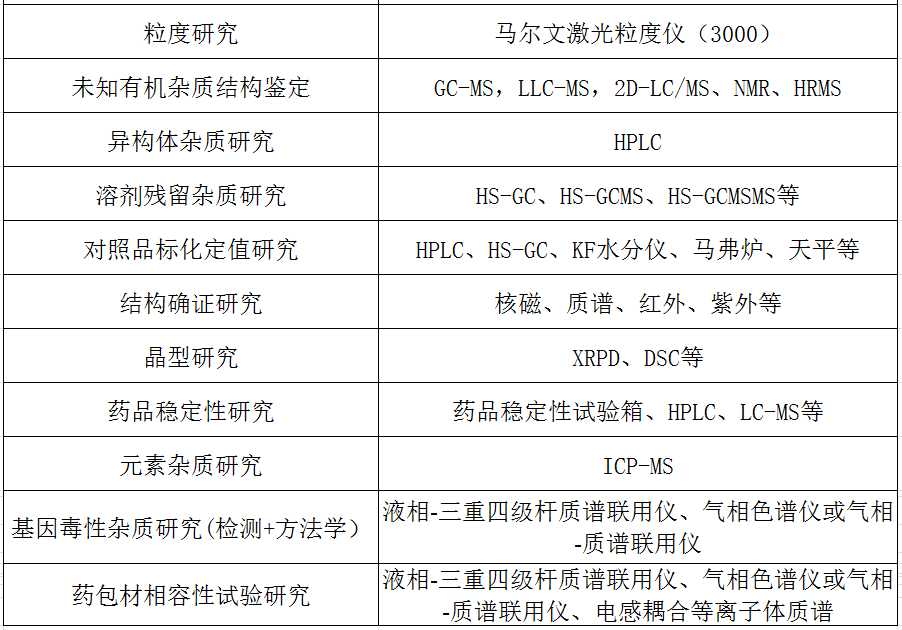

三、生物药检测服务

四、生物药质量研究服务
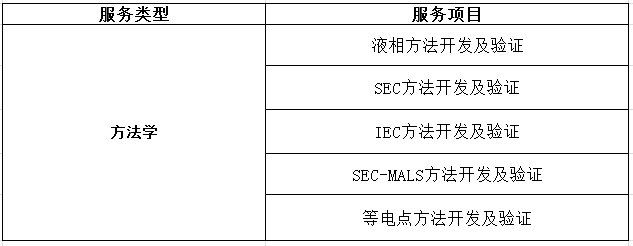
五、药品毒理安全性评价服务

六、药品包装材料理化检测
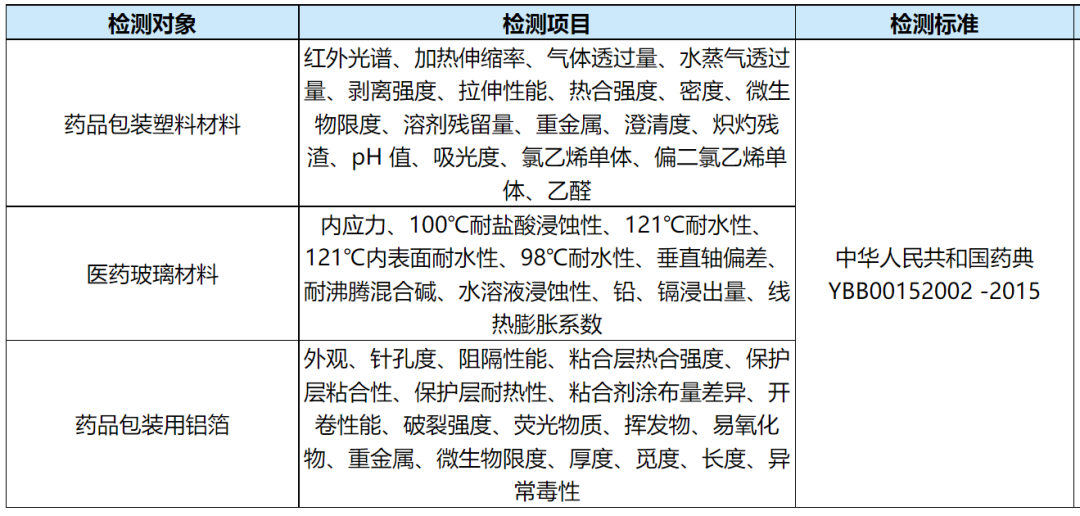
实验室资质:CMA、CNAS
实验室所在地:上海、苏州、青岛、广州、福州
联系我们:151-9002-7486/181-0068-0718(微信同号)


本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的单位、媒体或个人可与我们联系(274190388@qq.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。


