JAMA | 肿瘤减灭术联合化疗未改善多器官转移性结直肠癌患者生存——ORCHESTRA随机临床试验结果公布


结直肠癌是全球常见恶性肿瘤之一,约50%的患者在病程中发生远处转移。对于转移局限于肝脏或肺部的寡转移患者,局部根治性治疗已证实可带来生存获益。然而,临床实践中大量患者存在多器官转移(累及两个及以上器官),对于这类患者,局部治疗的价值尚不明确。
既往回顾性研究提示,肿瘤减灭术可能改善部分广泛转移患者的预后,但缺乏支持其生存获益的前瞻性随机对照试验证据。3月16日,JAMA在线发表了ORCHESTRA随机临床试验结果,该研究旨在明确在姑息性化疗基础上联合肿瘤减灭术能否改善多器官mCRC患者的总生存期。
研究背景
该研究为研究者发起的开放标签、多中心随机对照试验,在荷兰27家医院和英国1家医院开展,纳入时间为2013年5月至2023年5月,末次随访日期为2024年4月4日。入组标准为成年多器官转移性结直肠癌患者,经多学科团队评估认为可实现超过80%的肿瘤减灭(通过手术、放疗和/或热消融),并计划接受一线姑息性化疗。所有患者在随机分组前首先接受3个周期CAPOX(卡培他滨+奥沙利铂)或4个周期FOLFOX(5-氟尿嘧啶+奥沙利铂)±贝伐珠单抗的诱导化疗,仅在获得客观缓解或疾病稳定后,才被1:1随机分配至单纯化疗组(继续接受姑息性全身治疗)或减灭联合化疗组(先接受肿瘤减灭术,之后继续完成剩余周期化疗)。研究的主要终点为总生存期,次要终点包括无进展生存期和严重不良事件。
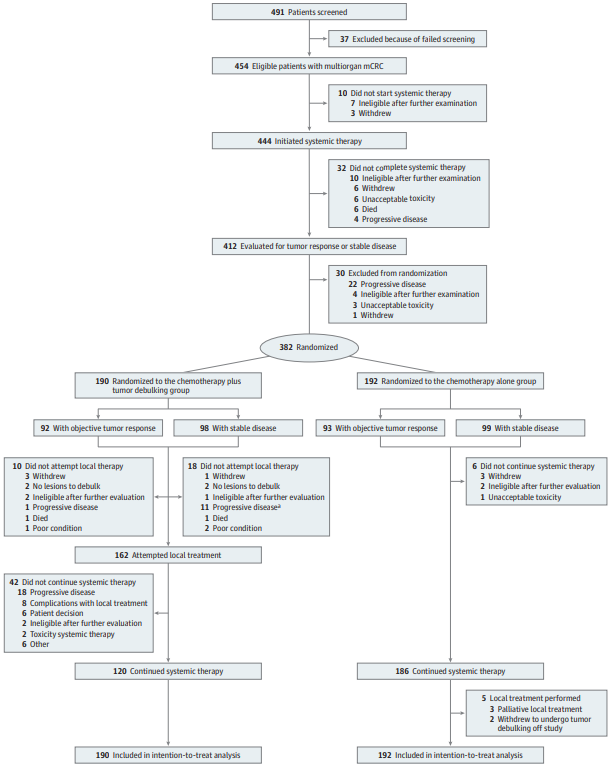
研究设计与方法
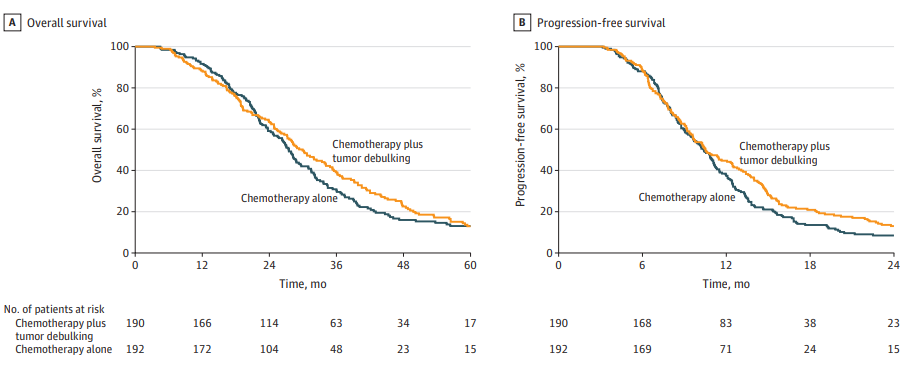
研究假设化疗组中位总生存期为18个月、减灭联合化疗组为24个月,共需随机化382例患者,检验效能80%,双侧α=0.05。共454例患者入组,其中72例在随机化前脱落(主要原因为疾病进展或独立多学科团队评估认为减灭不可行),最终382例患者被随机分组。化疗组192例(男性占69%,中位年龄64岁),减灭联合化疗组190例(男性占67%,中位年龄64岁)。两组基线特征和转移模式基本均衡(原文表1):肝转移占比约80%(化疗组80.2%,减灭联合化疗组80.0%),伴腹膜转移者约32%(化疗组33%,减灭联合化疗组32%),BRAF V600E突变率均为7%,RAS突变率分别为51%(化疗组)和41%(减灭联合化疗组),微卫星稳定者均占82%。随机化时,两组均有48%的患者达到部分或完全缓解,52%为疾病稳定。中位随访32.3个月,共发生308例总生存期事件(化疗组153例,减灭联合化疗组155例)。主要终点结果显示,化疗组中位总生存期为27.5个月(四分位区间19.5-39.2),减灭联合化疗组为30.0个月(四分位区间18.1-47.6),校正后风险比为0.88(95%置信区间0.70-1.10),P=0.26,无统计学显著差异。次要终点方面,化疗组中位无进展生存期为10.4个月(四分位区间7.4-13.6),减灭联合化疗组为10.5个月(四分位区间7.3-15.7),校正后风险比为0.83(95%置信区间0.67-1.02),P=0.08,亦无显著差异。安全性分析显示(原文表2),减灭联合化疗组严重不良事件(≥2级)发生率显著高于化疗组:分别为101例(53%)和74例(39%),风险差为14.62%(95%置信区间4.21%-25.03%),P=0.006。其中,减灭联合化疗组有8例发生5级(死亡)严重不良事件(4%),而化疗组为0例;4级事件减灭联合化疗组14例(7%),化疗组10例(5%)。治疗相关性分析显示,减灭联合化疗组中与局部治疗相关的严重不良事件共52例(27%),其中4级6例(3%)、5级4例(2%)。提示在化疗基础上增加局部治疗显著增加了治疗相关毒性。
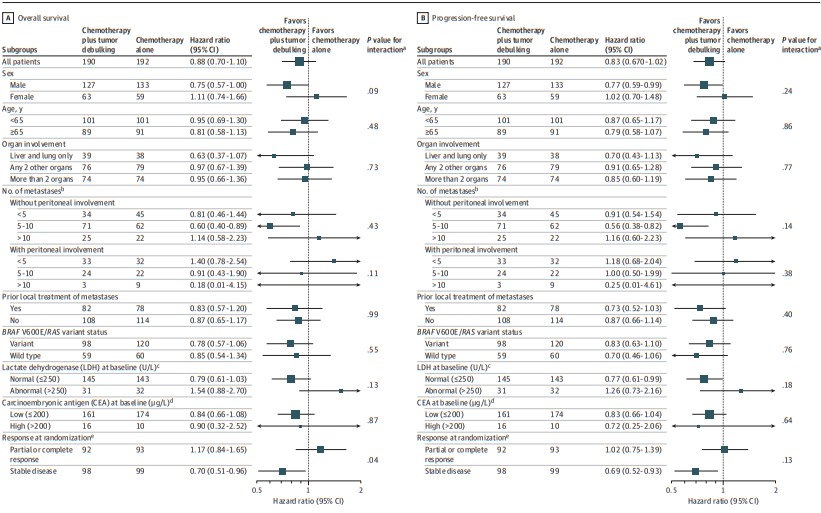
对数坐标轴上的总体生存率和无进展生存率森林图
结论与临床启示
本研究的主要结论是,在多器官转移性结直肠癌患者中,一线姑息性化疗基础上联合肿瘤减灭术(目标减灭≥80%)未能改善总生存期,且显著增加了严重不良事件发生率,因此该策略不应作为标准治疗方案。
与既往研究比较,三项随机试验(CAIRO4、iPACS、韩国研究)均显示无症状同步不可切除转移患者行原发灶切除无生存获益;而TransMet研究显示严格筛选的不可切除肝局限性转移患者接受肝移植联合化疗可改善5年总生存率(56.6% vs 12.6%),但入组标准极其严格(排除BRAF V600E突变和肝外转移)。研究存在一定局限性:入组周期长达10年,化疗方案主要为FOLFOX/CAPOX±贝伐珠单抗,未采用三药联合方案(FOLFOXIRI)或抗EGFR治疗(针对左半RAS/BRAF野生型),但研究者认为即便新型方案可能提高总生存,减灭术的相对获益比例不太可能改变;80%减灭阈值基于影像学检出极限和卵巢癌证据,缺乏直接验证;化疗组有8例交叉接受局部治疗,减灭联合化疗组28例未实际接受减灭;缺乏一线进展后的后续全身治疗数据。对于临床实践而言,该研究以高质量的随机对照证据表明,不应在广泛转移患者中常规推荐减灭性局部治疗,而应继续以全身治疗为基石。对于局限性寡转移患者,局部治疗的价值仍需等待ERASur、SABR-COMET-3/10等前瞻性试验结果。该研究为临床决策提供了重要的循证依据,避免不必要的手术风险和资源浪费。
参考文献:
Gooijes EC, Bakkerus L, Adhin AA, et al. Tumor debulking in combination with chemotherapy in multiorgan metastatic colorectal cancer: the ORCHESTRA randomized clinical trial. JAMA.