十年磨一剑:中国创新药如何以“质量”撬动全球格局?


2015年7月22日,一场以“质量”为核心的监管改革席卷中国制药界。十年后,中国从“仿制药大国”转向全球创新药的重要参与者,并在部分前沿领域展现出领跑态势。这背后究竟发生了什么?
近日,SCIENCE CHINA Life Sciences(《中国科学:生命科学》英文版)在线发表了中国医学科学院肿瘤医院李宁教授与黄慧瑶副教授牵头撰写的题为“Decade of quality-driven accelerated development of innovative drugs in China and its implications worldwide”文章。文章系统回顾了中国创新药在过去十年间从质量变革到生态重塑的跨越式发展,并探讨了这一“中国范式”对全球的启示意义。


十年变迁:一场质量驱动的生态演进
十年前,中国制药业一度面临临床数据规范性方面的挑战。近年来,随着数据质量与合规体系的持续提升,中国已成为全球创新药研发中不可忽视的力量。以临床质量为支点,中国创新药沿着研发、审评、支付、应用的全链条,重构了整个创新药生态系统。文章通过13个关键维度的量化对比,直观呈现了这一巨变。
在研发端,近年中国first-in-class药物从9个增至120个,me-too药物占比从50%降至35%。细胞治疗、抗体偶联药物等前沿领域,中国已成为全球重要力量。在审评端,新药上市时间缩短75%,中美上市时间差从8年缩至不足2年。在支付端,创新药的可及性大幅提高,上市两年内进入国家医保目录的比例从3%跃升至90%。在国际认可方面,15款药物被纳入2023年NCCN指南,特瑞普利单抗获FDA批准上市,为美国医疗系统节省超过1.7亿美元。

质量体系:从规范提升到系统协同
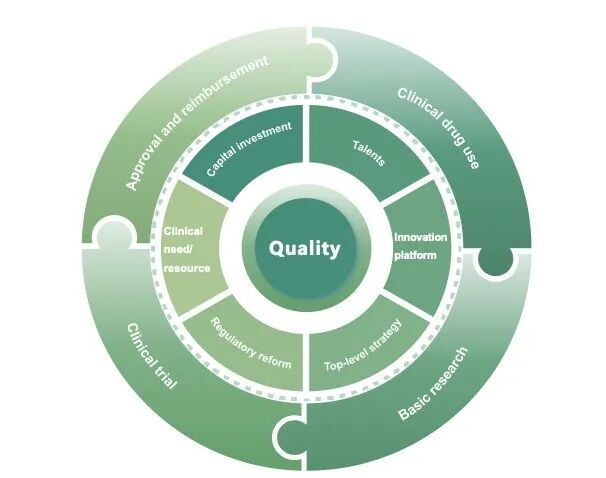
上述变化的起点,是十年前以高标准推动的行业规范化进程。“质量”逐步从合规要求演变为研发与评价的核心导向,临床价值导向的研发理念逐步确立。此后十年,中国围绕“质量”这一核心,逐步构建起覆盖创新药全生命周期的协同体系。从基础研究、临床试验、审评审批,到医保支付、临床使用,七大关键要素相互支撑、协同发力。质量既是这一生态的起点,也是贯穿始终的主线。
在这一生态的驱动下,政策体系不断完善。罕见病药物7年市场独占期、创新药IND 30天默示许可等政策相继落地。审评标准持续提升,2016年至2023年间,FDA对中国临床试验的检查中“无行动指示”比例从48%提升至85%。与此同时,资本与人才形成正反馈,海外人才加速回流,技术转移与高质量创新形成良性循环。值得关注的是,中国正逐步从全球数据的重要贡献者,转向国际规则的积极参与者。2023年,国家药监局加入ICH E6(R3)工作组,参与制定全球临床试验标准;2024年,牵头制定《传统医学国际多中心临床试验指南》。这些进展标志着中国在全球创新药治理中正扮演越来越重要的角色。

未来十年:挑战与机遇并存
站在新十年的起点,文章也指出了中国创新药面临的挑战与方向。在制度层面,专利保护、全球同步申报、高值药物支付路径有待进一步优化。在技术领域,中国在CAR-T、ADC、双抗等方向已形成集群优势,AI制药也有望加速新药发现。与此同时,质量不可松懈——在推动去中心化试验、AI辅助研发的过程中,必须确保数据质量与监管合规。在全球协同方面,依托“一带一路”推动药品审评互认,将有助于扩大中国创新药的全球可及性与规则制定权。
文章最后指出,中国创新药十年发展,证明了一条可行路径:以质量为核心,系统识别并打通产业链瓶颈,最终实现生态系统的整体跃迁。中国发展路径的探索经验和范式,或将为其他新兴经济体提供借鉴。
[点击下方链接或阅读原文]▼
https://doi.org/10.1007/s11427-025-3245-8


