2026年3月新药III期成功深度盘点:五大品种背后的行业分野
发布时间:2026-03-30来源:药事纵横
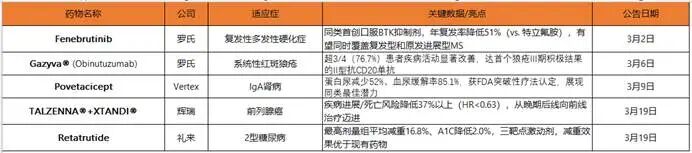
近期,全球生物医药领域迎来III期临床收获的集中爆发期,罗氏、辉瑞、礼来、Vertex四家巨头及标杆企业接连公布五项关键品种的III期阳性结果,覆盖神经、免疫、肿瘤、代谢、肾病五大治疗领域。这些突破并非孤立的研发胜利,更折射出当前全球新药研发的深层逻辑变迁——从“跟随式改良”向“机制性创新”转型,从“单一靶点攻坚”向“多维度协同”升级,不同赛道、不同企业的布局策略差异,正清晰勾勒出生物医药行业的竞争分野与未来走向。一、罗氏双响炮:神经与免疫领域的“破局者”
2026年3月,罗氏以两项重磅III期成功拉开全球新药收获季的序幕,两款药物分别剑指多发性硬化症(MS)与系统性红斑狼疮(SLE)两大“研发荒漠”领域,凭借机制层面的突破性创新,打破了长期以来的治疗困局,彰显了全球药企龙头在难治性疾病领域的研发硬实力。这两项突破的核心价值,不在于“疗效提升”的简单叠加,而在于从治疗机制上重新定义了对应疾病的治疗范式,为同类药物研发提供了全新的思路指引。3月2日,罗氏公布口服BTK抑制剂Fenebrutinib治疗复发性多发性硬化症的III期阳性结果,该药物成为全球首个在III期临床试验中被证明确实有效的口服BTK抑制剂,其核心亮点不仅在于显著的疗效数据,更在于独特的分子结构设计带来的中枢穿透能力。临床数据显示,Fenebrutinib可使复发性MS患者的年复发率降低51%,显著优于现有标准治疗药物特立氟胺,更值得关注的是,该药物能够穿透血脑屏障,直接靶向中枢神经系统的慢性炎症,这一特性彻底打破了传统MS治疗“仅能调节外周免疫、无法干预中枢病变”的局限。从机制层面来看,Fenebrutinib的突破源于对BTK靶点作用的深度挖掘与分子结构的精准优化。BTK作为B细胞受体信号通路的关键激酶,不仅参与外周免疫细胞的活化,更在中枢神经系统的小胶质细胞活化中发挥重要作用——MS的核心病理机制是中枢神经系统脱髓鞘病变,而小胶质细胞的异常活化是导致慢性炎症与脱髓鞘的关键诱因。传统BTK抑制剂因脂溶性不足,难以穿透血脑屏障,仅能抑制外周B细胞活性,无法触及中枢病变核心;而Fenebrutinib通过分子结构修饰,提升了脂溶性与血脑屏障穿透效率,可同时抑制外周B细胞与中枢小胶质细胞的活化,实现“外周免疫调节+中枢炎症干预”的双重作用,为MS治疗提供了全新的解决方案。更为重要的是,Fenebrutinib有望实现MS治疗的全覆盖,其临床数据显示,该药物不仅对复发性MS疗效显著,对原发进展型MS也展现出潜在的治疗价值,若能顺利获批,将成为首个同时覆盖复发型与原发进展型MS的口服BTK抑制剂,彻底改变当前MS治疗“分类型给药”的现状,推动MS治疗从“控制急性发作”向“兼顾急性发作与长期残疾进展”的全周期管理转型。仅时隔4天,3月6日罗氏再次公布Gazyva®(Obinutuzumab)治疗系统性红斑狼疮的III期ALLEGORY研究阳性结果。临床数据显示,Gazyva联合标准疗法治疗SLE,可使76.7%的患者疾病活动显著改善,同时将患者中位首次发作时间延长至52周以上,与安慰剂组相比,疾病复发风险降低42%,这一数据远超同类药物的临床表现,完整兑现了II型抗CD20单抗在SLE治疗中的临床价值。SLE作为一种异质性极高的自身免疫性疾病,其研发难度堪称“自身免疫领域的珠峰”,此前多款抗CD20单抗、免疫抑制剂在III期临床试验中折戟,核心原因在于未能精准靶向SLE的关键病理环节。Gazyva的成功,源于其作为II型抗CD20单抗的独特优势——与I型抗CD20单抗相比,Gazyva对CD20抗原的亲和力更高,能够更高效地诱导B细胞凋亡,同时可激活补体依赖的细胞毒性(CDC)与抗体依赖的细胞毒性(ADCC),双重机制清除异常活化的B细胞,从源头抑制自身抗体的产生,从而缓解SLE的全身多系统损伤。罗氏这两项III期成功的共性的的是,均避开了“me-better”的同质化竞争,选择从机制层面实现突破——Fenebrutinib聚焦MS的中枢病变核心,Gazyva精准靶向SLE的关键病理环节,这种“机制先行”的研发策略,正是当前生物医药领域“创新深水区”的核心竞争力所在,也彰显了龙头药企在难治性疾病领域的研发远见与技术积累。二、肿瘤与代谢的“前线化”与“多靶点化”
3月19日,辉瑞与礼来同时公布两项关键品种的III期阳性结果,分别聚焦前列腺癌与2型糖尿病两大领域,这两项突破虽分属不同赛道,却共同印证了当前新药研发的两大核心趋势——肿瘤治疗的“前线化”延伸与代谢疾病治疗的“多靶点化”协同,为两大领域的临床治疗带来了革命性的变化,也揭示了大型药企在成熟赛道的创新升级路径。辉瑞公布的TALZENNA®(talazoparib)联合XTANDI®(enzalutamide)治疗HRR基因突变的转移性去势敏感性前列腺癌(mCSPC)的III期TALAPRO-3研究结果,标志着前列腺癌治疗正式进入“前线联合治疗”的新时代。临床数据显示,与安慰剂联合XTANDI相比,TALZENNA联合XTANDI可使患者的疾病进展或死亡风险降低37%以上,风险比(HR)远低于预设的0.63目标,大多数患者在中期分析时仍保持无进展状态,同时在总生存期、客观缓解率、前列腺特异性抗原(PSA)反应等次要终点上均展现出显著获益。从治疗格局来看,这一突破的核心价值在于实现了前列腺癌治疗的“前线化”延伸。此前,TALZENNA联合XTANDI已获批用于转移性去势抵抗性前列腺癌(mCRPC)的后线治疗,而本次III期研究的成功,将这一“黄金组合”的应用场景拓展至更早阶段的mCSPC,意味着HRR基因突变的前列腺癌患者可在疾病更早期就获得高效的联合治疗,从而锁定长期获益,延缓疾病进展为mCRPC的时间。机制层面,这一联合方案的协同效应源于“PARP抑制+雄激素受体通路抑制”的双重作用。TALZENNA作为一种口服PARP抑制剂,可阻断PARP酶活性并将PARP困在DNA损伤部位,导致癌细胞生长停滞与死亡,尤其对HRR基因突变的肿瘤细胞具有显著的杀伤作用;而XTANDI作为雄激素受体通路抑制剂,可抑制雄激素受体的活化,阻断前列腺癌细胞的生长信号。两者联合使用,可从“DNA损伤修复”与“细胞生长信号”两个维度双重打击肿瘤细胞,实现“1+1>2”的治疗效果,且在临床研究中,该联合方案的安全性与单药治疗一致,未出现新的安全信号,为其临床应用提供了保障。该研究共招募了599名来自全球多个地区的mCSPC患者,覆盖BRCA与非BRCA HRR基因突变人群,结果显示,无论患者携带何种HRR基因突变,均能从该联合方案中获得一致的疗效获益,这表明该方案具有广泛的适用性,有望成为HRR基因突变mCSPC的标准治疗方案,改变当前前列腺癌的临床治疗实践。与辉瑞的“前线化”突破不同,礼来公布的Retatrutide治疗2型糖尿病的III期TRANSCEND-T2D-1研究结果,彰显了代谢疾病治疗“多靶点化”协同的强大潜力。作为全球首个进入III期的GIP/GLP-1/胰高血糖素三受体激动剂,Retatrutide在2型糖尿病患者中展现出前所未有的降糖与减重双重疗效,成为代谢疾病领域的“标杆性”突破。临床数据显示,在为期40周的III期试验中,Retatrutide各剂量组均达到主要终点与所有关键次要终点,其中12mg最高剂量组的表现最为亮眼:平均糖化血红蛋白(A1C)降低2.0%,平均体重减轻16.8%(相当于36.6 lbs),且体重减轻趋势未达平台期,患者在整个治疗期间持续减重;4mg、9mg剂量组也分别实现了11.5%、15.5%的体重减轻,显著优于安慰剂组的2.5%。此外,Retatrutide还能显著改善2型糖尿病患者的关键心血管风险因素,包括非HDL胆固醇、甘油三酯与收缩压的降低,为患者带来额外的心血管保护获益。Retatrutide的突破源于其独特的三靶点协同机制。传统的GLP-1受体激动剂仅能靶向GLP-1受体,主要聚焦于降糖与轻度减重;而Retatrutide同时靶向GIP、GLP-1与胰高血糖素三个激素受体,三者协同作用,实现了疗效的全面升级:GLP-1受体激动剂可延缓胃排空、抑制食欲、促进胰岛素分泌;GIP受体激动剂可增强GLP-1的降糖效果,同时改善胰岛素敏感性;胰高血糖素受体激动剂则可促进脂肪分解、增加能量消耗,三者协同作用,既实现了强效降糖,又达成了显著减重,同时兼顾心血管保护,完美解决了2型糖尿病患者“降糖与减重难以兼顾”的临床痛点。安全性方面,Retatrutide的不良事件类型与其他基于肠促胰素的治疗药物一致,最常见的不良事件为恶心、腹泻、呕吐,主要发生在剂量递增期间,且多为轻度至中度,随着治疗进展可逐渐缓解;12mg最高剂量组的停药率为5.1%,整体耐受性良好。此外,礼来还在多项III期临床试验中探索Retatrutide在肥胖、膝骨关节炎、阻塞性睡眠呼吸暂停等代谢相关疾病中的应用,其中针对肥胖伴膝骨关节炎的III期试验已取得阳性结果,显示其体重减轻幅度高达28.7%,同时显著缓解关节疼痛,彰显了其在代谢领域的广泛应用潜力。辉瑞与礼来的两项突破,清晰展现了当前生物医药领域的两大创新趋势:肿瘤治疗领域,“后线有效向前线拓展”成为提升患者长期获益的重要路径,通过在疾病更早期应用高效联合方案,可显著延缓疾病进展,改善患者预后;代谢疾病领域,“多靶点协同”成为突破疗效天花板的核心方向,通过同时靶向多个与疾病相关的靶点,可实现多维度的临床获益,满足患者的综合治疗需求。这两大趋势,也将成为未来肿瘤与代谢领域新药研发的核心导向。三、肾病赛道的“同类最佳”突围
在罗氏、辉瑞、礼来等巨头聚焦主流赛道的同时,Vertex凭借Povetacicept在IgA肾病领域的III期阳性结果,走出了一条“细分赛道差异化突围”的道路,其核心策略是在小众但未被满足需求较高的细分领域,通过机制差异化与数据优势确立“同类最佳”地位,这也为中型药企的创新突围提供了极具参考价值的范本。3月9日,Vertex公布Povetacicept治疗IgA肾病的III期RAINIER试验中期分析结果,亮眼的数据不仅彰显了其临床价值,更直接支撑其获得美国FDA的突破性疗法认定,成为IgA肾病领域的“潜力黑马”。IgA肾病是全球最常见的原发性肾小球疾病,也是导致终末期肾衰竭的主要原因之一,其核心病理机制是IgA免疫复合物在肾小球系膜区沉积,引发系膜细胞增殖、炎症反应与肾小球损伤,最终导致肾功能进行性下降。长期以来,IgA肾病的治疗手段极为有限,主要依赖激素、免疫抑制剂等非特异性治疗,疗效有限且不良反应较多,无法有效延缓疾病进展,临床需求长期未被满足。Povetacicept的III期数据展现出“同类最佳”的显著优势:与安慰剂组相比,Povetacicept治疗组的蛋白尿显著减少52%,而安慰剂组仅减少4.3%;同时,85.1%的患者血尿症状完全缓解,远超现有疗法的缓解率。此外,Povetacicept采用每月一次的给药方式,相较于现有每日给药的治疗方案,极大提升了患者的用药依从性,这一优势在慢性疾病的长期管理中尤为重要。从机制层面来看,Povetacicept的差异化优势源于其精准的靶点选择与独特的作用机制。该药物靶向B细胞活化因子(BAFF)与增殖诱导配体(APRIL),这两种细胞因子是IgA免疫复合物生成与沉积的关键驱动因素——BAFF可促进B细胞活化与增殖,诱导IgA抗体的产生;APRIL则可增强IgA抗体的聚合与沉积,加重肾小球损伤。Povetacicept通过同时抑制BAFF与APRIL的活性,从源头阻断IgA免疫复合物的生成与沉积,从而延缓肾小球损伤,保护肾功能,这种机制针对性地解决了IgA肾病的核心病理问题,与现有非特异性治疗形成了显著差异。FDA突破性疗法认定的授予,进一步印证了Povetacicept的临床价值与创新性——该认定主要授予用于治疗严重或危及生命疾病、且在疗效或安全性方面显著优于现有疗法的药物,Povetacicept凭借远超现有疗法的疗效数据,成为IgA肾病领域首个获得该认定的药物,也为其后续的上市申报提供了加速通道。Povetacicept的成功,为中型药企的创新突围提供了清晰的路径:在巨头扎堆的主流赛道之外,聚焦小众细分赛道的未被满足需求,通过精准的机制创新与扎实的临床数据,确立“同类最佳”地位,从而在竞争中占据优势。相较于巨头在主流赛道的大规模投入,中型药企在细分赛道的研发投入更具针对性,能够快速聚焦核心需求,通过机制差异化构建竞争壁垒,这种“小而精”的研发策略,正在成为中型药企实现弯道超车的重要路径。2026年3月的五项III期成功品种,不仅为五大治疗领域的患者带来了全新的治疗选择,更折射出全球生物医药行业的深刻变革。罗氏的“机制破局”、辉瑞与礼来的“趋势引领”、Vertex的“细分突围”,三种不同的研发路径,对应着不同企业的战略定位与竞争优势,也构成了当前生物医药行业的多元竞争格局。
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。