AZ明星药适应症+1,成人不再“蹭”儿药


3月30日,阿斯利康宣布其MEK抑制剂司美替尼(科赛优®)获NMPA批准拓展适应症,将适用人群由既往的儿童患者延伸至3岁及以上儿童及成人患者。至此,科赛优®成为国内首个且唯一覆盖全年龄段(3岁及以上)伴有症状、无法手术的丛状神经纤维瘤(PN)的1型神经纤维瘤病(NF1)治疗药物。
新适应症获批,一场跨越年龄的治疗“接力赛”
根据Pharma ONE数据库显示,司美替尼于2023年4月在中国获批用于儿童患者,填补了该领域“无药可医”的空白。然而,在实际临床中,NF1是一种进展性、终身性疾病,约50%的患者伴发PN,且肿瘤可能在成年后持续生长,体积增大,引发疼痛、畸形、功能障碍等残疾性症状,所以该治疗领域始终处于“儿童有药,成人无药”的尴尬境地。
此次拓展适应症的获批,是基于一项全球KOMETⅢ期研究的阳性结果:在145例成人患者中,司美替尼组经独立中心审查确认的ORR达到20%(14/71),而安慰剂组为5%(4/74)。中国亚组数据亦同步验证了显著临床获益,在纳入的4个研究中心数据中,中国患者的疗效表现与全球总体人群高度一致,部分指标甚至更为突出,肿瘤体积较基线中位缩小达54.5%,远超主要分析中的总体水平。

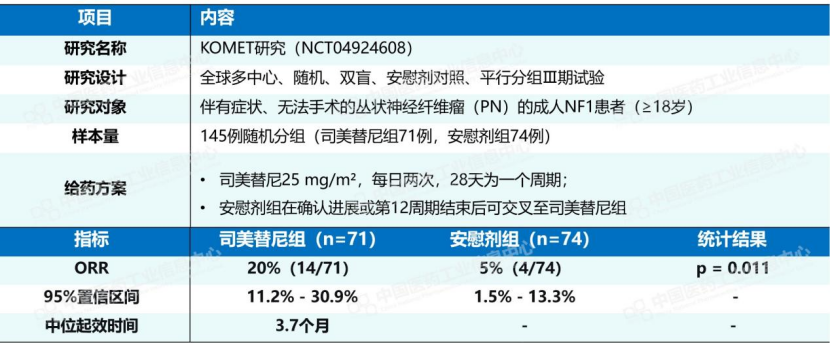
数据来源:Pharma ONE药物研发大数据平台-全球临床试验结果板块,中国医药工业信息中心
KOMET研究证实,即便在肿瘤负荷更高、病程更复杂的成人群体中,司美替尼仍可实现显著的肿瘤体积缩小与临床症状改善,为成年患者的规范化治疗提供了首个循证医学的标准方案。本次适应症的拓展,使同一款药物能无缝衔接儿童至成人的全病程管理,让患者转诊、长期随访、剂量调整可以“同药同策”,实现治疗策略上的“年龄脱钩”与“病程连续覆盖”。
科赛优®,从“唯一”到“之一”
在全球范围内,NF1-PN药物赛道正经历从司美替尼单药统治到多元竞争格局的演变。根据Pharma ONE显示,司美替尼曾凭借先发优势(2020年获FDA儿科适应症、2023年进入中国)长期占据垄断地位。直到2025年2月,SpringWorks Therapeutics的MEK抑制剂莫达美替尼(Mirdametinib,Gomekli®)获FDA批准用于2岁及以上NF1-PN患者,成为该适应症全球第二款上市药物,宣告“双雄并立”时代开启。

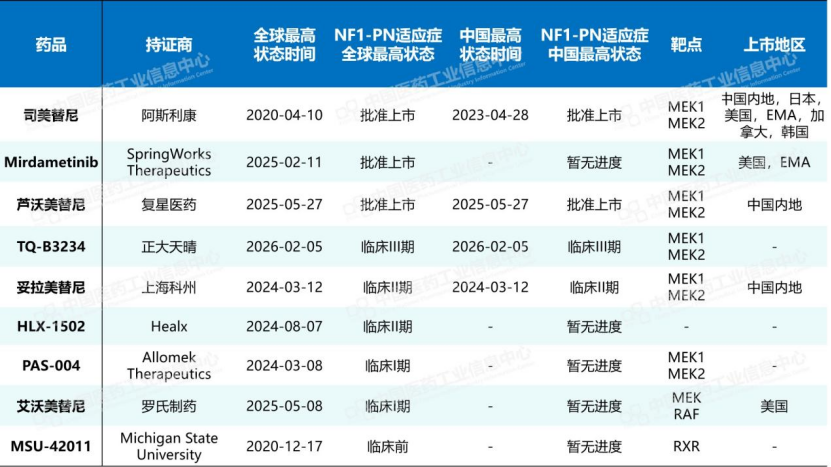
数据来源:Pharma ONE药物研发大数据平台-全球药物研发板块,中国医药工业信息中心
点击“阅读原文”获取更多数据
莫达美替尼在一项Ⅱb期研究中展示出成人ORR 41%、儿童ORR 52%的指标,且“3周服药,1周停药”有着更好的依从性。而司美替尼凭借长期临床使用经验、丰富的真实世界数据,和已建立的患者基础,在医生处方行为上占据先发优势。
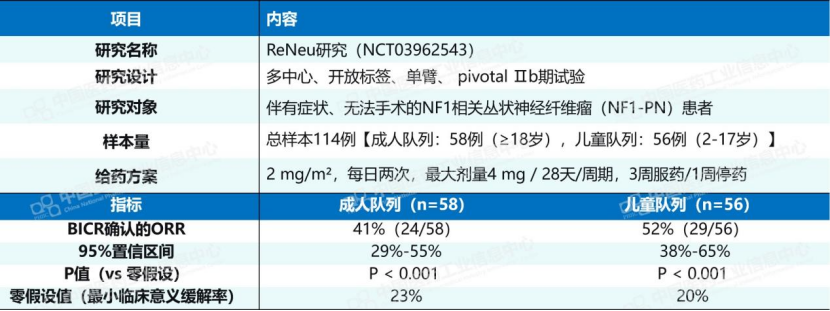
数据来源:Pharma ONE药物研发大数据平台-全球临床试验结果板块,中国医药工业信息中心
国内市场则呈现“进口主导+本土追赶”的特征。进口端,司美替尼通过本次成人适应症拓展,进一步巩固了其独家地位。本土创新也在迅速跟进:复星医药自主研发的芦沃美替尼于去年5月获批,成人适应症补充申请于今年2月获受理并纳入优先审评;此外,正大天晴和上海科州的MEK抑制剂处于临床2/3期。也就是说,在不久的将来,国内NF1-PN赛道将从“单一进口药”切换为“进口+国产”的多元选择。
阿斯利康如何筑起产品矩阵护城河?
面对竞品和本土追赶,阿斯利康如何围绕NF1-PN领域布局“体系化防御”?
剂型层面,司美替尼目前有胶囊和颗粒剂,莫达美替尼有胶囊和分散剂,颗粒剂和分散剂在低龄儿童、吞咽困难患者中确实更方便。阿斯利康在罕见病领域有过类似操作,比如把依库珠单抗从静脉针向皮下制剂延伸。因此,后续极有可能推动司美替尼开发更优的儿童顺应性剂型,如口服溶液或长效剂型。一旦剂型矩阵补全,将有效对冲竞品用药依从性优势。
管线协同层面,尽管阿斯利康尚未在NF1领域启动联合治疗的注册研究,但司美替尼与自家PD-L1抑制剂度伐利尤单抗的联用已在实体瘤领域探路。更重要的是,当年花大价钱买下的Alexion Pharmaceuticals,现在已经整合成内部罕见病部门,这个架构的好处是:使阿斯利康在未来开发药物联合疗法(例如将抗癌药司美替尼与抗炎、抗纤维化药物联用)时,能够更顺畅地进行跨团队、跨领域的内部资源整合与合作。
此外,阿斯利康靠罕见病部门构建的“诊断—治疗—随访”闭环,是其产品矩阵中难以被复制的隐性护城河。从支持患者组织,到铺多中心临床研究网络,这套全链条服务能力让司美替尼不只是一款药,而是一整套针对NF1-PN患者全病程的解决方案。在罕见病领域,生态级的布局比单药迭代更能拿捏住市场。
欢迎在评论区留下您的看法👏



