Cell Metab:皮肤"遥控"肠道,复旦大学黄立豪等合作揭示银屑病远程指挥炎症性肠病新机制
银屑病是一种典型的自身免疫性疾病,其影响远不止于皮肤。银屑病患者发生炎症性肠病的风险增加,但这种共病的机制仍不清楚。
2026年3月18日,复旦大学黄立豪、王嘉希、颜克香共同通讯在
Cell Metabolism(IF=30.9)
在线发表题为
Psoriasis modulates inflammatory bowel disease risk and intestinal epithelium lipid metabolism via IL-1β-producing macrophages
的研究论文。该研究发现银屑病通过产生IL-1β的巨噬细胞调节炎症性肠病风险和肠上皮脂质代谢。
该研究揭示了人类银屑病严重程度和餐后APOB48水平之间的反比关系。使用新开发的光转化APOB敲入小鼠和肠道类器官,表明产生IL-1β的巨噬细胞驱动APOB降解和上皮脂质积累,这揭示了银屑病和肠道炎症共病之间的新联系。

自身免疫性疾病,包括银屑病、类风湿性关节炎和系统性红斑狼疮,通常与代谢紊乱的风险增加有关,代谢紊乱会显著增加发病率和死亡率。银屑病是一种免疫介导的炎症性皮肤病,其特征是角质化细胞过度增殖和免疫细胞浸润,通常表现为皮肤外表现。
流行病学研究已经证实银屑病和肠道炎症之间存在密切的相关性。银屑病患者通常表现为亚临床肠道炎症,并且在患有溃疡性结肠炎(UC)和克罗恩病(CD)的情况下,患炎症性肠病(IBDs)的风险较高。
最近的研究发现,银屑病患者的血流中存在来自肠道的细菌DNA,这表明生物失调在IBD发病机制中具有潜在作用。虽然UC主要影响结肠,但CD主要涉及小肠,该区域的特点是与大肠相比,细胞分布、免疫反应和微生物负荷明显较低。
然而,银屑病和CD之间的机制联系,尤其是银屑病诱导的免疫激活如何独立于微生物区系变化而触发CD,仍然知之甚少。此外,尚不清楚治疗自身免疫的非IBD症状,如银屑病中的皮肤损害,是否足以减轻IBD共病。
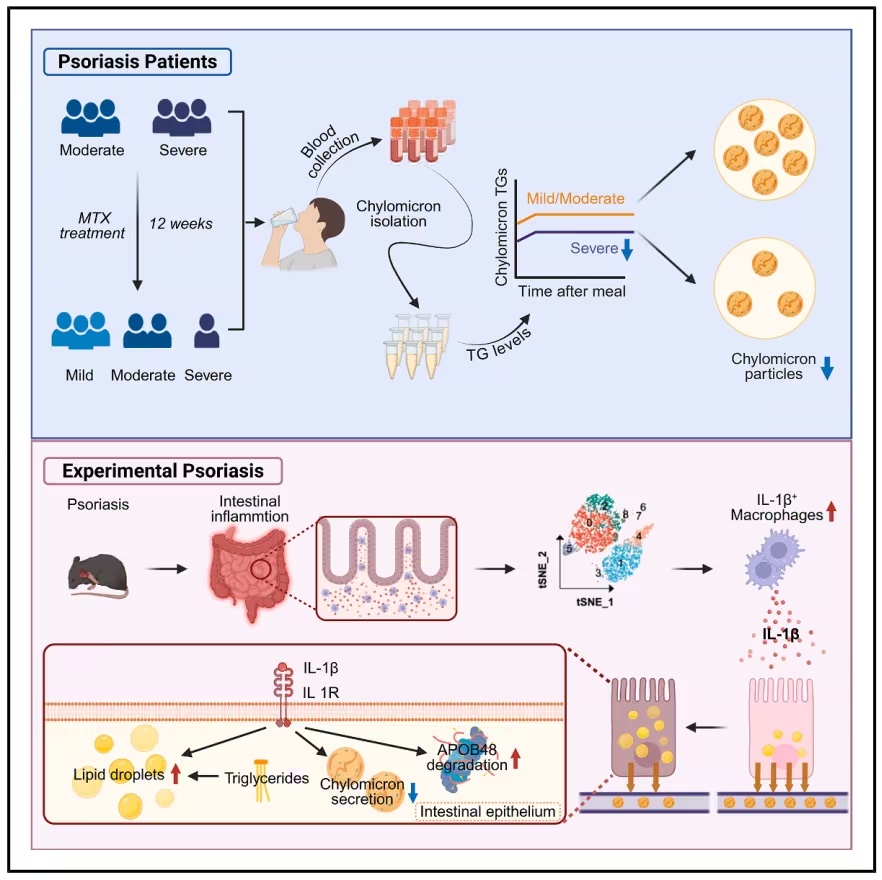
机理模式图(图源自
Cell Metabolism
)
在一项临床队列研究中,研究人员观察到银屑病严重程度与餐后血浆载脂蛋白B48水平呈负相关,这一发现在实验性银屑病小鼠模型中重现,表明肠道脂质处理受损。为了直接研究这一过程,研究人员开发了一种重组光可转换载脂蛋白B报告基因,能够实时定量肠内器官和体内内源性乳糜微粒的产生。
利用这一系统,证明银屑病促进产生白细胞介素(IL)-1β的肠巨噬细胞的扩张,从而加速载脂蛋白B的降解,损害乳糜微粒的分泌,驱动上皮脂质积聚,并加剧粘膜炎症。综合人类和实验数据,该发现表明巨噬细胞驱动的肠上皮细胞代谢失调是银屑病和肠道炎症之间的一种机制联系,并强调肠道IL-1β是一种潜在的治疗靶点。
复旦大学代谢与整合生物学研究院博士研究生吴嘉琪、刘双双以及硕士但维为论文共同第一作者。复旦大学代谢与整合生物学研究院黄立豪青年研究员、复旦大学人类表型组研究院王嘉希青年副研究员、复旦大学附属华山医院颜克香主治医生为本文共同通讯作者。
参考消息:https://www.cell.com/cell-metabolism/fulltext/S1550-4131(26)00057-4
