Nature:诺奖得主联手合作!新一代体内 CAR-T诞生!体内定点插入大片段DNA,高效生成CAR-T细胞
经过改造以表达嵌合抗原受体(CAR)或 T 细胞受体(TCR)的工程 T 细胞已经改变了癌症治疗的方式,并正被探索用于自身免疫性疾病和感染性疾病的治疗。通过基因编辑来增强 T 细胞的功能,无论是通过破坏内源性基因还是精确插入 DNA 负载物,都显示出相当大的潜力。
然而,体外制造过程漫长且成本高昂,限制了这些疗法的可及性。体内生成 CAR T 细胞可以克服这些障碍,但目前的方法要么依赖于短暂表达且持久性有限,要么依赖于随机整合缺乏特异性的 DNA 负载物。
2026年3月18日,加利福尼亚大学旧金山分校Justin Eyquem及Jennifer A. Doudna等团队合作在
Nature
在线发表题为
In vivo site-specific engineering to reprogram T cells
的研究论文,该研究证明了通过体内特定位点整合大型 DNA 负载物可以实现稳定且细胞特异性的转基因表达。
该研究开发了一个双载体系统,分别使用包被的递送载体和腺相关病毒来递送 CRISPR–Cas9 核酸酶复合物和 DNA 模板。研究人员对这两个载体进行了优化,以实现针对 T 细胞的特异性递送和基因靶向效率。
通过将一种嵌合抗原受体(CAR)基因转导至 T 细胞特异性位点,该研究在 B 细胞缺乏症的人源化小鼠模型以及血液系统和实体瘤模型中,在体内生成了具有治疗水平的 CAR T 细胞。这些发现为更高效、更精准且更易于普及的 T 细胞疗法提供了途径。

CAR T 细胞是治疗血液系统恶性肿瘤的一种很有前景的方法;截至目前,美国食品药品监督管理局已批准了七种 CAR T 细胞疗法。标准的 CAR T 细胞疗法需要根据患者情况进行个性化生产,其局限性在于产品质量不稳定、生产周期长以及成本高昂。
CAR 通常通过逆转录病毒载体进行递送,导致随机整合产生的表达结果存在差异性。通过使用 CRISPR-Cas9 和腺相关病毒(AAV)介导的同源定向修复(HDR),将 CAR 靶向整合到人类天然 TCRα 基因座(TRAC)中。
TRAC-CAR T 细胞显示出动态的 CAR 表达,能够延缓细胞耗竭并提高在异种移植和免疫功能正常模型中的肿瘤控制效果。这项工作对于异基因 CAR T 细胞疗法的发展至关重要,因为它在转基因插入后破坏了 TCR——这是限制移植物抗宿主病(GvHD)的必要步骤。
使用来自健康供体或诱导性多能干细胞的异基因 TRAC-CAR T 细胞进行的临床试验,在与深度淋巴细胞清除预处理相结合的情况下,已使患有血液系统恶性肿瘤的患者实现了完全缓解。异基因疗法可以通过从健康捐赠者身上提取细胞来制造现成的药物,从而解决生产方面的限制问题。然而,异基因嵌合抗原受体 T 细胞最终会被机体排斥,并且还出现了频繁复发的情况。
直接在体内生成嵌合抗原受体(CAR)T 细胞或许能够避开白细胞分离和生产过程中所遇到的种种障碍。它还有可能促进形成一个未高度分化的 CAR T 细胞群体,这一特征与增强的抗肿瘤活性有关。
迄今为止,体内生成 CAR T 细胞的努力使用了随机整合的病毒载体来实现持续的 CAR 表达,或者使用脂质纳米颗粒(LNPs)来实现短暂的 CAR 表达。这两种方法最近在非人类灵长类动物中得到了验证,并且最近也在一项 I 期临床试验中进行了评估。这些方法面临诸多挑战,包括如何将基因高效递送至治疗剂量以及避免脱靶转导的风险。
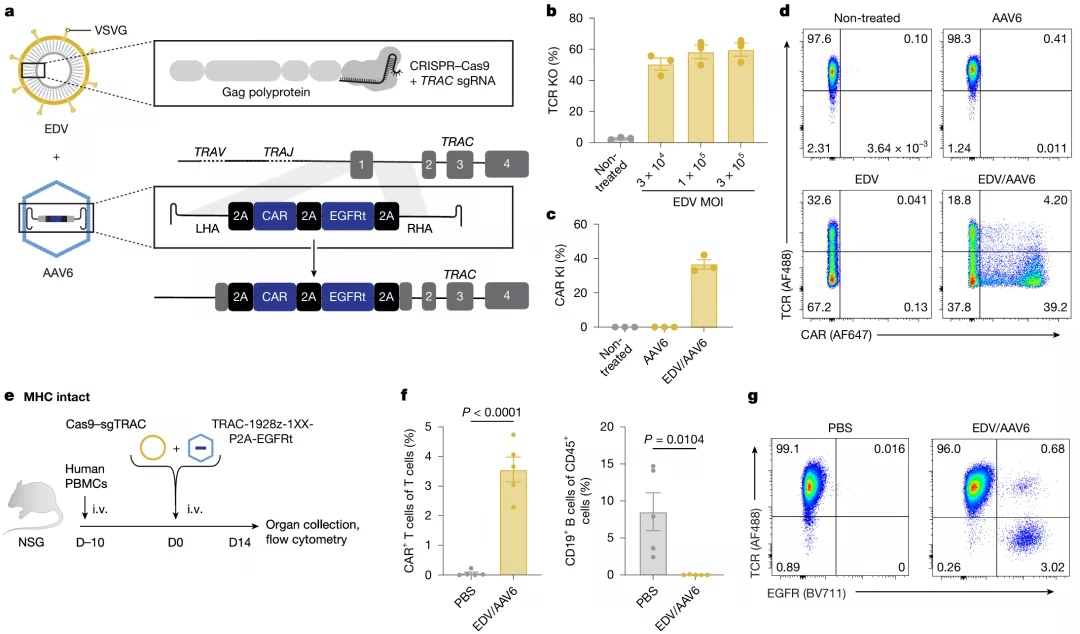
将 Cas9-EDV 和 HDRT-AAV 一同递送,能够在体外和体内生成 TRAC-CAR T 细胞(图源自
Nature
)
递送和 CAR 表达都应具有 T 细胞特异性,因为对造血干细胞(HSCs)进行脱靶改造可能会导致突变性转化,而 CAR 在肿瘤细胞中的表达可能会阻止细胞表面表达 CAR 目标蛋白并导致抗原阴性的复发。脂质纳米颗粒递送 CAR mRNA 会导致短暂的 CAR 表达,这可以防止插入性突变或稳定的肿瘤细胞表达,但所需的剂量仍不清楚。
慢病毒载体的包膜结构可以经过改造以提高对 T 细胞的特异性,但任何被转导的非 T 细胞也会表达这种嵌合抗原受体(CAR),除非使用细胞谱系特异性启动子,否则这些细胞存在潜在的插入突变风险。研究人员提出了一种假设,即在体内将无启动子的 CAR 转基因整合到 TRAC 位点上,能够实现 T 细胞特异性和生理状态下的 CAR 表达,同时避免了体外细胞制造的过程。截至目前,仍无法在人体 T 细胞体内实现大 DNA 负载的精确体内整合。
该研究开发了一种将腺相关病毒(AAV)与包膜递送载体(EDV)相结合的方法,用于在体内对人类原代 T 细胞进行定位特异性转基因整合。通过优化 AAV 和 EDV 工具,以提高细胞特异性递送效率并增强对人类中和抗体的抵抗力,研究人员能够在体内生成具有治疗水平的 TRAC-CAR T 细胞,并在多个人类化小鼠模型中控制肿瘤生长。
参考消息:https://www.nature.com/articles/s41586-026-10235-x
