又一款阿尔茨海默病 (AD) AAV基因疗法即将启动临床
阿尔茨海默病 (Alzheimer’s Disease, AD) 俗称老年痴呆症,是一种以记忆力减退、认知功能进行性下降为特征的神经退行性疾,目前尚缺乏非常有效治疗方法。据统计,目前全世界有超过5000万的AD患者。2021年我国现存的AD及其他痴呆患病人数达1699万多例,约占全球患病人数的29.8%,是我国老龄化社会的重大挑战,开发有效的治疗药物尤为迫切。
近日,在哥本哈根举行的2026年阿尔茨海默病与帕金森病 (AD/PD) 国际会议上Ultragenyx旗下子公司Amlogenyx首次披露了其用于治疗阿尔兹海默病的在研AAV9基因疗法AM805的最新临床前数据。结果显示,AM805在小鼠模型中不仅能显著降低淀粉样蛋白水平,并且降解幅度不逊于甚至在部分情况下超越了目前已获批的单抗药物,有望为全球数千万AD患者带来革命性的治疗选择,也让基因疗法在神经退行性疾病领域的应用再添新进展。
机制破局:从“免疫标记”转向“催化降解”
近日,在哥本哈根举行的2026年阿尔茨海默病与帕金森病 (AD/PD) 国际会议上,Ultragenyx (NASDAQ: RARE) 旗下子公司Amlogenyx首次披露了其用于治疗阿尔兹海默症的在研AAV9基因疗法AM805的最新临床前数据。结果显示,AM805在小鼠模型中不仅能显著降低淀粉样蛋白水平,并且降解幅度不逊于甚至在部分情况下超越了目前已获批的单抗药物,有望为全球数千万阿尔茨海默病患者带来革命性的治疗选择,也让基因疗法在神经退行性疾病领域的应用再添新进展。

阿尔茨海默病 (Alzheimer’s Disease, AD) 俗称老年痴呆症,是一种以记忆力减退、认知功能进行性下降为特征的神经退行性疾。其核心病理特征之一是β淀粉样蛋白 (amyloid beta-peptides, Aβ) 在大脑内异常蓄积,形成细胞外斑块和细胞内沉积,最终导致神经元损伤和认知功能衰退。目前获批的主要用于早期认知障碍至轻度阿尔茨海默症的仑卡奈单抗 (Leqembi) 和多纳奈单抗 (Kisunla) 均依赖抗体标记淀粉样蛋白,通过免疫系统介导清除,虽能缓解疾病进展,但存在明显局限。
溶酶体系统是降解蛋白质、核酸等生物大分子的主要途径之一,内含多种水解酶,与细胞自噬息息相关,对维持细胞内稳态具有重要意义。越来越多的证据表面,溶酶体功能障碍和溶酶体区室的寡聚化在阿尔茨海默病的Aβ积累和组织损伤中起着关键作用,也是潜在的治疗靶点。针对溶酶体功能障碍开发包括针对阿尔茨海默病在内的神经退行性疾病的治疗方法已成为临床上一个日益重要的目标。
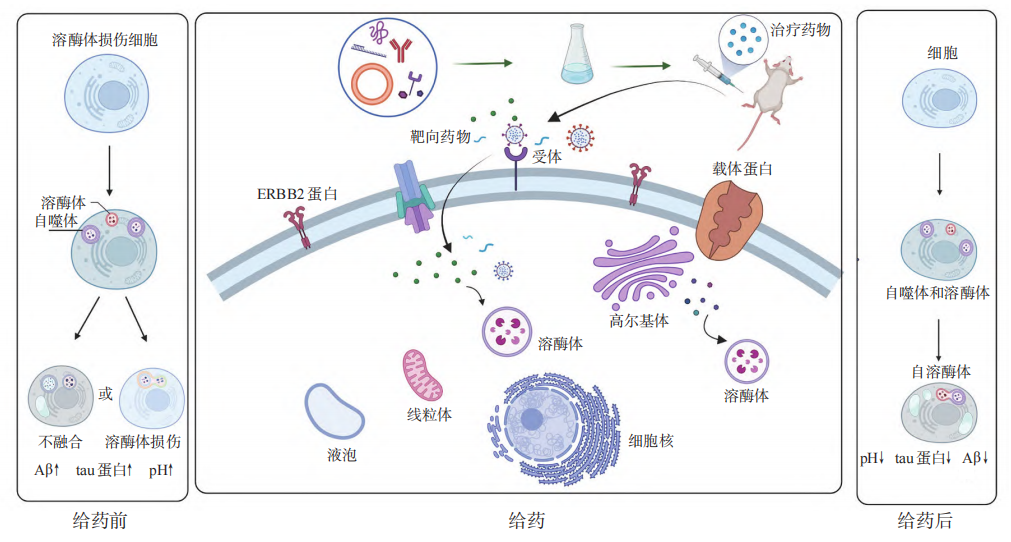
▲ 靶向溶酶体药物治疗阿尔茨海默病的研发示意图闻
AM805 (AAV9-PPCA) 疗法通过采用具有良好的中枢神经系统靶向性的AAV9载体将编码保护性蛋白/组织蛋白酶A (protective protein/cathepsin A, PPCA) 的基因直接递送至递送至神经元,从而主动降解细胞内Aβ和细胞外斑块。PPCA是一种位于溶酶体中的多功能蛋白,作为一种溶酶体羧肽酶,它可作为淀粉样蛋白降解蛋白酶在神经元溶酶体内直接催化分解β淀粉样蛋白,有望绕过仅限于细胞外靶向的局限性,实现“催化性淀粉样蛋白降解”,这一过程既能清除细胞外的淀粉样斑块,也能解决抗体疗法无法触及的细胞内淀粉样蛋白蓄积问题。
▉ 临床前数据亮眼:剂量依赖性起效
此次披露的临床前数据,覆盖了重度、中度阿尔茨海默病病理状态的小鼠模型,包含年轻和老年动物,全面验证了AM805的疗效和安全性。结果显示,给药12周后所有测试的给药途径均能使大脑中PPCA酶活性呈剂量依赖性升高,同时显著减少淀粉样蛋白阳性脑区面积;通过4G8阳性信号检测,细胞内和细胞外的β淀粉样蛋白水平均出现明显下降。
更值得关注的是,在非人灵长类动物中完成的安全性验证显示,PPCA可被安全递送至大脑,且酶表达水平与小鼠模型中观察到的治疗效果一致,这意味着AM805的治疗效果具备一定的物种通用性,为后续人体试验奠定了基础。不过需要注意的是,Amlogenyx公司尚未披露具体的定量终点、统计分析结果及详细安全性数据。
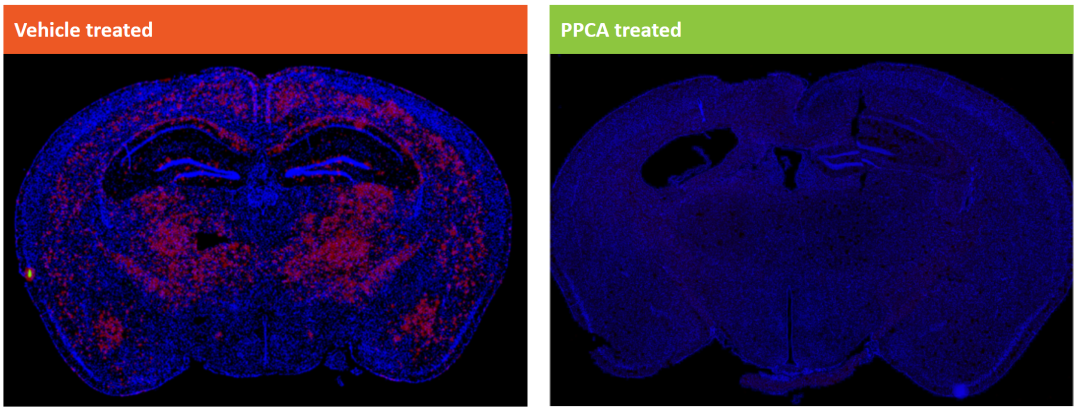
▲ AM805临床前数据
当前,阿尔茨海默病治疗市场已进入抗淀粉样蛋白抗体时代,但现有疗法的局限也十分突出,诸如需要长期静脉输注,且存在淀粉样蛋白相关影像学异常 (amyloid-related imaging abnormalities, ARIA) 风险,其中仑卡奈单抗 (Leqembi) 在亚洲人群中的ARIA-E (伴水肿或渗出) 发生率约为6.2%,多奈单抗的ARIA-E发生率则高达24%,均需要定期进行MRI监测。此外,抗体疗法无法触及细胞内淀粉样蛋白蓄积,难以实现更彻底的病理改善。
AM805作为一次性基因疗法,其理论上可实现“一次给药、长期有效”,彻底消除重复输注的负担,同时通过避免抗体介导的免疫激活,潜在降低ARIA风险;而催化性降解机制则能同时清除细胞内、外的淀粉样蛋白,有望实现更显著的病理改善。而且溶酶体酶过表达是否会扰乱神经元内正常的蛋白质稳态,AAV9在的转导效率如何确保足以逆转全脑的β淀粉样蛋白病理改变等核心问题都是巨大的挑战。如果Amlogenyx能按计划在2027年提交IND申请并顺利进入人体试验,AM805有望将跻身少数进入阿尔茨海默病人体试验的基因疗法之列,为全球数千万患者带来新的希望。
