BTK自免赛道势头强劲:2025年2款新药上市,2026年或再迎获批
布鲁顿酪氨酸激酶(Bruton's tyrosine kinase,BTK)靶点自发现至今已逾三十年,其在自身免疫疾病治疗领域的临床价值正加速兑现。
而继2025年两款BTK抑制剂(BTKi)接连成功获批自免适应症后,2026年有望再迎来一款重磅产品,持续验证这一靶点在自免疾病治疗中的广阔前景。
BTK抑制剂技术演进:从肿瘤靶向到免疫调节
BTK在B细胞受体和Fc受体信号通路具有至关重要的作用,同时还参与Toll样受体和趋化因子受体的调节,由于其在免疫过程中的关键作用,BTKi被视为治疗炎症和自身免疫性疾病的重要策略[1]。
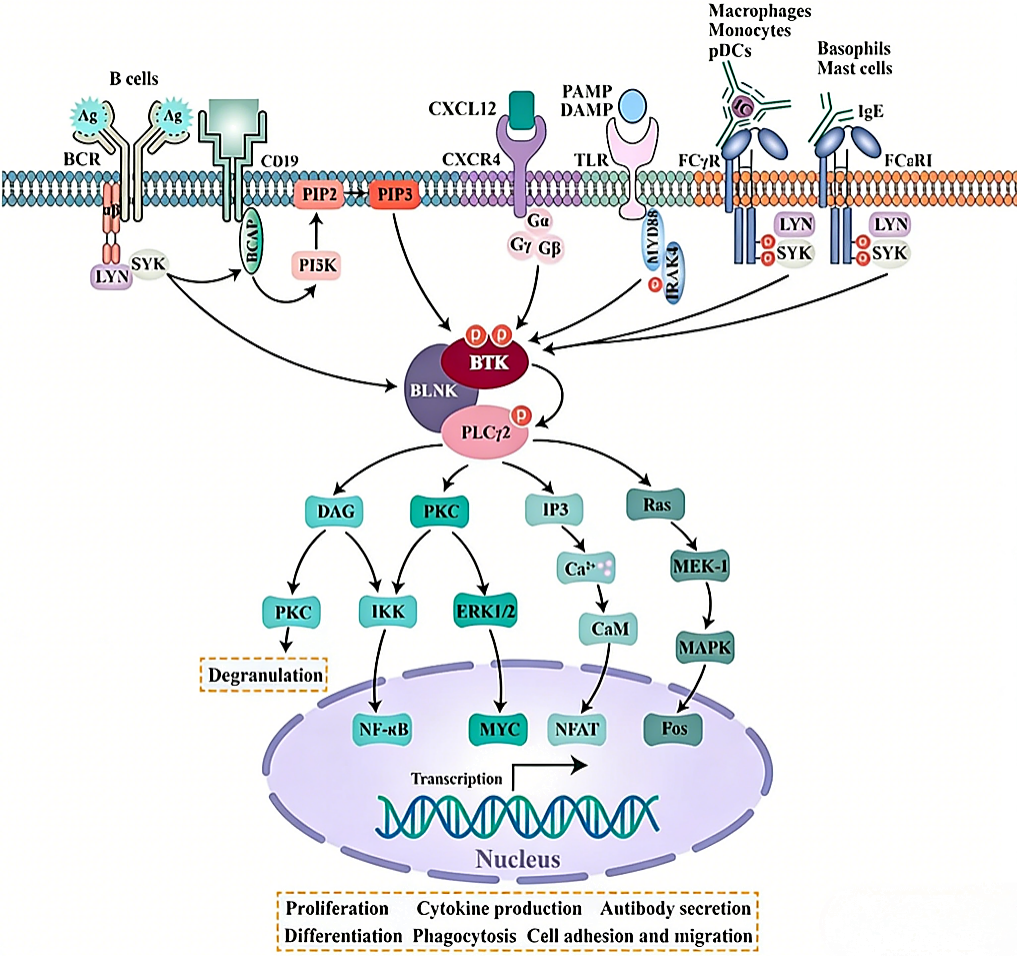
图1. BTK调节的多种受体信号通路
图片来源:参考文献[1]
自2013年首代BTKi伊布替尼开启血液肿瘤靶向治疗以来,BTKi已历经三代技术迭代:
第一代:以伊布替尼为代表,共价不可逆抑制,打破惰性淋巴瘤治疗僵局,年销售额一度迫近100亿美元。
第二代:通过提高选择性降低脱靶毒性,泽布替尼等凭借头对头临床优势实现国产替代与出海。
第三代:通过抑制方式革新(非共价可逆/共价可逆)克服C481S耐药突变,并将治疗边界拓展至原发性免疫性血小板减少症、慢性自发性荨麻疹等自身免疫领域。
截至2026年3月17日,见下表,全球已有8款BTKi上市,其中两款于2025年获批自免适应症,标志着该靶点从“肿瘤驱动”向“免疫调节”跨越。
表1.全球已上市BTK抑制剂
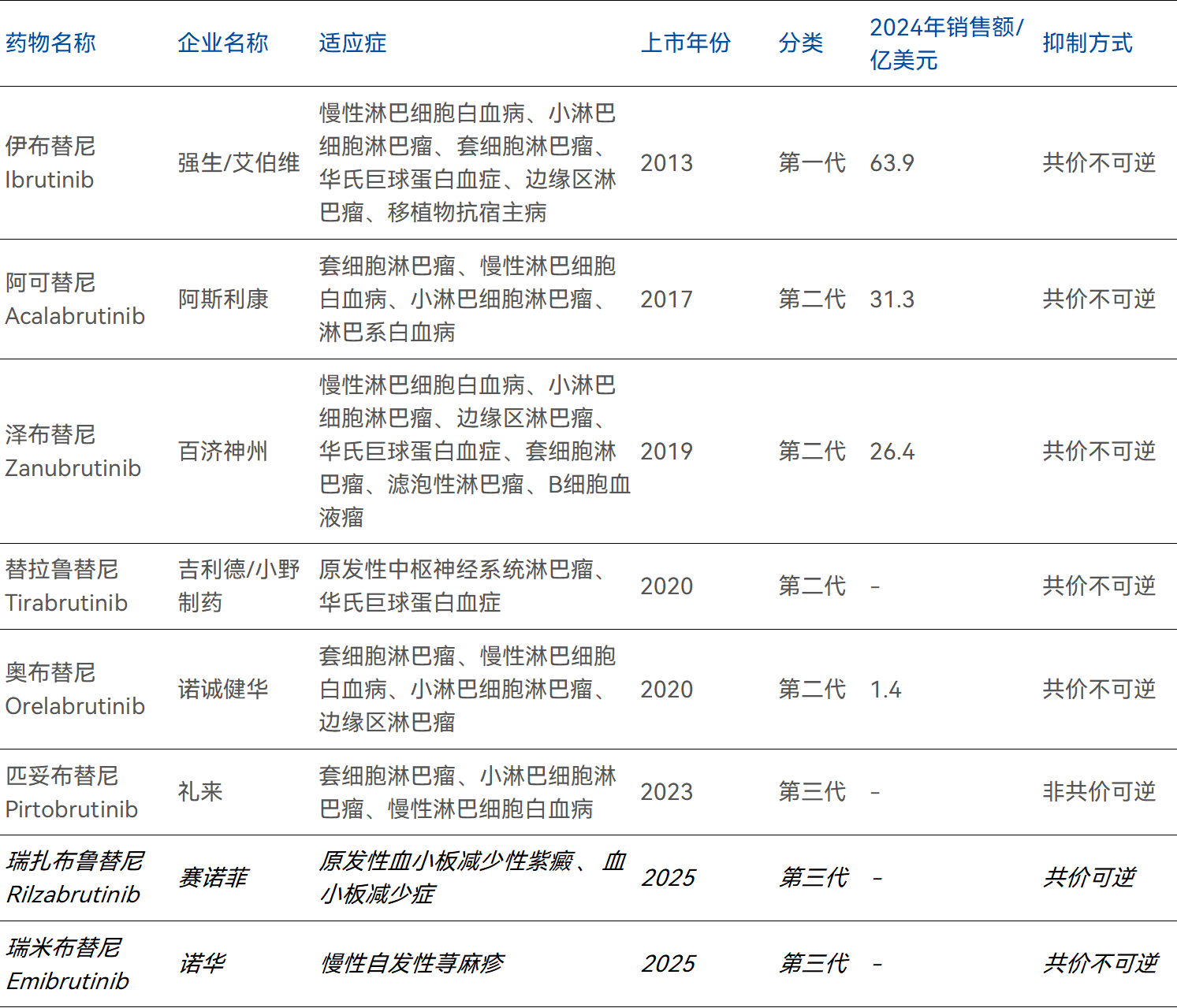
数据来源:药智数据,药智咨询整理(如有错误请指正,点击查看大图)
自免领域研发布局:三大核心赛道加速突破
截至2026年3月17日,全球已有超过40款BTKi针对自免适应症进入临床阶段。从临床进度、竞争激烈度、商业化潜力三个维度来看,ITP(原发性免疫性血小板减少症)、CSU(慢性自发性荨麻疹)、MS(多发性硬化)已成为BTK自免赛道的“三驾马车”。
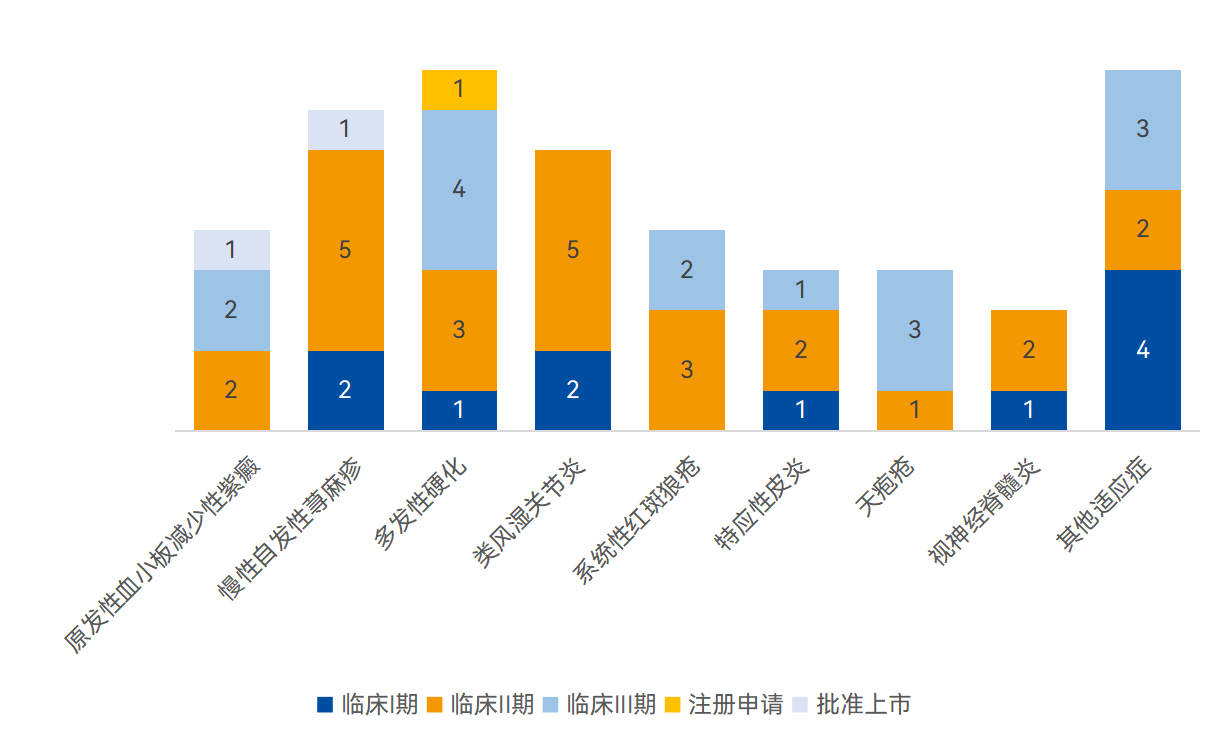
图2. BTK抑制剂自免适应症临床阶段分布
数据来源:药智数据,药智咨询整理
① ITP:赛诺菲率先撞线,国产紧跟其后
从数据上来看,ITP应当是BTKi在自免领域首个实现突破的适应症。
2025年,赛诺菲的瑞扎布鲁替尼率先获批,成为全球首款自免BTKi。其III期LUNA3研究显示,其持久应答率达23%,中位起效时间仅15天,出血评分显著改善,安全性良好,而该事件最大的意义在于,其成功验证了BTK靶点在ITP中的临床价值。
同时,另一方面国产梯队紧随其后。诺诚健华的奥布替尼已进入III期研究,其II期研究中,50mg剂量组连续两周血小板≥50×10⁹/L的患者比例达40%,对GC/IVIG无应答者亚组应答率高达75%。而三因泰医药的邦赛替尼也于2025年11月完成III期首例入组,未来国产双雄格局初现。
表2. 瑞扎布鲁替尼与奥布替尼ITP临床试验结果
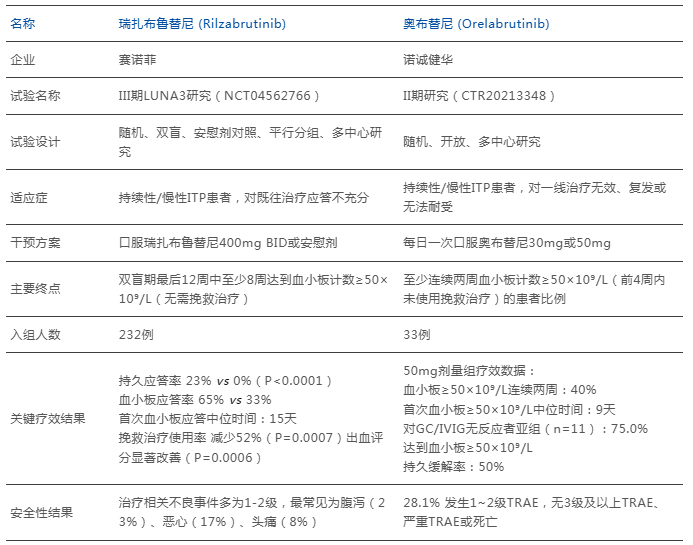
数据来源:公开数据,药智咨询整理
② CSU:诺华一马当先,后来者多路径突围
在CSU领域,诺华的瑞米布替尼凭借一周内快速起效、疗效持续至52周且无肝损伤信号的临床优势成为全球首个获批CSU的BTK抑制剂,为后来者树立了明确的疗效与安全标杆。
而面对领域内瑞米布替尼这一先发优势,国内外玩家也试图通过适应症拓展及降解剂技术等路径寻求差异化突破。
在领域II期临床梯队中,差异化布局成为主旋律。比如,赛诺菲的瑞米布替尼在多个自免领域广泛布局;小野药品的替拉鲁替尼同步探索天疱疮等适应症。国产力量方面,知微医药的TM471-1已进入II期,武汉人福的HWH-486则通过同时布局CSU和类风湿关节炎探索跨适应症策略,展现出“错位竞争”的清晰思路。
很明显,针对应用于CSU领域的BTK靶点药物,其下一代技术路径已开始浮出水面。百济神州的BGB-16673以BTK降解剂的全新机制入局,挑战“降解vs抑制”的临床优势;创响生物与和黄医药联合开发的IMG-004则走可逆性非共价抑制剂路线,力求通过不同的结合动力学特征提升安全性。这些创新管线的涌现,预示着CSU治疗正从传统的激酶抑制向更加多元的技术方向演进。
表3. 全球CSU领域BTK靶点临床在研管线
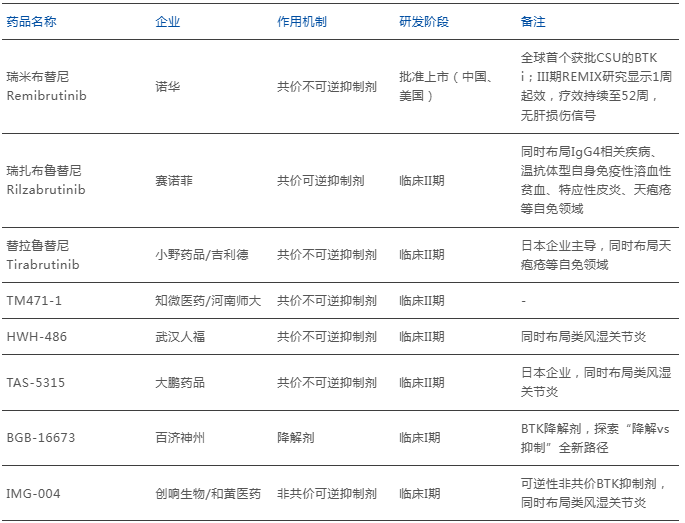
数据来源:公开数据,药智咨询整理
③ MS:分化加剧,安全性成“生死线”
如果说上述两适应症拥有先发优势,那么多发性硬化则或许是BTKi竞争最激烈的赛道,而疗效与肝毒性之间的平衡,正是决定谁能笑到最后的关键。
目前,在该领域内,罗氏的Fenebrutinib全面领跑。FENhance 2研究显示,其在复发型MS中使年复发率降低59%;FENtrepid研究证实,其在原发进展型MS中非劣效于奥瑞利珠单抗,上肢功能改善26%。该药计划于2026年上半年申报上市,有望成为首个覆盖RMS和PPMS的口服BTKi。
而另一方面,赛诺菲的Tolebrutinib则因安全性受阻。其在非复发性继发进展型MS研究中使6个月残疾进展风险降低31%,但4.1%的患者出现转氨酶升高≥3倍,FDA未予批准。肝毒性成为BTKi在MS领域的监管“生死线”。
国内方面,诺诚健华的奥布替尼同样瞄准nrSPMS,计划于2026年启动全球III期研究。若能复制Tolebrutinib的疗效,同时规避肝毒性风险,有望凭借更优安全性实现后来居上。
表4. 芬奈布鲁替尼与托布替尼MS III临床试验结果
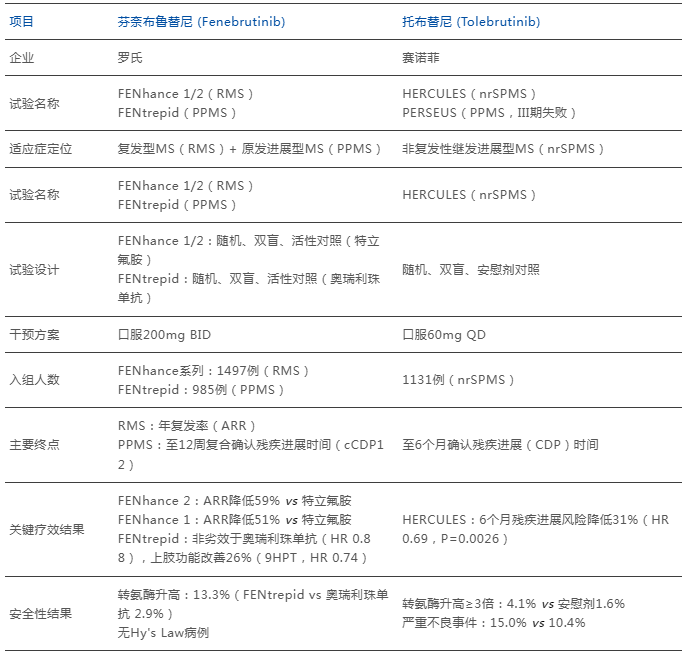
数据来源:公开数据,药智咨询整理
当然,除了上述三大核心赛道,BTKi也正在向多个罕见病和难治性自免领域渗透,展现出广泛的应用潜力。
在血液免疫领域,瑞扎布鲁替尼已进入温抗体型自身免疫性溶血性贫血和IgG4相关性疾病的III期研究,能否再下一城备受关注。在皮肤免疫领域,瑞扎布鲁替尼和Tirabrutinib齐聚天疱疮III期,同台竞技。在肾脏自免领域,百济神州的泽布替尼正在狼疮性肾炎和原发性膜性肾病中探索B细胞通路的治疗价值。此外,瑞米布替尼也在干燥综合征和全身型重症肌无力中布局II/III期研究,持续拓展BTKi的疾病边界。
结 语
2025年,瑞扎布鲁替尼和瑞米布替尼的成功上市,正式拉开了BTK抑制剂征战自免领域的序幕。
目前,BTK自免赛道格局已愈发清晰:ITP将迎来国产梯队III期数据集中读出,CSU形成“一超多强”的差异化竞争格局,MS则进入疗效与安全性双重验证的关键阶段。三大核心赛道之外,BTK的疾病边界正持续向wAIHA、IgG4-RD、天疱疮、狼疮性肾炎等多个罕见病和难治性自免领域拓展。
2026年,随着罗氏Fenebrutinib申报上市、诺诚健华奥布替尼III期数据揭晓、赛诺菲瑞扎布鲁替尼多项III期结果读出,BTK靶点在自免领域的临床价值将迎来新一轮集中验证。
谁能兼顾疗效、安全与差异化,谁就能在这条赛道上占据先机。
2026年,BTK抑制剂的“免疫调节”时代,正在加速到来。
参考文献
1.杨婉萍,房小宝,马宇乐,施志浩.BTK抑制剂治疗炎症和自身免疫性疾病的研究进展[J].药物化学,2022,10(1):70-83.
2.临床数据:据各企业公告

责任编辑:惜姌
声明:本文系药智网转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。
