新研究:牙周炎致病菌“基因刹车”将实现精准微生态治疗
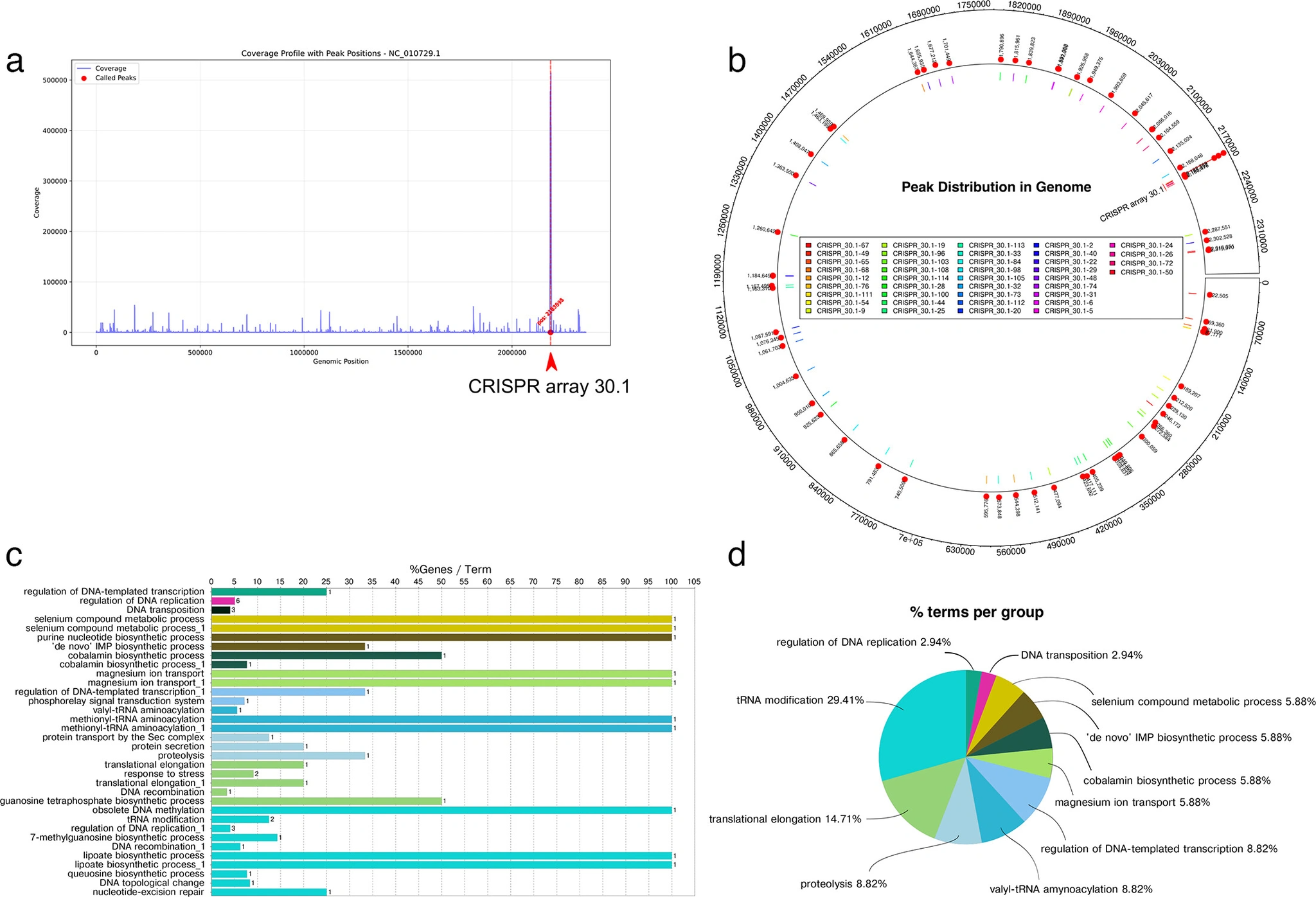
图源:A CRISPR array orchestrates virulence and host response in Porphyromonas gingivalis
佛罗里达大学(UF)近日发布新闻称,其发表于《Microbiology Spectrum》的一项针对牙龈卟啉单胞菌(Porphyromonas gingivalis)的研究显示,该病原体携带一种名为 CRISPR 阵列 30.1 的内部“基因刹车”,通过锁定该机制有望在不破坏口腔微生态平衡的前提下精准抑制牙周炎进展。
由佛罗里达大学(UF)牙科学院口腔生物学家 Jorge Frias-Lopez 博士领导的研究团队发现,牙周炎的主要致病菌 P. gingivalis 不仅利用 CRISPR 系统防御外部病毒,还通过这一系统进行自我调节。研究识别出的 CRISPR 阵列 30.1 其内部基因片段(spacers)并不匹配任何已知病毒,而是与细菌自身的 DNA 相匹配。
研究人员利用基因编辑技术删除了该阵列后发现,P. gingivalis 变得异常具有侵略性。实验结果显示,突变菌株产生的生物膜(牙菌斑的主要成分)数量是野生型的两倍。在 Galleria mellonella(大蜡螟)感染模型中,突变株诱导 50% 死亡的时间仅为 130 小时,而野生型为 200 小时(P < 0.0001)。此外,该突变株还引发了人类免疫细胞产生更强的炎症反应,分泌更多的 IL-6、CXCL1、CXCL2 和 CXCL9 等细胞因子。
Jorge Frias-Lopez 博士指出,P. gingivalis 这种“自我抑制”的生存策略极为狡猾。通过将侵略性控制在触发免疫系统全面攻击的水平之下,该病原体得以在牙龈中长期潜伏,将原本短暂的感染转化为长达数年的慢性炎症。
目前,牙周炎的常规治疗主要依赖洁治与刮治以机械清除菌斑,或使用抗生素。然而,抗生素往往会无差别杀灭口腔内的有益菌,导致微生态失调并产生耐药性。未来的精准疗法有望利用工程化噬菌体(专一性针对特定细菌的病毒)向 P. gingivalis 注入特定的 CRISPR 指令,将其内部“基因刹车”永久锁定,从而在不干扰健康微生物群的情况下实现治疗目标。
研究人员指出,牙周病是导致成年人牙齿脱落的主要原因,在美国影响约 42% 的 30 岁以上人群。据估计,牙周病每年给美国造成的经济损失超过 1500 亿美元,且其病原体毒素可进入血液,诱发心脏病和糖尿病等全身性炎症疾病。根据此前报道,学术界一直在探索各种精准干预路径,包括利用抗抑郁药的抗炎特性降低严重牙周炎风险,以及采用异体牙髓干细胞注射实现微创再生治疗。佛罗里达大学的这一新发现为牙周炎的靶向治疗提供了底层机制支撑。
据官方披露,该研究由美国国立卫生研究院(NIH)下属的国家牙科和颅面研究所(NIDCR)资助(资助编号:DE029775)。研究人员表示,尽管实验室数据表现出色,但该基因调控机制在人体临床中的转化仍需进一步验证。
【特别鸣谢】如果本文有错漏之处需要勘误,请联系我们的客服,届时我们会为您准备小礼物,感谢!
【免责声明】上述内容源于公开信息,可能存在不准确性,仅供参考。本文不构成对任何人的投资与决策建议,不对因使用本资料而导致的损失承担任何责任,并对本内容拥有最终解释权。文中图片均已获版权方授权
