绕过烦人的KRAS基因突变!CDK4/6+EGFR双药组合“借力打力”,胰腺癌治疗迎来全新破局!
胰腺癌被称之为癌中之王,这个类型的肿瘤恶性程度很高。此外胰腺癌还有一个特点就是近90%的患者携带的都是KRAS基因突变,但是可别想简单了。KRAS基因突变的位点可是有很多,比如G12C、G12D、G12V、G12R等等。总不能每一个位点都研发一款药吧。今天癌度给大家介绍一项最新的研究,这个研究给出了一条截然不同的思路:我们能不能"绕过"KRAS,去攻击它的"七寸"?
本文参考文献刊例示意图
一、胰腺癌治疗的困境:盯着KRAS打的无可奈何
胰腺癌(尤其是胰腺导管腺癌)之所以难治,一个核心原因就是超过90%的患者都存在KRAS基因突变。这个突变非常有特点,它强势地驱动着癌细胞疯狂生长、转移。但是对于KRAS的靶向药一直到最近才开始出来,而且还只是针对KRAS基因的G12C突变,而胰腺癌比较多的是KRAS的G12D。
即便是对于那极少数携带G12C突变的胰腺癌患者,使用KRAS靶向药之后效果也往往不尽如人意,不仅疗效与传统化疗相比并无明显的优势,而且耐药几乎必然出现,患者生存获益的时间通常也很短。
所以科学家一直在想,对于KRAS基因这个难啃的骨头该怎么办?如果说直接抑制KRAS突变基因比较困难,那么能不能用其他的方式给“驯服”或“套住”这个突变基因的致癌信号。
二、新突破:激活一个"刹车",同时关掉"油门"和"导航"
这是日本金泽大学的研究团队发表在《细胞死亡与分化》杂志上的一项研究,他们给出了一个令人振奋的答案。我们完全可以通过"借力打力"来解决烦人的KRAS,具体的形式是利用一个叫RB1的"刹车蛋白"来间接压制KRAS。
关键角色RB1:RB1是一个抑癌基因,该基因负责控制细胞的分裂。而KRAS突变的一大作用就是通过一系列信号传递,把这个"刹车"给"踩松"了,这就导致了细胞不受控制地分裂。
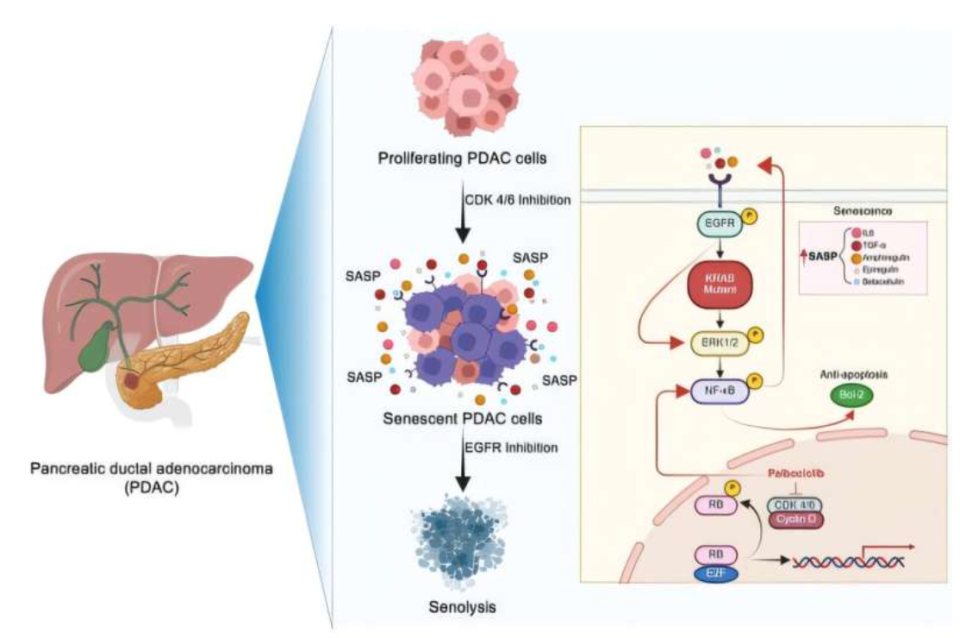
"借力打力"的策略:上面说到KRAS基因突变把RB1这个"刹车"给踩松了,那我们的策略就是哪里出问题就解决哪里的问题,使用目前上市的药物(CDK4/6抑制剂)把RB1重新"激活"或"踩紧"。当研究者用这类药物(例如已经获批用于乳腺癌的帕博西尼)处理胰腺癌细胞时,他们惊喜地发现:RB1的激活确实能反过来抑制KRAS的活性。
但是事情也并没这么简单。研究者后来还发现当CDK4/6抑制剂激活RB1后,癌细胞虽然被"刹车"逼入了"衰老"状态(不再分裂),但癌细胞并没有大量死亡。相反癌细胞启动了一个"自救"程序,它们通过分泌大量信号分子激活了细胞表面的EGFR,这个EGFR可是肺癌患者比较熟悉的致癌因素。所以大家能理解EGFR被激活之后癌细胞又继续能生存了,从而对CDK4/6抑制剂产生了抵抗。
三、双药联合精准清除,开启治疗新方案
上面咱们说到了既然癌细胞通过激活EGFR来抵抗帕博西尼,那咱们就把这两个基因都给抑制住!研究者们尝试了CDK4/6抑制剂 + EGFR抑制剂的组合疗法。
结果令人非常振奋。无论是在体外临床试验,还是在患有胰腺癌的小鼠身上,这两种药物的联合使用都展现出了强大的效果。双药联合将癌细胞精准地推向了断头台。
这个研究还发现组合疗法的用药顺序很重要。必须先用CDK4/6抑制剂让癌细胞进入"衰老"状态,再用EGFR抑制剂进行清除。如果顺序颠倒那么效果就会大打折扣。
这个发现最让人欣喜的地方在于这两种药物在临床上都已经获批使用。CDK4/6抑制剂(如帕博西尼)用于乳腺癌,EGFR抑制剂(如西妥昔单抗)用于结直肠癌和头颈癌等。这意味着这个组合方案一旦通过临床试验验证,就能快速应用到胰腺癌患者身上,不需等待新药漫长的研发周期。
这个"双药组合"策略绕开了KRAS抑制剂疗效不佳、易耐药的困境,为占绝大多数的、没有KRAS基因G12C突变的胰腺癌患者带来了切实的治疗新希望。癌度也期待这个治疗方案能尽快启动人体临床试验,也欢迎大家关注联系癌度申请全球新药临床试验入组的机会!
2026年福利
“吉爱3000”惠民检项目,最低2000+可及的二代基因检测专属福利,详情微信扫码进行基因检测报告解读、拼单团购美国/日本会诊、申请新药临床试验!
参考文献:
Yuanyuan Zhang et al, Deprivation of EGFR signal causes senolysis in PDAC with CDK4/6 inhibition, Cell Death & Differentiation (2025).