B7-H3 CAR-T 外泌体递送核酸治疗实体瘤,首款外泌体 CAR-T 明年将启动临床

2026 年 4 月 3 日
医麦客新闻 eMedClub News

外泌体可在稳定脂质双层膜内包裹核酸、蛋白质、脂质等物质,介导细胞间通讯。其纳米尺寸使其能高效穿透生物屏障、实现肿瘤部位选择性富集并延长体内循环时间,具有治疗实体瘤的潜力。
免疫细胞来源的外泌体(包括 DC、NK、T 及 CAR-T 细胞)已展现出良好抗肿瘤效果。T 细胞来源外泌体可携带穿孔素、颗粒酶等细胞毒性分子,不依赖细胞活化与增殖即可诱导肿瘤细胞凋亡。CAR-T 细胞分泌的外泌体同样携带 CAR 分子及颗粒酶、穿孔素等杀伤因子,因此继承了部分 CAR-T 的肿瘤杀伤能力,且不含 PD-1,可避免肿瘤细胞介导的免疫抑制。
食管鳞状细胞癌(ESCC)恶性程度高、进展快、预后差,晚期治疗选择极为有限。B7-H3 在 ESCC 及多种实体瘤中广泛高表达,参与肿瘤进展、免疫抑制及血管生成,且与患者不良预后显著相关,是理想治疗靶点。
微小 RNA(miRNA)长度约 20–24 nt,主要通过结合靶基因 3′-UTR 抑制 mRNA 表达或促进其降解,广泛调控生物学过程。miR-145 在多种肿瘤中表达下调,发挥抑癌作用,能够通过靶向不同的受体蛋白调控各种肿瘤的进展。
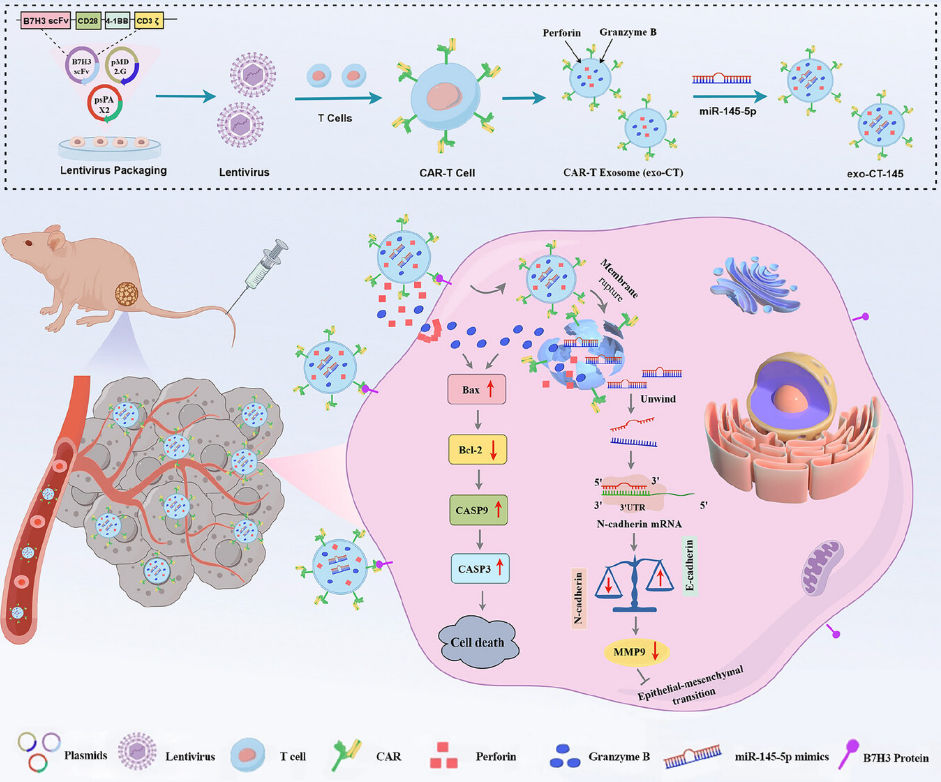
因此,研究人员构建靶向 B7-H3 的 CAR 慢病毒并转导 T 细胞,再经过扩增、诱导外泌体大量分泌、纯化等一系列步骤获得外泌体,并装载 miR-145,获得双功能的工程化外泌体(exo-CT-145),具有以下优势:可穿透实体瘤基质,解决 CAR-T 浸润不足问题;无活细胞,不扩增,安全性高;储存、制备、给药更简便,可标准化生产。
在体外研究中,exo-CT-145 可显著抑制 ESCC 细胞增殖、侵袭、迁移并诱导凋亡;在体内小鼠研究中,exo-CT-145 可高效靶向富集于肿瘤组织,显著抑制肿瘤生长、降低肿瘤血管生成,延长小鼠生存期。对体重、主要脏器(心、肝、脾、肺、肾)无明显损伤,肝肾功能指标正常,未诱发 IL-2、IL-8、TNF-α 等细胞因子风暴。
CAR-T 与外泌体融合发展
CAR-T 和外泌体均是当下的热门,CAR-T 衍生外泌体和利用外泌体递送开发 CAR-T 均已经有有研究者进行探索。
CAR-T 衍生外泌体
在一篇题目为「Sequential Targeting Hybrid Nanovesicles Composed of Chimeric Antigen Receptor T-Cell-Derived Exosomes and Liposomes for Enhanced Cancer Immunochemotherapy」的文章中,研究团队通过超速离心技术从培养的双特异性 MSLN/PD-L1 CAR-T 细胞培养基中分离并纯化外泌体,进而与肺靶向脂质体融合并装载紫杉醇(PTX)得到混合纳米囊泡(Lip-CExo@PTX)。

Lip-CExo@PTX 能迅速在肺部积聚并靶向 MSLN 阳性肿瘤细胞,PTX 促进细胞裂解并诱导免疫原性细胞死亡(ICD),进而吸引更多淋巴细胞浸润肿瘤组织,同时阻断 PD-L1 以减少浸润性 T 细胞的耗竭。
一篇题为「Inhalable CAR-T cell-derived exosomes as paclitaxel carriers for treating lung cancer」的文章报道了一种利用 CAR-T 细胞产生的外泌体(CAR-Exos)递送 PTX 以治疗非小细胞肺癌的方法。
Nature 上有一篇「CAR exosomes derived from effector CAR-T cells have potent antitumour effects and low toxicity」文章报道了 CAR-Exos 在小鼠体内展现出的强大抗肿瘤活性,并在小鼠异种移植模型中显示出剂量依赖性的肿瘤生长抑制作用。重要的是,研究人员发现 CAR-Exos 不表达 PD-1,因此不会像 CAR-T 疗法那样在实体瘤治疗中受到活性限制。
在利用 CAR-T 衍生外泌体的研究中,主要是集中在实体瘤这一适应症上,利用外泌体装载小分子治疗药物或者核酸类药物,结合 CAR-T 外泌体自身的抗原靶向性与细胞毒性,构建协同治疗体系,同时规避传统 CAR-T 疗法在实体瘤中面临的困境,提供了潜在治疗手段。
外泌体 CAR-T
今年 2 月,中国医药大学附属医院和长圣生技共同宣布成功研发全球首创 EXO001 靶向外泌体平台,可直接在体内编程 T 细胞,生成纳米抗体多靶点 CAR-T 细胞,已经在多项实体瘤动物研究中展现出显著疗效,甚至能够完全清除肿瘤细胞。
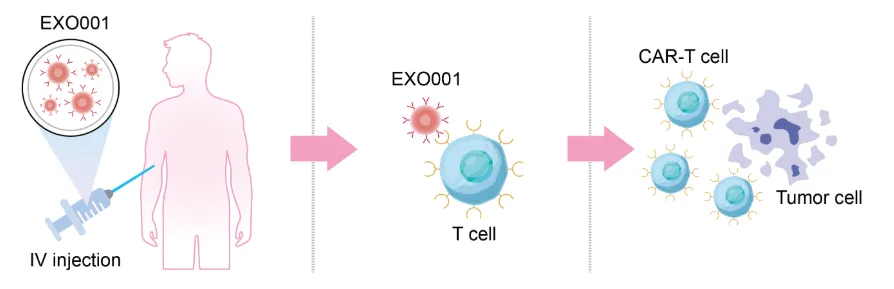
EXO001 是由基因工程 HEK293T 稳定细胞产生的 CD3e Nb-EVs 候选产品,核心设计是让外泌体成为「体内免疫训练的载体」。经静脉注射后,外泌体进入体内循环后,会经过脾脏等重要免疫器官,将 Nb-CAR.BiTE 精准递送至 T 细胞,在病人体内完成免疫编程,训练 T 细胞转化为多靶向 CAR-T 细胞,再由这些细胞瓦解免疫抑制性肿瘤微环境并杀伤肿瘤细胞。
研究团队在直肠癌、胰腺癌、恶性脑瘤与卵巢癌等多种实体瘤小鼠模型中证实,静脉注射 EXO001 可在体内有效生成 CAR-T 细胞,并成功渗透肿瘤微环境,显著抑制肿瘤生长,将生存期延长 2 至 3 倍,部分动物更出现癌细胞完全消失、长期无复发的成果。 同时,EXO001 采用外泌体作为递送载体,相较于病毒或合成脂质材料,具更高生物相容性和安全性,不易产生抗药抗体,有助于降低免疫相关风险。
相关研究成果已经在刊登在国际权威期刊 Advanced Science 上,目前,长圣生技正在进行开发和临床试验筹备,预计将在明年启动。
总结
整体而言,CAR-T 与外泌体的发展呈现出交叉融合的趋势,CAR-T 衍生外泌体将向多功能协同治疗方向探索,外泌体 CAR-T 将成为体内 CAR-T 制备的突破口之一,目前两个发展方向均处于早期阶段,作为新兴前沿技术,二者未来将有望推动治疗手段朝着更高效、更安全、更具临床转化价值的方向稳步前进。
责任编辑丨浔
校对丨浔
参考资料:
1.Yang, R.,,, et al. 2026. “Engineered CAR-T–Derived Exosomes Co-Delivering miR-145 and Cytotoxic Proteins for Targeted Solid Tumour Therapy.” Journal of Extracellular Vesicles15, no. 3: e70245.
精彩活动
长按识别二维码立即参与↓
推荐 1
4 月 9 日 19:00-20:30
CRBN 分子胶库革命:从设计到 IRF5 靶向降解的突破性筛选策略

推荐 2
4 月 16 日 19:00-20:30
2026 核算药物爆发启示,开发、药效机制研究与爆发的底层逻辑


点点“分享”、“点赞”和“在看”
给我充点儿电吧~