全球制药业洞察 | Structure口服GLP-1在减重方面具备竞争力 安全性在可控范围内
本文来自彭博终端,终端用户可运行NSN TCFCHBKGZAJP <GO>阅读原文。非终端用户可点击文末“阅读原文”预约演示。
全球市场版图日新月异,彭博行业研究(Bloomberg Intelligence)为您的企业战略助力。在制药与生物技术领域,无论是全球行业资讯与热点,还是制药管线里程碑及催化剂事件、财务预测…… BI涵盖广泛且深度的关键信息,旨在为您的决策提供可靠且具有竞争力的洞见支撑。

扫描二维码立即订阅
彭博生物制药双周报
本期主题:Structure口服GLP-1在减重方面具备竞争力 安全性在可控范围内
(彭博行业研究)——Structure旗下肥胖症候选药物aleniglipron的二期试验在更长随访期的数据表明,其疗效至少与诺和诺德的Wegovy口服剂型相当,并优于礼来的orforglipron。较低的起始剂量缓解了我们此前对耐受性的担忧,该方案也将用于三期试验;三期试验计划于今年下半年启动,并有望为2028年获批铺路。
更长随访显示aleniglipron具备同类最佳潜力
Structure的aleniglipron在ACCESS II(44周)及ACCESS开放标签扩展(OLE)研究(56周)中显示,绝对减重幅度最高达15%-16%,且截至试验期末,减重曲线未出现平台期。整体疗效与诺和诺德的Wegovy口服剂型相当,并优于礼来的orforglipron;后两者虽在三期试验中测试时间更长,但受试患者基线体重更轻。ACCESS II研究中,180mg与240mg aleniglipron剂量组的体重下降幅度相近,其中180mg组的耐受性与120mg相当,而240mg组观察到更高比例的呕吐和恶心症状。
扩展阶段以及另一项身体成分研究中的停药率均处于低单位数水平,支持Structure提出的“低剂量起始,缓慢增加”的滴定策略,该策略将用于三期试验。肝脏安全性方面未发现明显风险信号。
Aleniglipron的二期临床数据
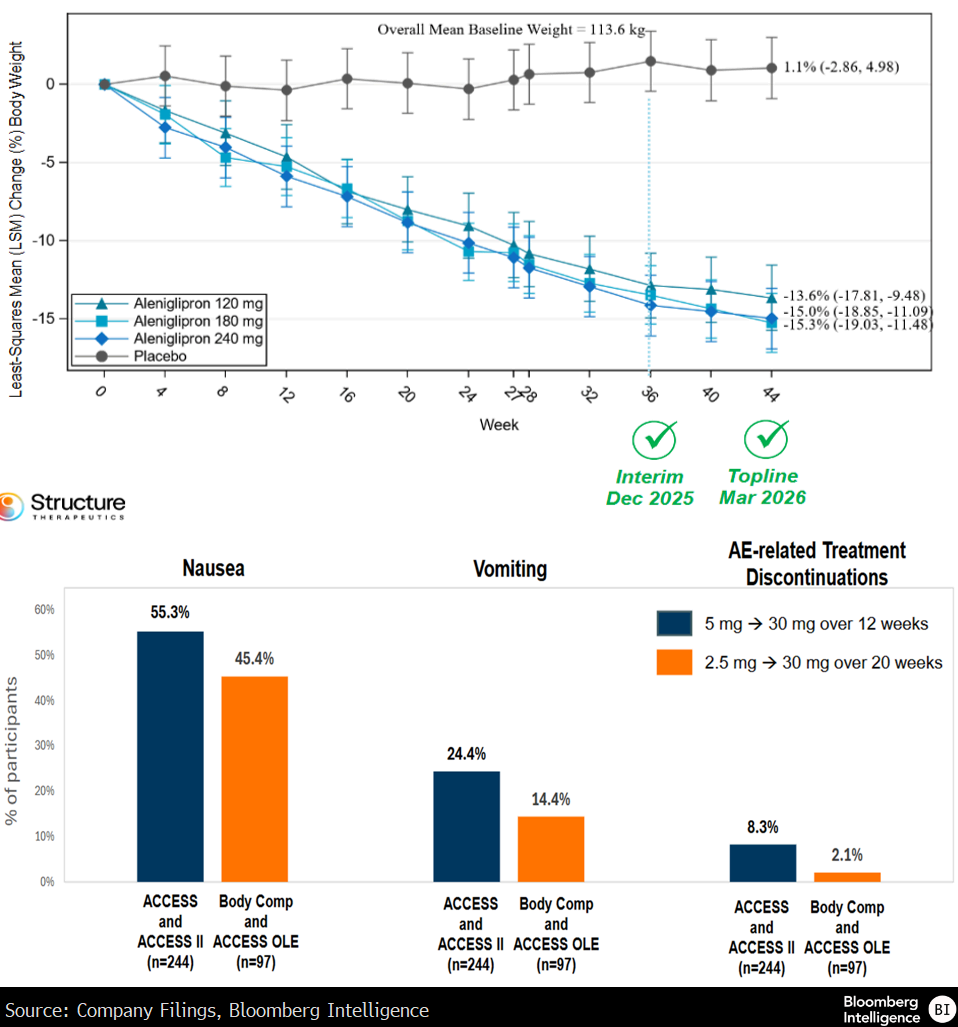
数据来源:公司文件、彭博行业研究
Aleniglipron疗效具备竞争力 高剂量下优于礼来
Structure的aleniglipron在二期b阶段ACCESS试验中,120mg剂量组体重下降12.1%,而安慰剂组仅下降0.8%;在36周时,减重曲线尚未出现平台期。该结果与礼来orforglipron在其中期研究中取得的疗效相当;后者测试对象的基线体重更轻,但女性受试者占比相近。在研究的开放标签扩展阶段,安慰剂组受试者在36周后转为使用aleniglipron 2.5mg,并在40周递增至5mg。这一人群在36-44周期间减重约3%,而此前接受活性治疗的各剂量组则额外实现1.1%-1.3%的体重下降。
在ACCESS II研究中,aleniglipron测试剂量最高至240mg;经安慰剂校正后,观察到最高达15.3%的体重下降,且在已披露的36周之后,疗效仍有进一步提升的可能。
减重效果对比
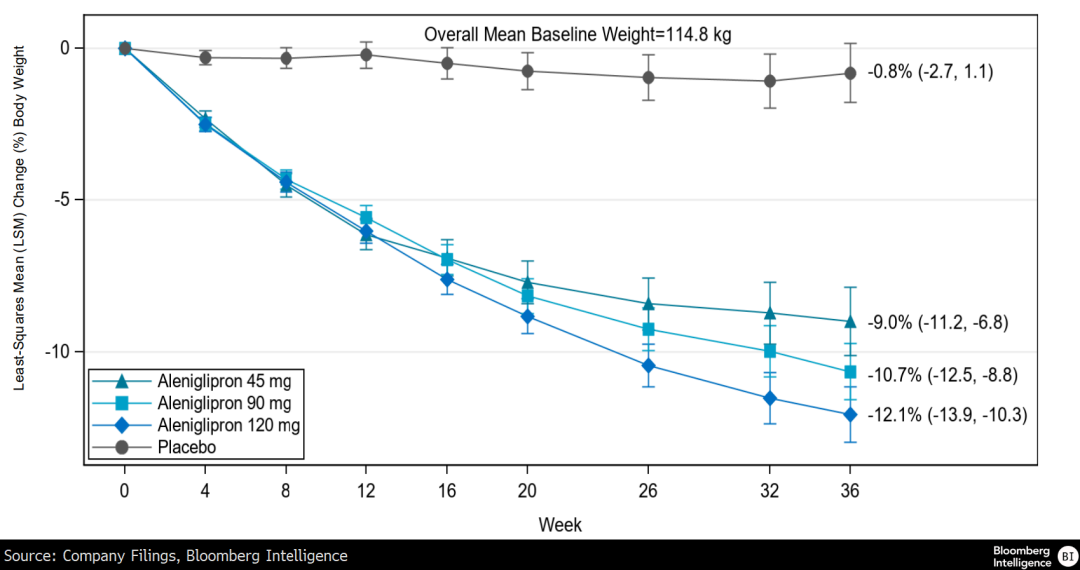
数据来源:公司文件、彭博行业研究
低起始剂量方案有望改善耐受性
Aleniglipron的疗效表现令人印象深刻,但早期数据在安全性方面的说服力相对不足,尽管尚未观察到肝毒性。ACCESS项目中的患者停药率处于同类药物区间内,且主要集中在前12周;不过,与orforglipron相比,其胃肠道副作用发生率偏高,尤其是呕吐和恶心,其中恶心在整个ACCESS试验中(120mg剂量下)均有发生。Structure在试验中采用电子日记记录症状,这种方式可能高估发生率,幅度最高可达一倍。三期试验将采用更低的起始剂量2.5mg(此前为5mg),这一调整有望改善耐受性;这一点已在OLE及身体成分研究的初步数据中得到体现,其中服用aleniglipron患者的停药率仅为2%,而ACCESS与ACCESS II研究合计的停药率为8%。
安全性对比
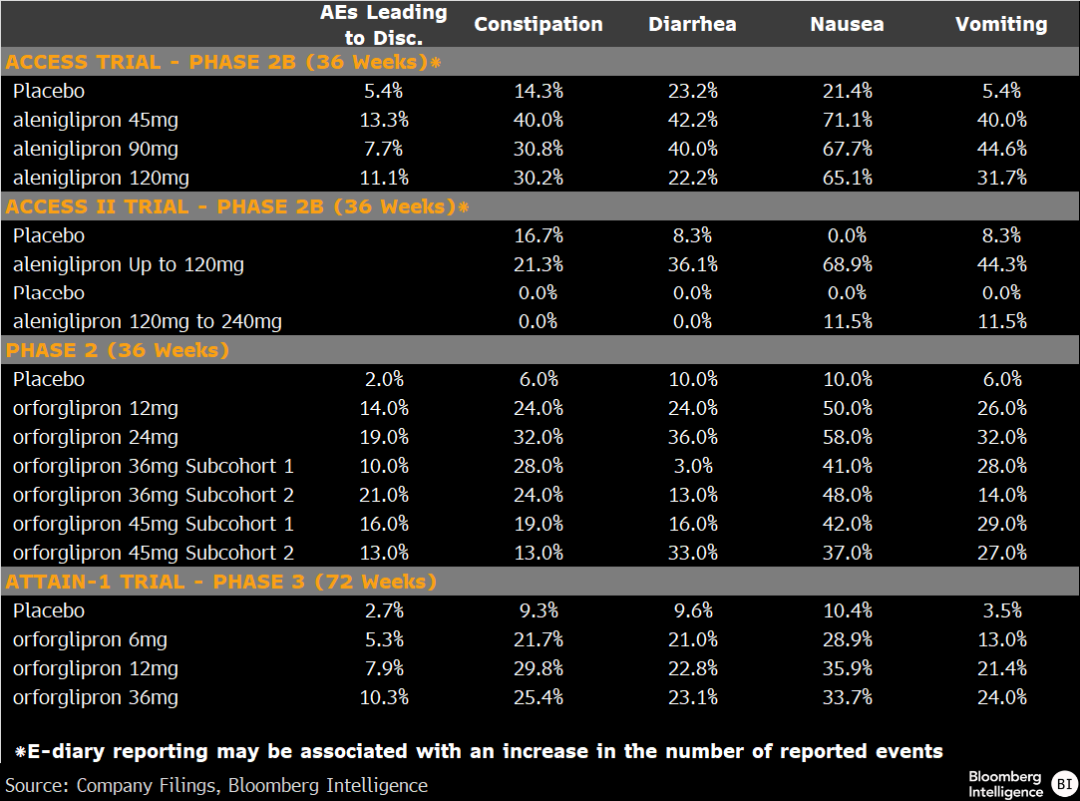
数据来源:公司文件、彭博行业研究
三期试验或于下半年启动 2028年前获批可能性不大
Structure预计将在二季度与美国食品药品监督管理局举行二期试验结题会议,这将为aleniglipron于下半年启动三期试验铺路。后期试验的最高剂量尚不明确。这款小分子口服GLP-1药物预计最早在2028年才有望上市,届时将与诺和诺德的Wegovy口服剂型(多肽)以及礼来的orforglipron(小分子)展开竞争。ACCESS研究开放标签扩展研究的初步结果显示,aleniglipron可能具备同类最佳的疗效,同时也突显了较低2.5mg起始剂量在耐受性方面的优势。身体成分数据预计于下半年公布。根据ATTAIN-1三期试验数据,orforglipron减重效果中约27%来自瘦肌肉流失。
此外,下半年还将公布SWITCH研究(评估从已获批GLP-1注射剂转换用药)的结果,以及用于2型糖尿病适应症的相关数据。
后续催化剂
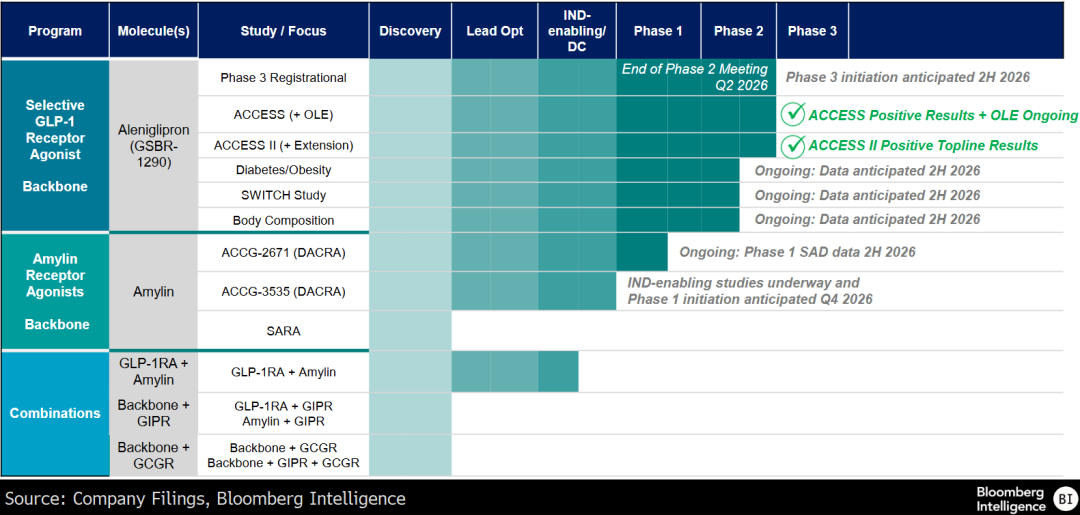
数据来源:公司文件、彭博行业研究
彭博行业研究(Bloomberg Intelligence)能够为企业客户提供与市场紧密相关的资讯与数据、分析与洞见,为您的企业策略提供可靠支撑,助您的团队保持领先地位。如需了解更多,欢迎点击“阅读原文”预约演示。
订阅生物制药研究双周报
想要实时获取BI关于生物制药行业的最新研究成果?请扫描文末二维码>关注彭博专业服务号>根据提示注册成会员。我们将持续为您发送精彩内容!

免责声明:本报告最初以英文发布,该翻译版本为彭博本地化团队和翻译服务公司的产品。如中、英文版本有任何出入或歧义,概以英文原版为准。
彭博Bloomberg享有对本文的独家版权,未经许可,请勿直接转载或用于其他商业用途,否则将追究法律责任。
点击 “阅读原文” ,预约彭博终端演示。

