3月268款新药获批临床!15款纳入特殊审评,涉及赛诺菲、辉瑞、华东医药

3月国内新药获批临床情况
3月共有268款新药获批临床(共计477个受理号),较上个月增加了123款;
3月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有164个,占比55%;
3月获批剂型主要为注射剂与片剂,分别有256个,133个。
全球获孤儿药/突破性/快速通道资格认定品种盘点
3月共有15款药物获孤儿药/突破性/快速通道资格认定。
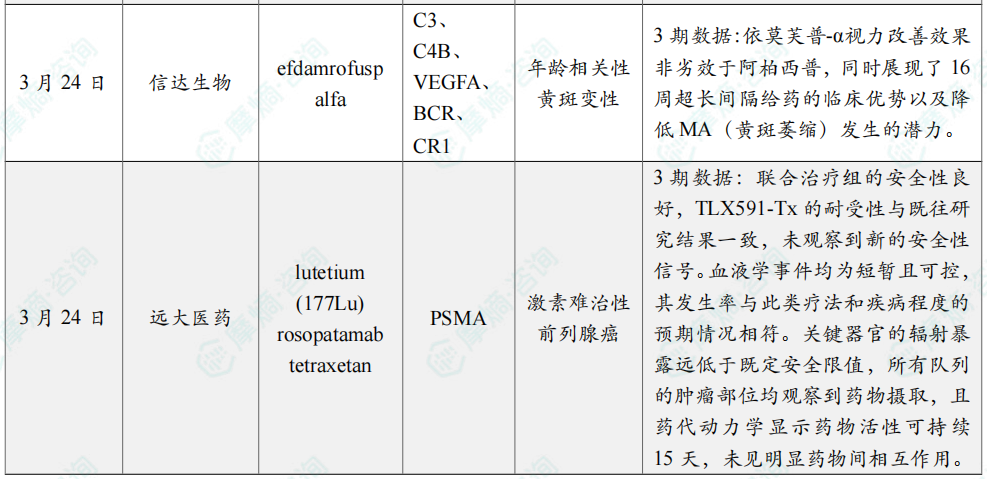
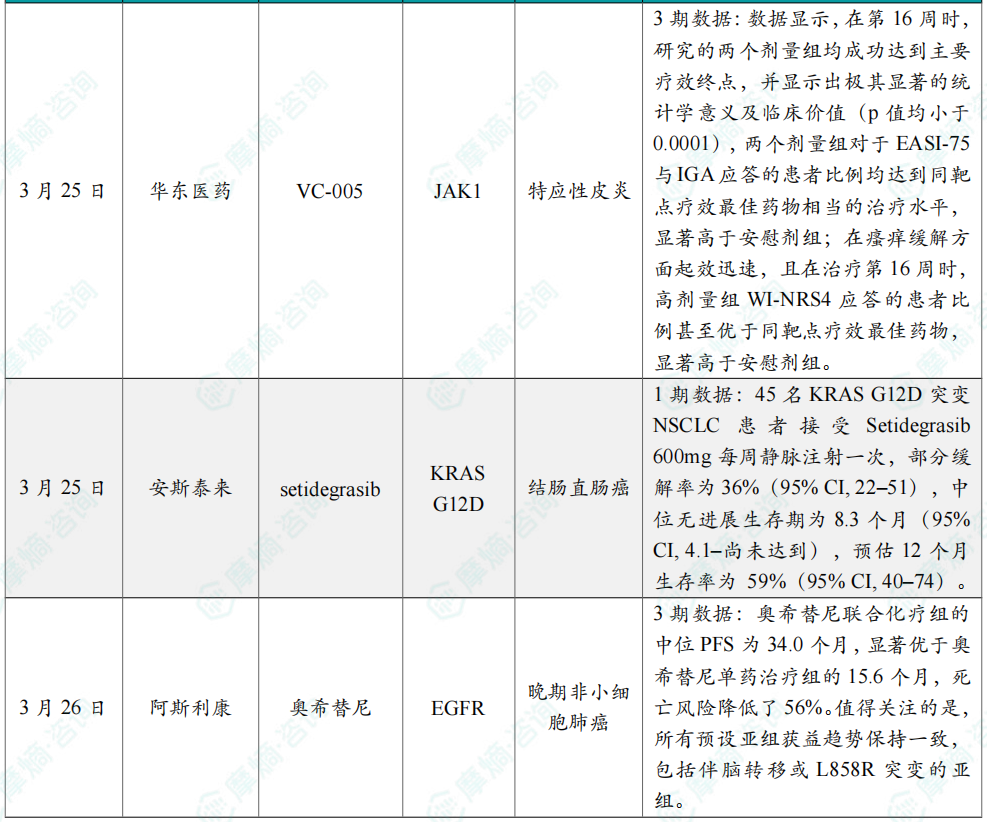
全球在研创新药积极/失败临床结果最新动态速递
凌科药业JAK1抑制剂治疗特应性皮炎3期临床取得积极结果;
罗氏BTK抑制剂芬布替尼又一项III期临床成功;
艾伯维IL-23抗体公布三期积极临床结果;
中国生物制药IDH1抑制剂III期研究成功。
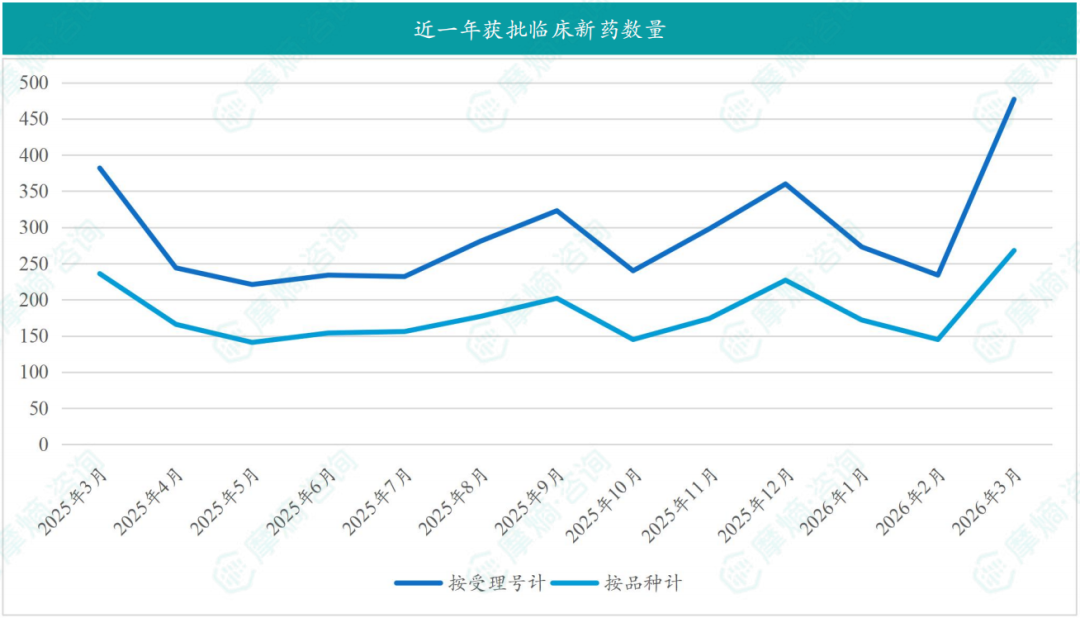
截图来源:摩熵咨询月报
本月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有164个,占比55%,消化系统与代谢药物获批数量也比较多,有55个。获批剂型主要为注射剂与片剂,分别有256个,133个。
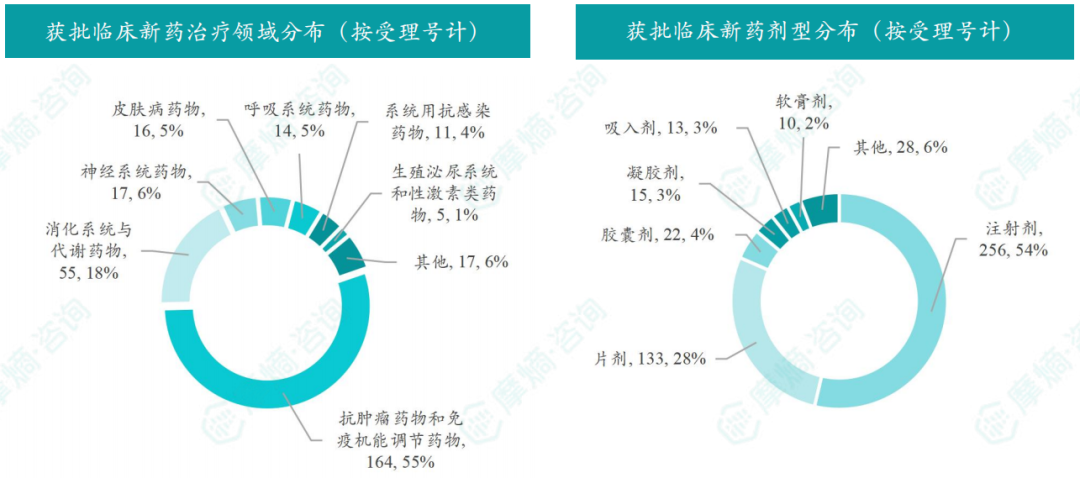
截图来源:摩熵咨询月报
2026年3月,国内医药市场迎来了5款创新药物的获批上市,涉及罗伐昔替尼片,用于中危-2或高危的原发性骨髓纤维化(PMF)、真性红细胞增多症后骨髓纤维化(PPV-MF)或原发性血小板增多症后骨髓纤维化(PET-MF)成年患者的一线治疗。
3月27日,阿斯利康宣布,特泽利尤单抗注射液(商品名:泰适卓,英文商品名:Tezspire)已获得中国国家药品监督管理局正式批准两项适应证:用于成人和12岁及以上青少年重度哮喘的维持治疗;与鼻用糖皮质激素联合使用治疗系统性糖皮质激素和/或手术治疗无法充分控制疾病的慢性鼻窦炎伴鼻息肉(CRSwNP)成人患者。特泽利尤单抗是全球首个且唯一获批靶向胸腺基质淋巴细胞生成素(TSLP),通过阻断上皮细胞因子作用于炎症级联反应顶端,治疗重度哮喘和慢性鼻窦炎伴鼻息肉的生物制剂。
除重度哮喘、慢性鼻窦炎伴鼻息肉以外,特泽利尤单抗还在开发用于慢性阻塞性肺疾病(COPD)和嗜酸性粒细胞性食管炎(EoE)。2021年10月,特泽利尤单抗获美国FDA授予治疗EoE的孤儿药资格。
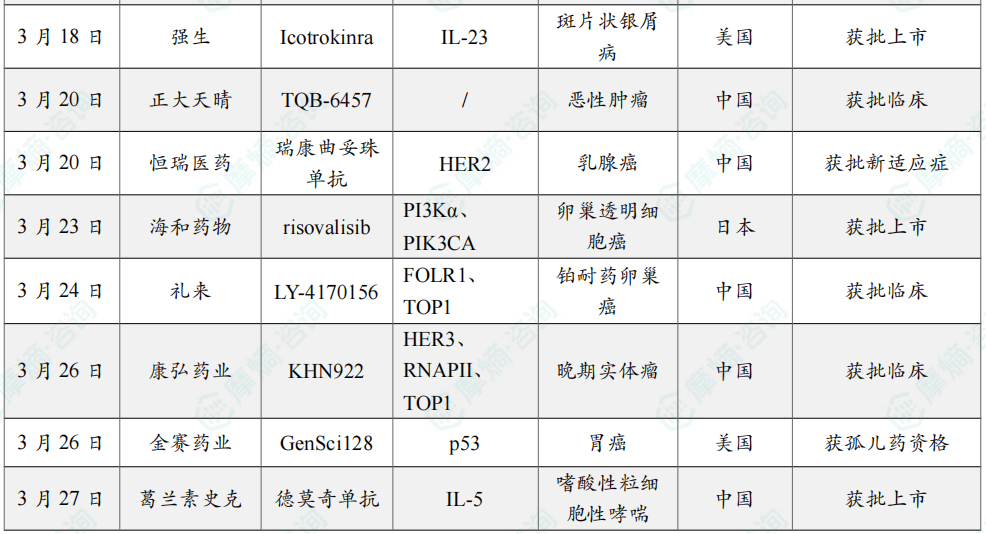
2026 年3月国内获批上市的新药
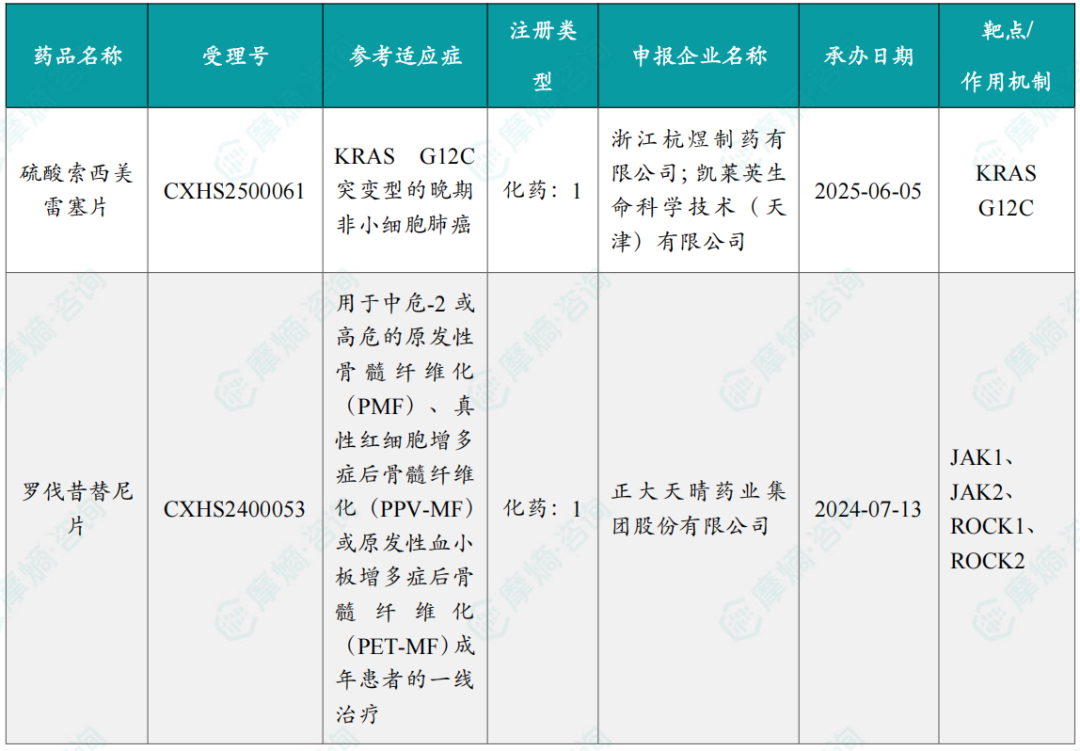
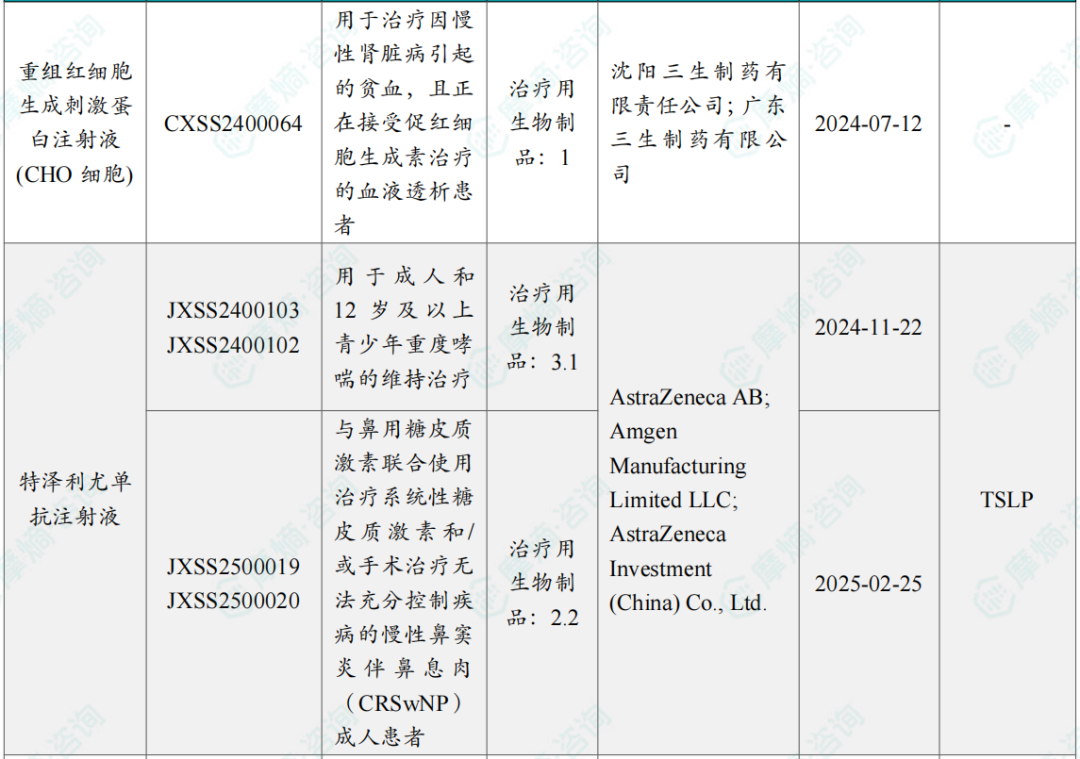
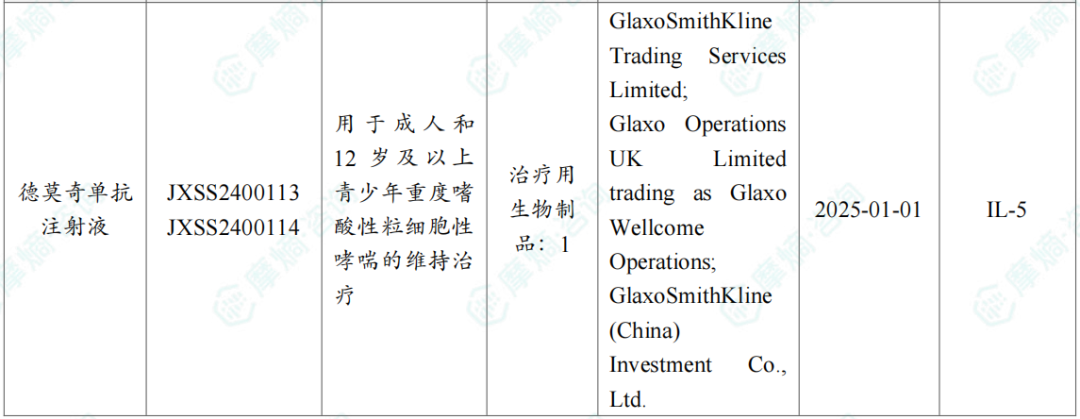
截图来源:摩熵咨询月报(完整数据识别文末二码下载查看)
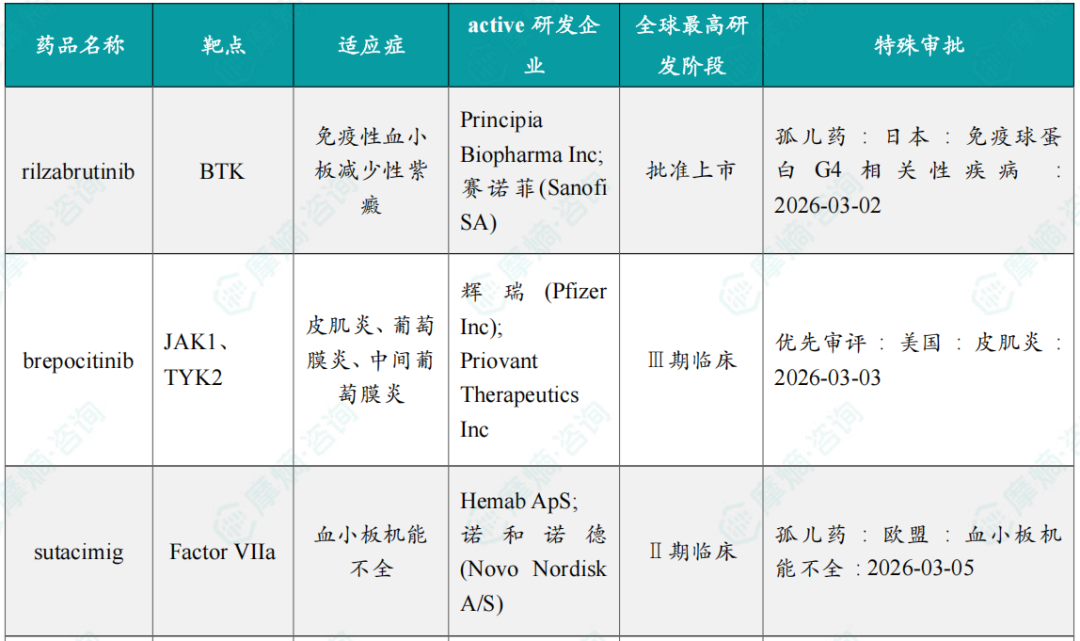
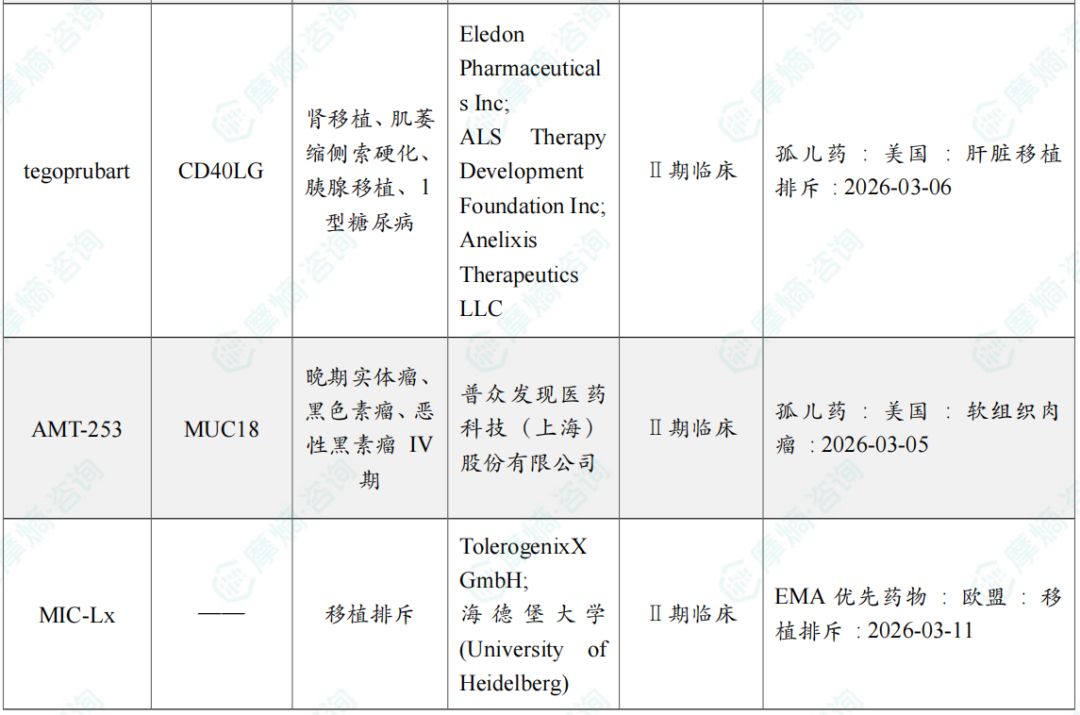
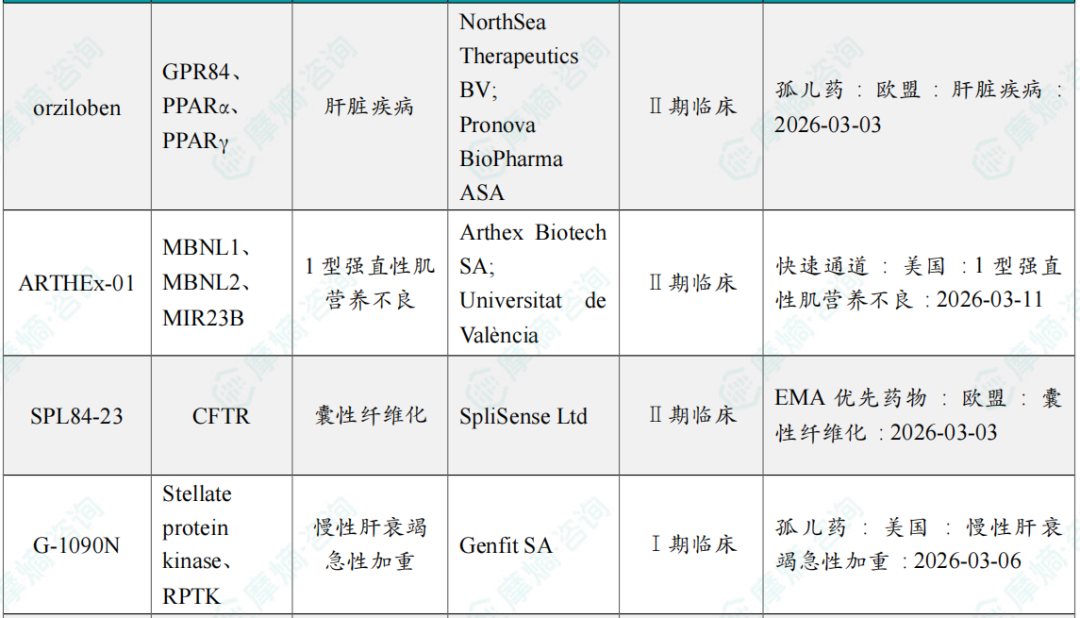
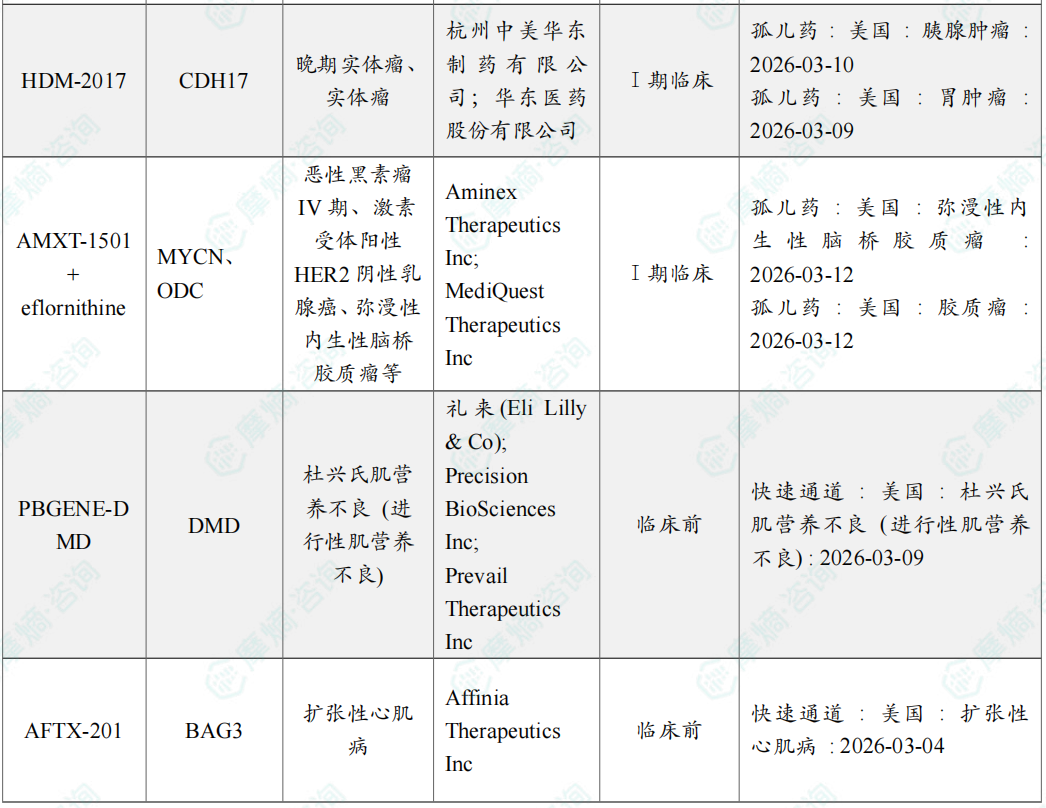
备注:完整数据识别文末二维码下载查看
期中分析结果显示,相比对照组,TQB3454可显著降低晚期胆道癌患者的疾病进展或死亡风险,显著延长患者的PFS和OS。其安全性数据与已知风险一致,未发现新的安全性信号。中国生物制药计划于今年开展的国际权威学术大会公布详细研究数据。
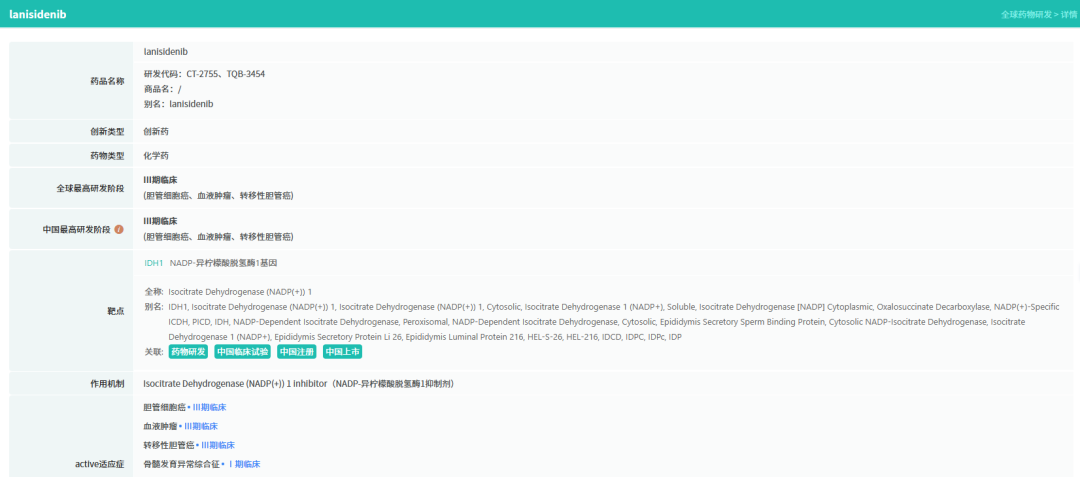
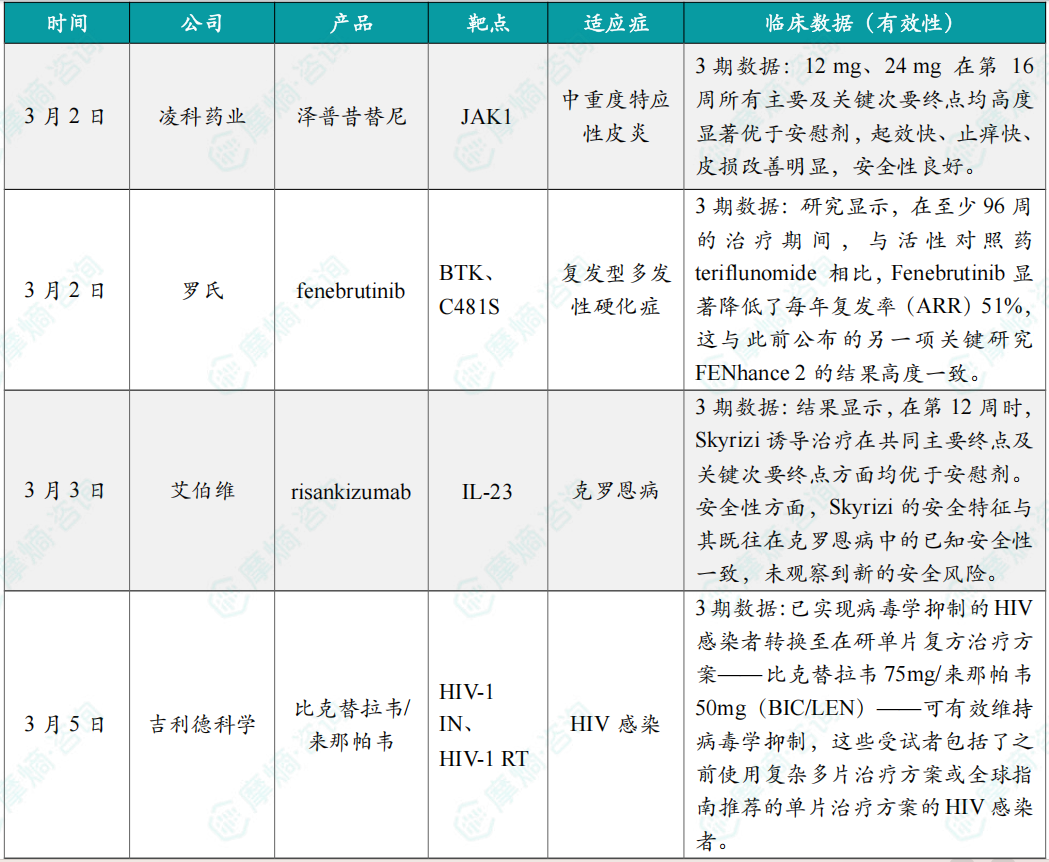
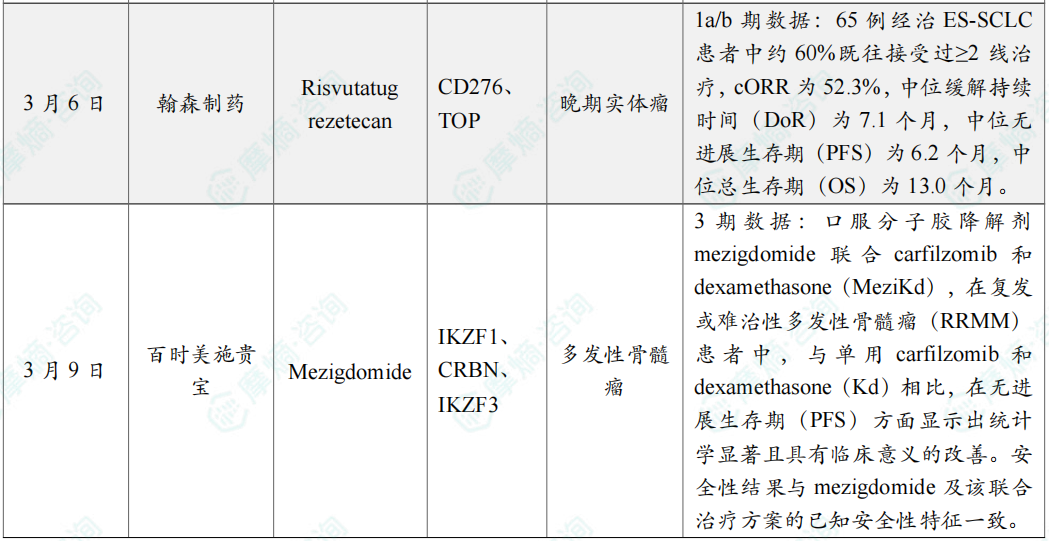
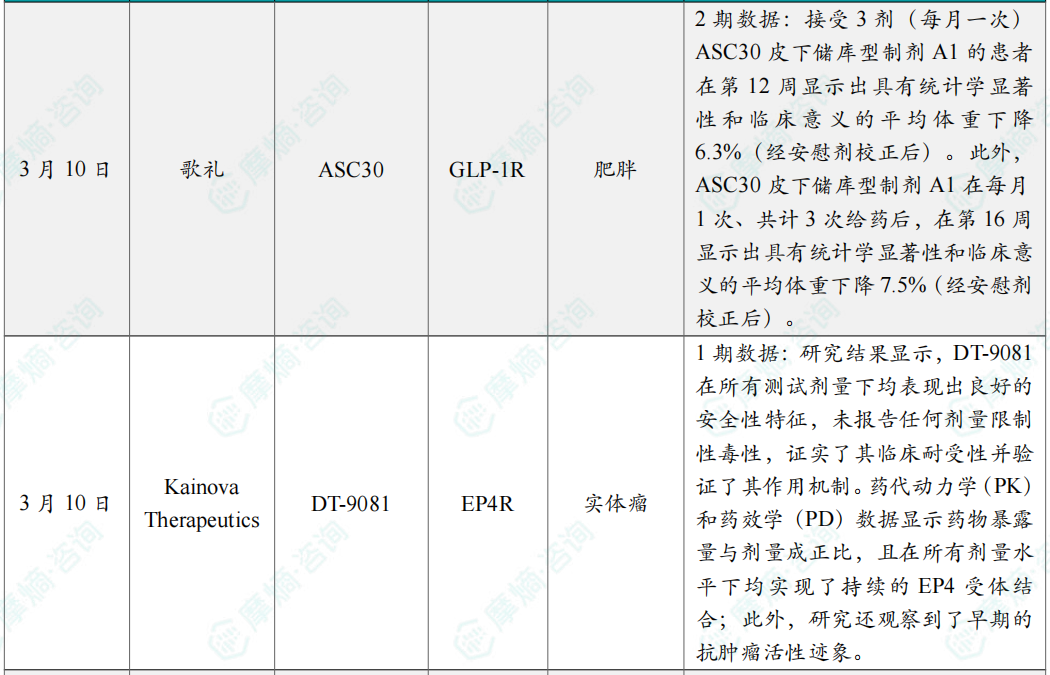
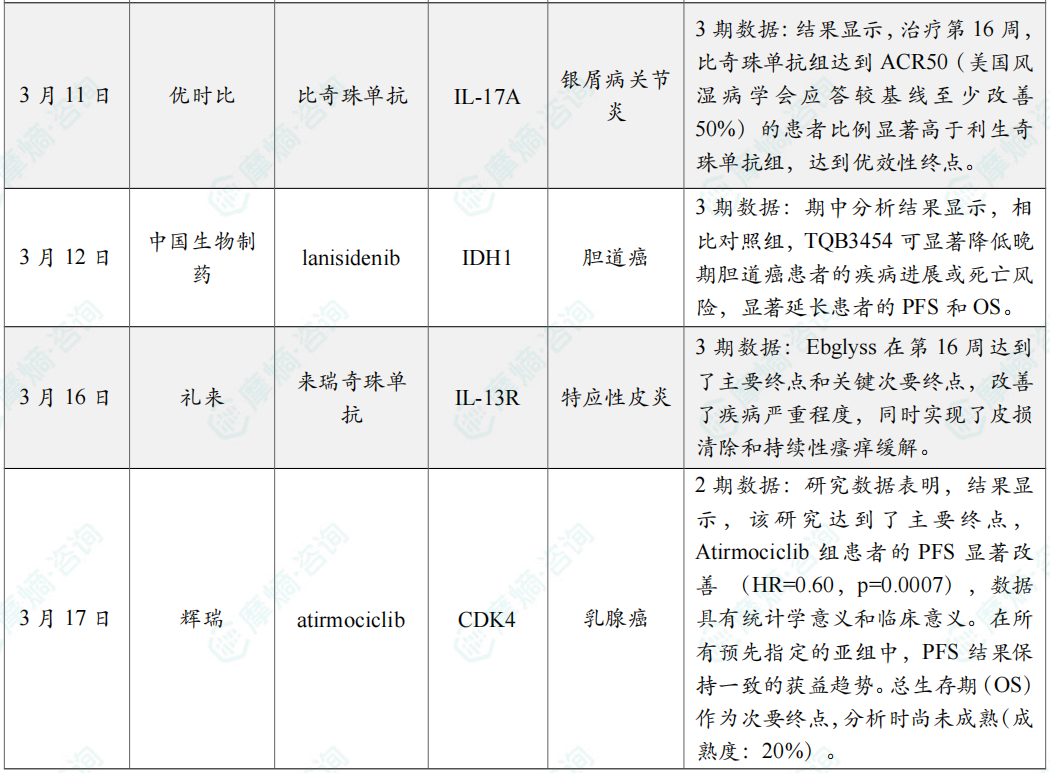
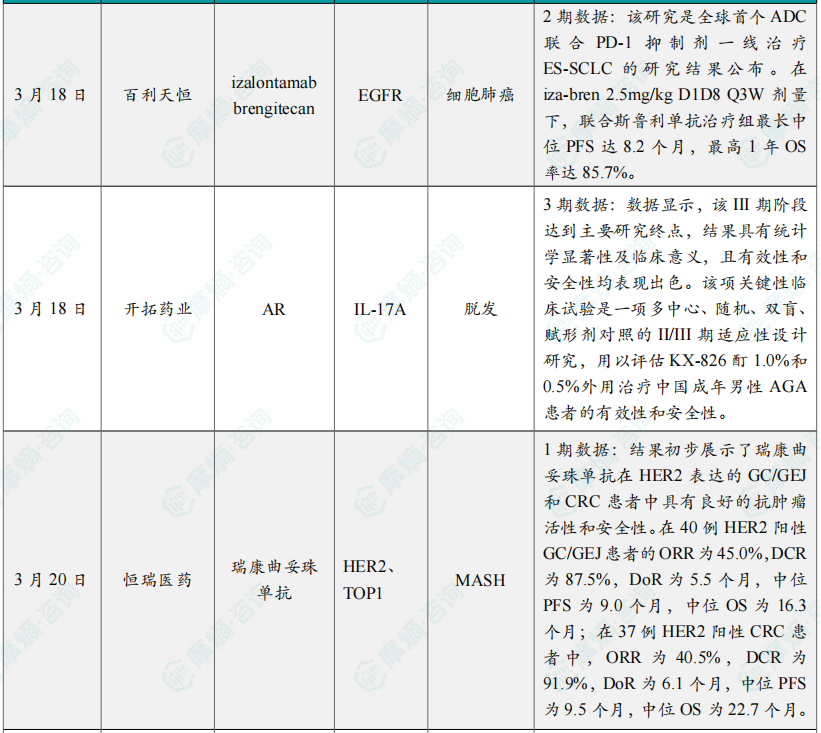
备注:完整数据识别文末二维码下载查看
3月3日,中国国家药监局药品审评中心(CDE)官网公示显示,礼来(Eli Lilly and Company)申报的3.1类新药来瑞奇珠单抗注射液上市申请获得受理。公开资料显示,来瑞奇珠单抗(lebrikizumab)是一款抗IL-13单抗,此前已经于2024年9月获美国FDA批准用于治疗中度至重度特应性皮炎成年和青少年患者,这些患者尽管使用局部药物治疗但病情仍无法得到控制。该产品能以每月一次的维持剂量为患者提供更便利的治疗。
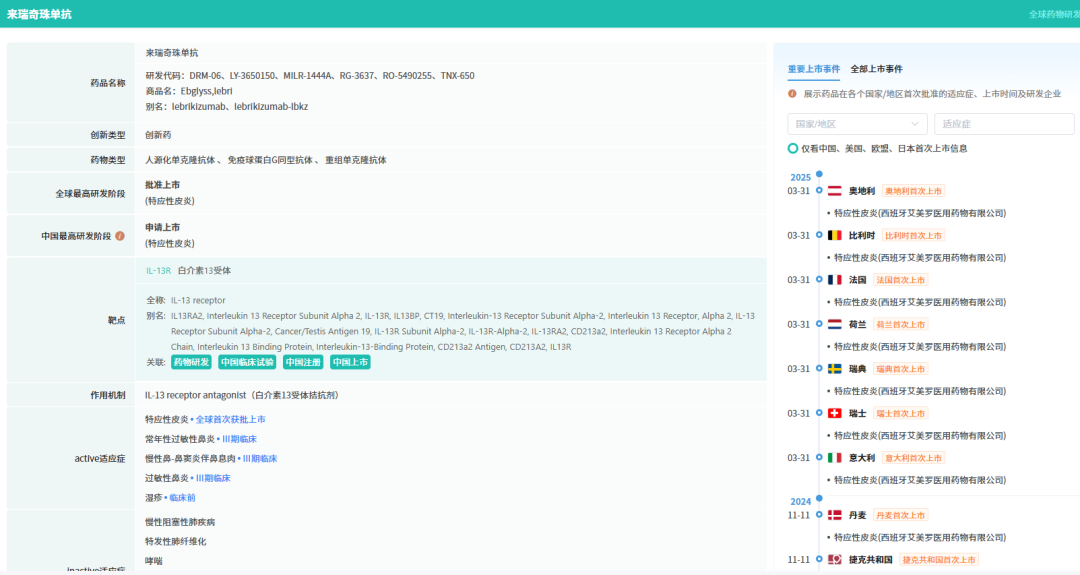
Lebrikizumab是一种单克隆抗体,能够以高结合亲和力和缓慢解离速率选择性地靶向并中和IL-13。Lebrikizumab与IL-13细胞因子结合的位置与IL-13Rα1/IL-4Rα异源二聚体中IL-4Rα亚基的结合位点重叠,从而阻止该受体复合物的形成并抑制IL-13信号传导。IL-13是特应性皮炎的一种主要细胞因子,驱动皮肤中的2型炎症循环,导致皮肤屏障功能障碍、瘙痒、皮肤增厚和感染。公开资料显示,礼来拥有在美国和除欧洲以外的全球其他地区开发和商业化lebrikizumab的独家权利。
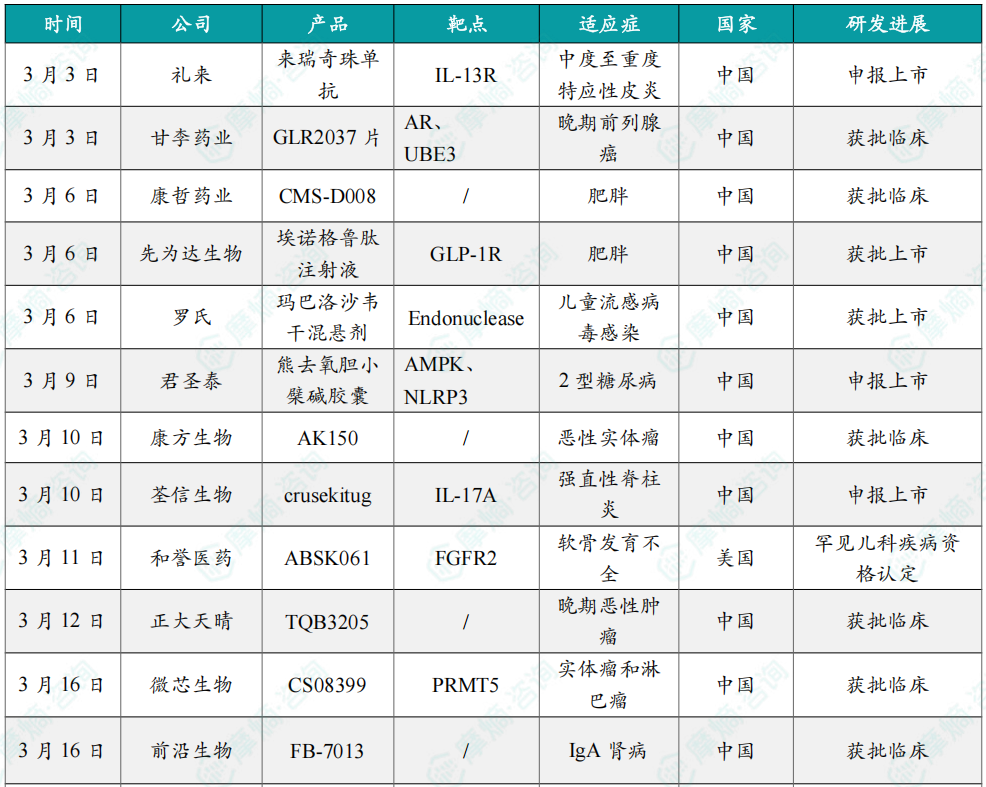
截图来源:摩熵咨询《2026年3月全球在研新药月报》

本报告在每月初定期发布,敬请期待

END
本文为原创文章,转载请留言获取授权
中国临床试验趋势与国际多中心临床展望-202505
近期更多摩熵咨询热门报告,识别下方二维码领取