仅10天!GSK新药又批新适应症


4月3日,GSK易适来®(德莫奇单抗)在中国获批用于治疗慢性鼻窦炎伴鼻息肉(CRSwNP),这是该药10天内的第二项适应症获批,3月25日,这款药获批用于成人和12岁及以上青少年重度嗜酸性粒细胞性哮喘的维持治疗。作为全球首款半年一次的IL-5超长效生物制剂,德莫奇单抗背靠2型炎症这一共同生物学基础,以同一分子实体快速覆盖哮喘和鼻息肉两大适应症。
疗效“够用”就行
易适来®此次获批新适应症,基于ANCHOR-1和ANCHOR-2两项III期研究。主要终点方面,鼻息肉评分(NPS)较安慰剂改善约0.7分,鼻塞评分改善约0.24分。横向对比度普利尤单抗(IL-4R抑制剂)在SINUS试验中的数据:NPS改善约2分,鼻塞改善约0.8分。专业期刊Med曾评论:德莫奇单抗在该适应症上的临床获益较其他生物制剂“有限”。

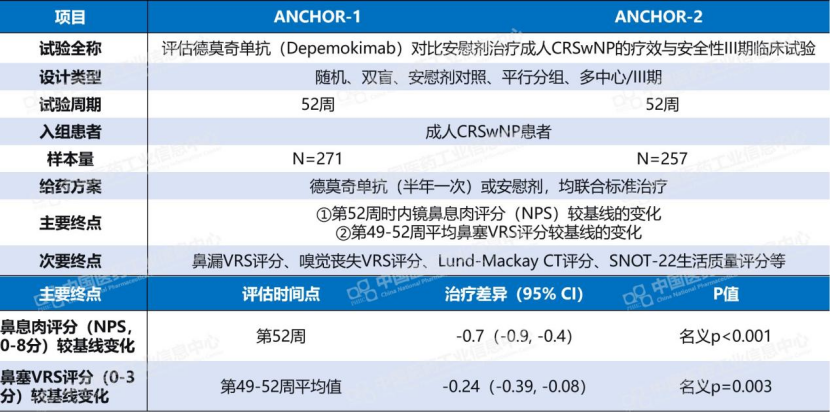
数据来源:Pharma ONE药物研发大数据平台-临床试验结果板块,中国医药工业信息中心

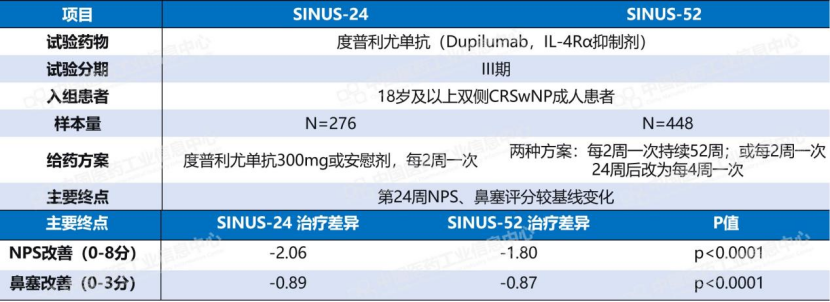
数据来源:Pharma ONE药物研发大数据平台-临床试验结果板块,中国医药工业信息中心
点击“阅读原文”获取更多数据
但获批逻辑成立的理由有二。其一,手术规避终点。德莫奇单抗组52周内未接受手术或疾病调节药物的比例为88%,安慰剂组83%(p=0.146)。尽管未达统计学显著性,但5个百分点的绝对差在真实世界中具有临床参考价值,尤其对于反复手术史且对再次干预抗拒的患者群体。其二,安全性相当,无新增风险信号。

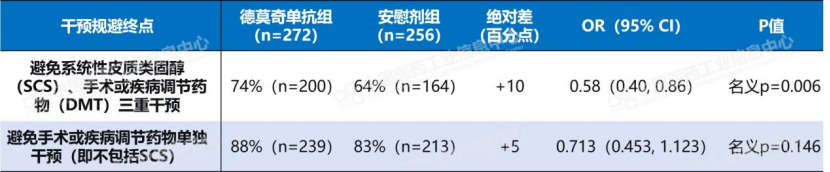
数据来源:Pharma ONE药物研发大数据平台-临床试验结果板块,中国医药工业信息中心
中国亚组数据值得关注。尽管疗效信号偏弱,但安全性信号明确,德莫奇单抗组严重不良事件发生率3%,安慰剂组14%。

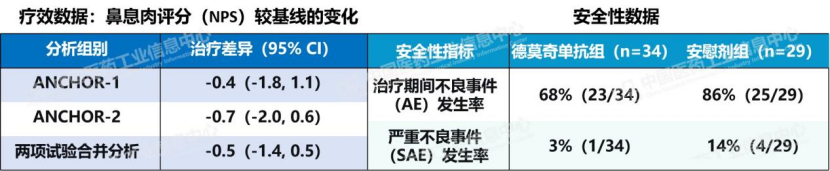
数据来源:Pharma ONE药物研发大数据平台-临床试验结果板块,中国医药工业信息中心
GSK的主动迭代与后来者
GSK在2023年财报中将德莫奇单抗定位为美泊利珠单抗接班产品。美泊利珠单抗美国核心专利2027年7月到期,中国正处于快速成长期,三大适应症(哮喘、EGPA、CRSwNP)去年2月纳入医保。GSK此时推出该产品,是用新药接棒老药,通过主动迭代完成患者转换。

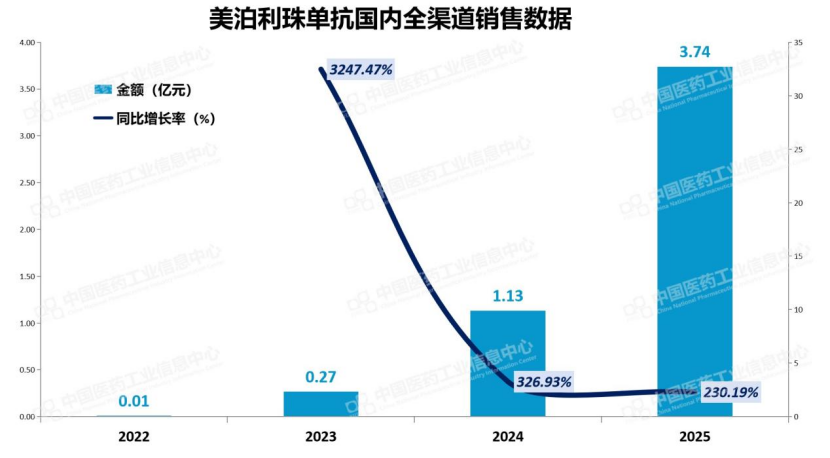
数据来源:PDB药物综合数据库-国内全渠道放大板块,中国医药工业信息中心
点击“阅读原文”获取更多数据
易适来®的优势是“半年一次”给药,比美泊利珠单抗(每月一次)和阿斯利康的本瑞利珠单抗(每8周一次)都长,而本瑞利珠单抗靠的是快速清除嗜酸性粒细胞拿下难治患者。
国内在研方面,恒瑞SHR-1703大概率也能做到半年一次,但德莫奇单抗已先手卡位。三生国健SSGJ-610则是每月一次,III期预计2027年完成。国产后来者就算复制了给药频率,还需要有差异化。
跨靶点来看,德莫奇单抗在CRSwNP上的真正对手是度普利尤单抗(IL-4R)。后者在避免手术的数据上更亮眼(手术比例从22.1%降至0.5%)。这意味着CRSwNP赛道未来是两线并行,IL-5靶点的“长效竞赛”与跨靶点的“疗效竞赛”。
从鼻到肺,再到罕见病:
2型炎症的合围之势
德莫奇单抗接连获批哮喘和CRSwNP,是GSK围绕“2型炎症”构建了气道全疾病谱矩阵。从解剖学看,CRSwNP属上气道疾病,哮喘属下气道疾病,两者在嗜酸性粒细胞介导的炎症机制上高度同源。德莫奇单抗通过阻断IL-5,实现对上、下气道2型炎症同步抑制。相当比例的CRSwNP患者合并哮喘,反之亦然。GSK将这一协同治疗价值传达给耳鼻喉科与呼吸科医生,将形成跨科室处方联动。
进一步审视GSK的呼吸与免疫管线,其布局已从单分子、单适应症开发,演进为“核心分子+多适应症扩展”的立体生态。根据Pharma ONE显示,除已获批的哮喘和CRSwNP外,德莫奇单抗还在III期阶段探索用于慢阻肺(ENDURA系列)、嗜酸性肉芽肿性多血管炎(OCEAN试验)以及高嗜酸性粒细胞综合征(DESTINY试验)。这些疾病均以2型炎症或嗜酸性粒细胞异常升高为核心特征。
在联合疗法层面,CRSwNP的标准治疗仍以鼻用糖皮质激素为基础,严重者辅以口服激素或生物制剂。GSK虽在鼻用激素领域已有布局(如糠酸氟替卡松鼻喷剂),但德莫奇单抗作为首个超长效IL-5单抗,在CRSwNP生物制剂领域建立了差异化优势。例如,对合并哮喘的CRSwNP患者(约占40-60%),德莫奇单抗联合吸入性ICS/LABA的“全身+局部”策略,可实现上下气道一体化管理。此外,GSK也在探索德莫奇单抗在手术前后及鼻窦支架等器械治疗中的最佳介入时机。
德莫奇单抗以依从性为支点,把IL-5赛道的竞争从“拼疗效”拉到了“拼频率”——半年一次,患者更容易坚持。
欢迎在评论区留下您的看法👏



