海和重磅药上市前夕,对手撤市!


4月3日,NMPA官网显示,上海海和药物研究开发股份有限公司、江苏宣泰药业有限公司申报的艾普美妥司他片上市申请获得受理,拟用于治疗不可手术的局部晚期或转移性经治上皮样肉瘤(Epithelioid Sarcoma, ES)患者。今年2月,该适应症已被纳入优先审评审批程序,是国产首款递交新药上市申请(NDA)的EZH1/2双靶小分子抑制剂。
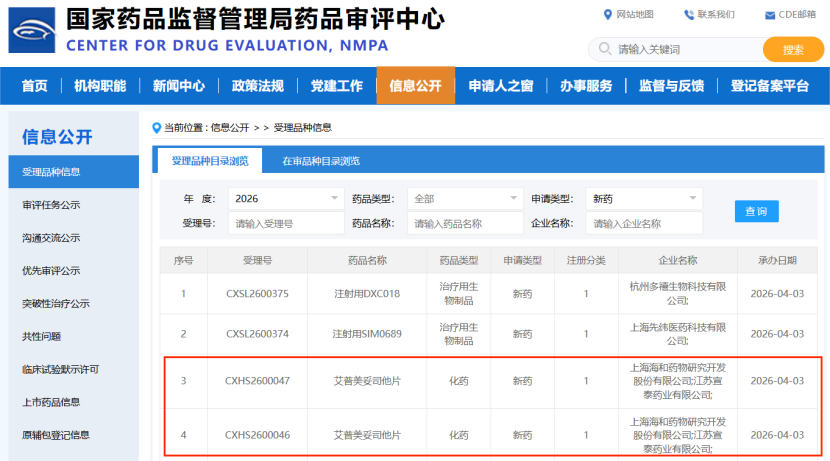

上市前夕,竞争对手“跑”了?

上皮样肉瘤(ES)是一种罕见的、侵袭性较强的软组织肉瘤,在所有软组织肉瘤中占比不足1%。从发病特点来看,其远端型多见于青壮年,近端型则好发于中老年人,且男性发病率高于女性。该肿瘤的核心分子特征为INI1(SWI/SNF复合体的关键亚基)表达缺失。ES恶性程度高、侵袭性强,极易发生转移。对于无法手术的局部晚期或转移性经治患者,传统化疗效果有限,可用的靶向治疗药物极少,临床需求极为迫切。
Pharma ONE药物研发大数据平台显示,目前针对上皮样肉瘤的治疗药物中,仅有一款获批上市——即Ipsen旗下Epizyme公司开发、和黄医药引进的EZH2抑制剂他泽司他(tazemetostat,商品名:达唯珂)。


上皮样肉瘤治疗药物
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
2021年8月,和黄医药与益普生旗下公司Epizyme达成战略合作,获得达唯珂在中国大陆、港澳台的研究、开发、生产及商业化权。2025年3月,达唯珂通过“附条件批准”在中国上市,用于治疗特定复发/难治性滤泡性淋巴瘤成人患者,成为国内首个也是唯一的EZH2抑制剂。2025年7月,达唯珂在中国开出首张处方,开始商业化销售,上市仅9个月后,被纳入首版《国家商业健康保险创新药品目录》。
遗憾的是,今年3月,和黄医药宣布已在中国内地、香港及澳门启动达唯珂撤市及产品召回程序,并同步停止所有正在进行的他泽司他的临床试验。原因是其全球开发方益普生(Ipsen)基于III期SYMPHONY-1研究中发现的继发性血液系统恶性肿瘤安全风险,评估认为风险超过临床获益,遂主动在全球撤市。至此,达唯珂从获批到撤市仅历时约一年,成为国内创新药附条件批准后因安全性问题退市的典型案例。
达唯珂的撤市为整个医药行业敲响了警钟,凸显了创新药研发的高风险性与不确定性。附条件批准在加速新药可及性的同时,也对上市后的安全性监测提出了更高的要求。

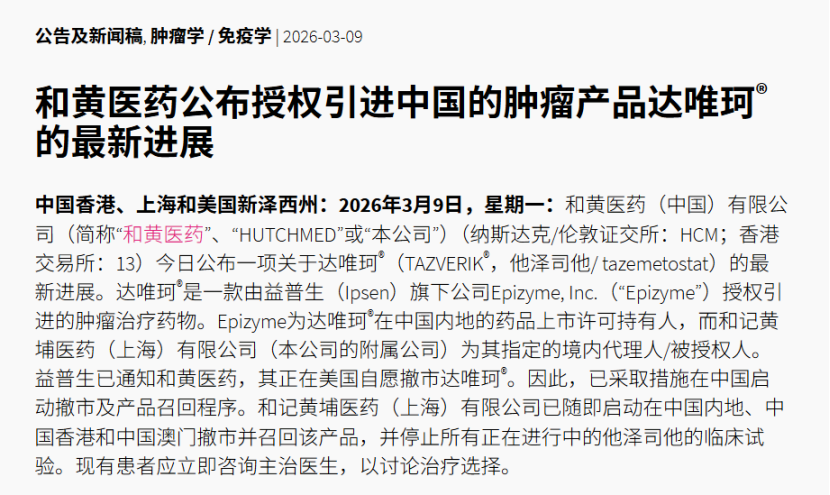
来源:和黄医药官网
EZH1/2赛道还有哪些玩家?
艾普美妥司他片(HH2853)是一款强效、高选择性的EZH1/2双靶小分子抑制剂,抑制EZH2的同时也有效抑制EZH1的补偿作用。临床前研究表明,HH2853能强效抑制细胞内H3K27me3水平,在体内外多种肿瘤模型中显示强效抗肿瘤作用,包括含有野生型或突变型EZH2的淋巴瘤细胞和含有SWI/SNF核心亚基突变(包括INI1缺失)的实体瘤细胞,且在同等剂量下,HH2853抗肿瘤活性与FDA批准的EZH2单靶抑制剂Tazemetostat相比更优。在经治ES患者中,HH2853展现出可观的疗效及良好的安全性,具有极大的临床应用潜力。
Pharma ONE药物研发大数据平台显示,除了晚期上皮样肉瘤外,艾普美妥司他片也在中国、美国拓展外周T细胞淋巴瘤、非霍奇金淋巴瘤、滤泡性淋巴瘤等适应症。
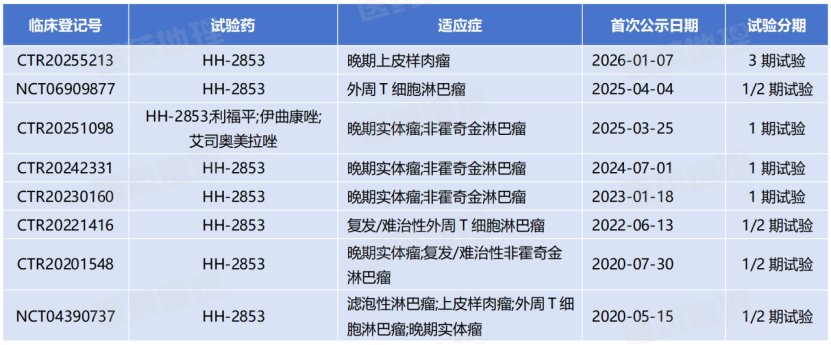
艾普美妥司他片(HH2853)全球临床研究一览
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
在EZH1/2双靶小分子抑制剂赛道,目前全球范围内仅有第一三共的伐美妥司他获批上市。除此之外,还有Constellation的托米美妥司他、Hanmi的HM-97594、和黄医药的HMPL-500等药物已经进入临床。

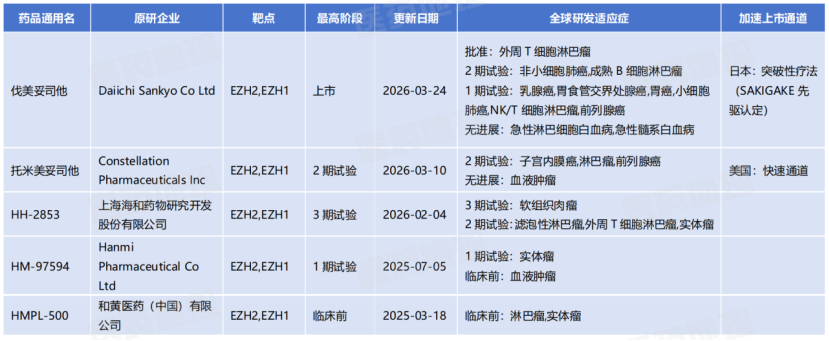
EZH1/2双靶小分子抑制剂在研药物一览
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心



