炎症性肠病合并抑郁、焦虑及其共病机制的研究进展

文献来源:中华炎性肠病杂志,2026年第10卷第1期
作者:吴志丰1,2 蔡旭1,2 金希亚1,2 柳涛1,2
作者单位:1南昌大学第一附属医院儿科;2江西省创烧伤及疼痛重点实验室
通信作者:柳涛
引用本文:吴志丰,蔡旭,金希亚,等. 炎症性肠病合并抑郁、焦虑及其共病机制的研究进展[J]. 中华炎性肠病杂志(中英文),2025,09(06):492-498.DOI:10.3760/cma.j.cn101480-20241126-00128


炎症性肠病(inflammatory bowel disease,IBD)是一种慢性免疫介导性疾病,具有显著的肠道-精神共病特征。临床研究显示,IBD患者抑郁与焦虑共病率分别达25.2%(95% CI:22.0%~28.5%)和32.1%(95% CI:28.3%~36.0%) [ 1 ],共病患者死亡率较普通IBD人群高4 ~ 6倍 [ 2 ]。值得注意的是,这种关联呈现显著的双向性。有研究表明,抑郁症患者发生克罗恩病(Crohn's disease,CD)和溃疡性结肠炎(ulcerative colitis,UC)的风险分别增加2.11倍( HR = 2.11,95% CI:1.65~2.70)和2.23倍( HR= 2.23,95% CI:1.92~2.60) [ 3 ];而抑郁/焦虑又显著增加IBD复发率、住院率及死亡风险 [ 4 ]。因此,国际IBD研究组织发布的共识建议将心理评估纳入IBD标准化诊疗路径 [ 5 ]。IBD共病抑郁、焦虑的潜在病理机制一直被广泛探讨。Lee等 [ 6 ]强调肠道菌群-肠-脑轴的关键作用,而神经炎症假说则聚焦于外周炎症通过血脑屏障诱发中枢改变 [ 7 ]。本文基于啮齿类动物模型研究,系统阐述免疫-炎症轴、菌群-代谢通路、肠脑神经调控等核心机制,并探讨靶向干预策略,为临床转化提供理论依据。

一、用于共病机制研究的动物模型
IBD共病抑郁、焦虑的机制研究高度依赖动物模型,其中啮齿类动物因其标准化的遗传背景和可操作性优势,成为解析IBD-精神共病机制的核心实验体系( 表1 )。
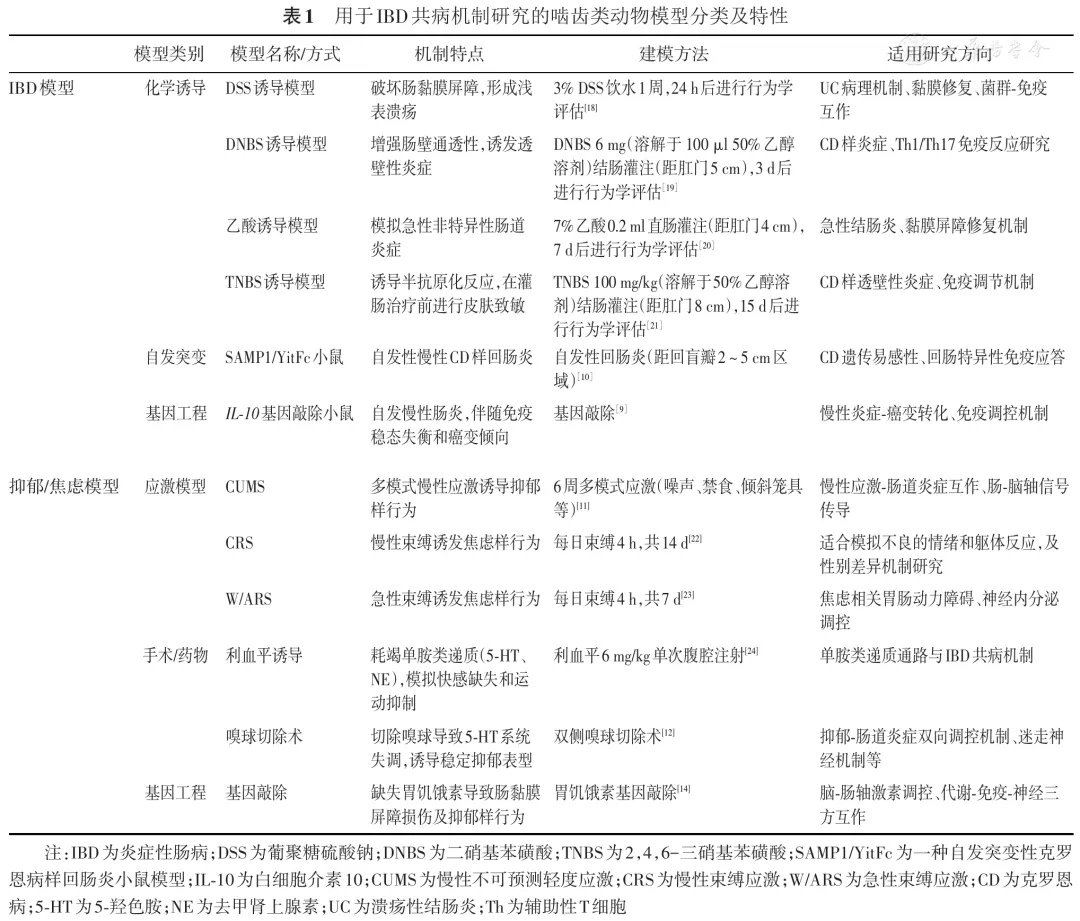
1.IBD动物模型:主要包括化学诱导和基因工程模型。化学诱导通过不同给药途径(口服/灌肠)和剂量调控,可模拟IBD的不同亚型和病程,应用最为广泛。如葡聚糖硫酸钠(dextran sulfate sodium,DSS)诱导模型主要破坏肠黏膜屏障,形成浅表溃疡,适用于模拟UC;而二硝基苯磺酸(dinitrobenzene sulfonic acid,DNBS)则诱发透壁性炎症,更符合CD病理特征 [ 8 ]。此外,基因工程模型则聚焦特定免疫分子,如白细胞介素10(interleukin-10, IL-10)基因敲除小鼠可自发出现慢性肠道炎症,并伴随肠腺癌转化倾向 [ 9 ]。值得注意的是,除上述两类模型外,还存在无需人工干预的自发性模型,SAMP1/YitFc小鼠便是典型代表。该模型无需化学诱导或基因改造,可自然发生CD样回肠炎,能稳定模拟CD特征性的慢性回肠病变,是研究CD慢性病程的重要工具 [ 10 ]。
2.抑郁/焦虑动物模型:慢性不可预测轻度应激(chronic unpredictable mild stress,CUMS)抑郁模型 [ 11 ]采用多模式应激,能较好地再现人类面对慢性压力时的心理行为改变;而束缚应激焦虑模型适合模拟不良的情绪和躯体反应,但需注意性别差异。此外,手术造模以嗅球切除术 [ 12 ]为代表,虽能诱导稳定的抑郁样行为,但动物死亡率高;而药物造模则通过给予利血平等神经递质调节剂 [ 13 ],能较好地在病理分子层面构建抑郁模型。再者,如胃饥饿素基因敲除小鼠被证明可出现肠道炎症和抑郁 [ 14 ],但其机制验证仍需更多研究支持。
除了啮齿动物模型外,DSS诱导的斑马鱼模型可呈现肠道炎症与焦虑行为 [ 15 ];而犬IBD模型同样会出现精神状态下降 [ 16 ],但这些研究都缺乏对机制的深入探讨。目前仍缺少可以完全复制人类的模型,不同动物模型各有优势,且之间存在分子或表型差异。正如Wen等 [ 17 ]总结的一样,豚鼠因其神经-免疫交互特性适用于IBD机制解析;而猪模型则在营养代谢研究中有独特优势。研究者应依研究目的、机制层级及临床转化需求选择合适的模型,如 表1 所述 [ 9 , 10 , 11 , 12 , 14 , 18 , 19 , 20 , 21 , 22 , 23 , 24 ]。

二、IBD引起抑郁、焦虑的机制研究
IBD合并抑郁、焦虑的可能机制涉及以下五个方面,见图1 。
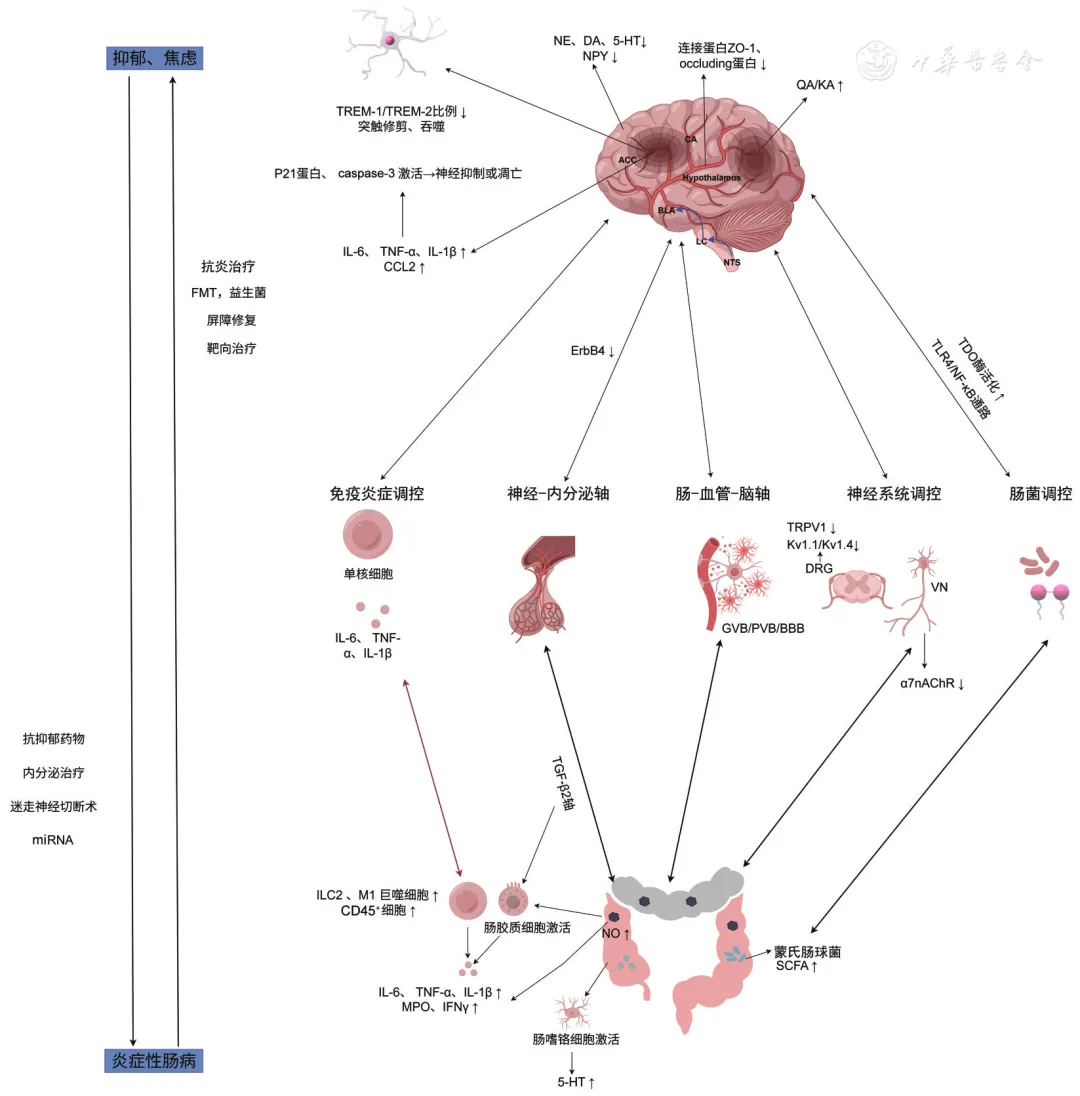
图1 炎症性肠病共病抑郁、焦虑机制及治疗策略图
注:miRNA为微小RNA;FMT为粪菌移植;TREM-1和TREM-2为髓系细胞表面受体1/2;caspase3为胱天蛋白酶3;IL-6为白细胞介素6;TNF-α为肿瘤坏死因子α;IL-1β为白细胞介素1β;CCL2为趋化因子2;NE为去甲肾上腺素;DA为多巴胺;5-HT为5-羟色胺;NPY为神经肽Y;ErbB4为Erb-b2受体酪氨酸激酶4;ACC为前扣带回皮质;CA为海马;hypothalamus为下丘脑;BLA为基底外侧杏仁核;LC为蓝斑;NTS为孤束核;QA为喹啉酸;KA为犬尿喹啉酸;TDO为色氨酸2,3 -双加氧酶;TLR4为toll样受体4;NF-κB为核因子κB;GVB为肠-血管屏障;PVB为脉络丛血管屏障;BBB为血脑屏障;TRPV1为瞬时受体电位香草醛亚家族1;Kv1.1和Kv1.4分别为电压门控钾离子通道亚型1.1和1.4;DRG为背根神经节;VN为迷走神经;α7nAChR为α7烟碱乙酰胆碱受体;ILC2为Ⅱ型固有淋巴细胞;MPO为髓过氧化物酶;IFNγ为干扰素γ;TGF-β2为转化生长因子β2;NO为一氧化氮;SCFA为短链脂肪酸
1.肠-脑免疫炎症级联网络:IBD与抑郁、焦虑具有相似的免疫炎症特征。研究表明,在结肠炎缓解期,诱导性一氧化氮合酶(iNOS)介导的一氧化氮(NO)爆发及促炎因子异常蓄积不仅直接损伤肠上皮屏障,还可激活脑内小胶质细胞,引发神经炎症相关的抑郁或焦虑表型 [ 25 ]。此外,肠神经系统内的肠胶质细胞是启动和维持神经炎症反应的关键参与者,Li等 [ 26 ]发现UC小鼠肠胶质细胞的持续活化,可释放促炎介质,诱发抑郁和焦虑样行为。除了肠道炎症机制外,外周免疫细胞及炎症的迁移在肠-脑交互中发挥枢纽作用。Cluny等 [ 27 ]发现外周血整合素α4β7 +单核细胞通过趋化中性粒细胞浸润脑血管系统,显著提升脑内IL-1β和趋化因子2(CCL2)水平,进而触发焦虑样行为。在中枢神经系统层面,IL-6、肿瘤坏死因子α(tumor necrosis factorα,TNF-α)和IL-1β等炎症因子可引起炎症级联反应,这些因子在海马体区域的异常蓄积既可激活p21蛋白抑制神经发生 [ 28 ],又能通过胱天蛋白酶3(caspase-3)通路触发神经元凋亡 [ 29 ]。此外,小胶质细胞作为大脑的先天免疫细胞,可通过突触修剪、吞噬及调节屏障修复等机制在IBD精神合并症中发挥重要作用 [ 30 ]。Wu等 [ 31 ]研究发现,在前扣带皮质中小胶质细胞的髓系细胞触发受体2(TREM-2)激活即TREM1/TREM2比例失衡是抑郁发生的关键环节,而靶向消融后可有效阻断行为异常。总的来看,炎症机制涉及:(1)肠道局部炎症向全身的扩散;(2)免疫-神经系统的交互应答;(3)中枢与外周炎症信号的协同作用等。因此,靶向调控肠脑轴的免疫-炎症机制可能成为改善IBD及其精神共病的潜在治疗策略。
2.肠道微生物群及其代谢产物的调控网络:肠道微生物群在调节行为、情绪和认知功能方面发挥着重要作用。研究发现,IBD共病抑郁焦虑患者的肠道菌群呈现特征性改变,其群落丰富度和多样性显著区别于单纯IBD或精神疾病患者 [ 32 ],将IBD共病患者菌群移植至健康小鼠,可诱发肠道炎症与抑郁共病 [ 33 ]。另外,蒙氏肠球菌可通过荚膜多糖抑制小鼠结肠和海马神经肽Y(NPY)的表达,从而介导肠道炎症共病焦虑抑郁 [ 34 ]。值得注意的是,菌群失调不仅通过免疫激活促进神经炎症,还存在独立于免疫的"菌群-脑"直接作用通路。Vicentini等 [ 35 ]证实,如果将DSS小鼠的盲肠内容物移植到无菌或抗生素治疗的小鼠中,受体小鼠不会出现任何结肠或神经炎症,但可表现出类似的行为改变。在代谢层面,短链脂肪酸(short chain fatty acid,SCFA)的失衡与色氨酸代谢异常构成关键调控节点。首先,SCFA水平下降可激活toll样受体4/核因子κB(TLR4/NF-κB)通路,通过神经炎症途径诱导抑郁行为 [ 36 ]。其次,IBD诱导的色氨酸2,3-双加氧酶(tryptophan 2,3-dioxygenase,TDO)过度活化,促使色氨酸代谢向犬尿氨酸途径偏移,导致神经毒性喹啉酸(QA)蓄积与保护性犬尿喹啉酸(KA)减少,该失衡状态可通过TDO抑制剂干预显著改善抑郁焦虑表型 [ 37 , 38 ]。这些研究共同构建了"微生物组成改变→代谢紊乱→免疫/非免疫信号传递→中枢失调"的调控框架,为靶向菌群的重建策略(如益生菌干预、代谢产物调控、菌群移植优化)提供了理论依据,有望成为IBD精神共病恶性循环的新突破口。
3.肠脑屏障系统的调控机制:肠道与中枢屏障共同构成"肠-脑"双向防御体系,血脑屏障紧密连接的破坏促进炎症因子和免疫细胞的细胞旁途径流入。在IBD共病抑郁的大鼠中,Wadie等 [ 39 ]发现脑组织中紧密连接蛋白ZO-1、occludin表达量下降约50%,提示结肠炎症通过破坏血脑屏障完整性损害神经元微环境,参与抑郁发生。同样,使用醋酸诱导的结肠炎模型也能检测到血脑屏障通透性显著增加 [ 20 ],尤其是在脑实质的脑室周围器中,如果靶向增强紧密连接蛋白表达可同步修复肠道与脑屏障功能,显著缓解抑郁焦虑样行为 [ 40 ]。有趣的是,肠-血管屏障(gut-vascular barrier,GVB)在精神共病中表现出矛盾作用,虽然肠道炎症通常伴随GVB破坏并引发焦虑行为,但Carloni等 [ 41 ]发现即使保持GVB完整的基因小鼠同样会出现短期记忆丧失和焦虑样行为,这表明IBD相关行为和认知改变并非完全由炎症引起,可能还涉及GVB/脉络丛血管屏障(PVB)的动态调控机制。总的来说,屏障保护机制为IBD精神共病提供创新治疗思路,即通过屏障系统联合修复策略,阻断肠源性炎症因子及免疫细胞的中枢渗透,或能实现肠道与精神症状的协同改善。
4.内分泌网络调控:肠道是机体重要的内分泌器官,其肠道嗜铬细胞(enterochromaffin cell,EC)通过5-羟色胺(5-hydroxy tryptamine,5-HT)信号系统可实现"肠-脑"双向调控。Bayrer等 [ 42 ]揭示EC细胞功能紊乱可诱发焦虑行为,而阻断5-HT信号传导可逆转该表型。此外,神经递质与微生物代谢产物存在交叉调控,表面活性素通过重塑菌群结构促进脑内5-HT/去甲肾上腺素合成,间接缓解抑郁焦虑 [ 43 ];而植物乳杆菌则可直接上调IBD模型小鼠脑内5-HT、去甲肾上腺素、多巴胺水平,实现肠道炎症与抑郁行为的同步改善 [ 44 ]。从神经-内分泌轴来看,下丘脑-垂体-肾上腺(HPA)轴-性激素调控网络呈现性别特异性特征。雌激素受体β缺失通过双重机制促进共病发生:(1)改变肠道菌群组成增加结肠炎易感性;(2)下调应激状态下丘脑Erb-b2受体酪氨酸激酶4(ErbB4)表达,通过HPA轴过度活化诱发焦虑 [ 45 ]。因此,HPA轴与激素的调节可能与多种因素交叉调控IBD共病抑郁焦虑,其在双向调控肠道与神经系统中扮演重要的角色,通过多层级干预模式有望突破当前IBD精神共病的治疗瓶颈。
5.神经环路的调控机制:IBD相关精神共病的神经机制涉及外周-中枢信号传导通路的系统性重塑。神经影像学显示IBD患者内侧前额叶皮质等脑区出现皮质厚度改变 [ 46 ]及γ-氨基丁酸(GABA)/谷氨酰胺代谢紊乱 [ 47 ]。在关键脑区调控层面,海马与导水管周围灰质的谷氨酸能系统失衡尤为突出。Wang等 [ 18 ]发现,海马区谷氨酸代谢受体1过度激活可通过谷氨酸能突触异常兴奋诱导结肠炎小鼠的焦虑样行为;而腹外侧导水管周围灰质谷氨酸能神经元活动减弱则与抑郁表型相关,Α-氨基-3-羟基-5-甲基-4-异恶唑丙酸受体(AMPA)激动剂可通过增强突触传递发挥抗抑郁作用 [ 48 ]。此外,研究者发现DSS诱导结肠炎加剧了结肠投射传入神经元持续的自发活动,从而引起大鼠的腹部不适和焦虑以及抑郁样行为,其可能与背根神经节瞬时受体电位香草醛亚家族1(TRPV1)通道上调、Kv1.1/Kv1.4钾通道下调相关 [ 49 ]。值得注意的是,迷走神经传入通路是构成肠-脑信号传递的核心桥梁。Chen等 [ 50 ]的研究表明DSS诱导的结肠炎症导致双侧迷走神经传入神经激活以传递外周炎症信号,然后通过"孤束核-蓝斑-基底外侧杏仁核"去甲肾上腺素能环路导致焦虑,而化学遗传学沉默或迷走神经切断可阻断该过程。基于上述机制,通过靶向特定的离子通道或神经通路,或许能为IBD精神共病的疗法提供新方向。

三、抑郁、焦虑影响IBD的机制研究
如图1 所示,应激及心理压力也可以通过脑-肠轴加重IBD并且独立激活实验性结肠炎。Ghia等 [ 12 , 51 ]报道迷走神经-胆碱能系统在调控中起枢纽作用,发现抑郁小鼠通过抑制副交感神经功能,降低α7烟碱乙酰胆碱受体(α7nAChR)介导的抗炎信号,显著提升结肠炎易感性,而三环类抗抑郁药通过恢复胆碱能张力可有效缓解肠道炎症。在内分泌系统层面,慢性应激通过糖皮质激素-转化生长因子β2(TGF-β2)轴双重破坏肠道神经系统:一方面诱导肠胶质细胞向促炎表型分化,经集落刺激因子1(CSF-1)信号激活单核细胞/TNF依赖性炎症;另一方面通过TGF-β2抑制神经元成熟,导致乙酰胆碱分泌不足和肠道动力障碍 [ 9 ]。另外,精神应激通过HPA轴-细胞因子网络重塑免疫微环境,焦虑激活HPA轴促使Ⅱ型固有淋巴细胞(ILC2)异常分泌IL-5/IL-13,加重结肠炎 [ 23 ];而抑郁则通过干扰素调节因子5(IRF5)驱动的M1型巨噬细胞极化,促进干扰素γ(IFNγ)、IL-6等促炎因子释放 [ 52 ],或诱导肠道CD45 +免疫细胞浸润、髓过氧化物酶(MPO)活性加重结肠炎症 [ 53 ]。精神共病与IBD存在双向恶化循环:精神应激→神经/内分泌失调→免疫激活/屏障损伤→肠道炎症加重→中枢功能恶化。针对此环路,精神药物(如5-羟色胺再摄取抑制剂、三环类抗抑郁药)在动物模型中展现出多靶点干预潜力,也为临床干预提供了新思路。

四、总结与展望
IBD患者除抑郁、焦虑外,常伴睡眠障碍、创伤后应激等症状,显著降低生活质量 [ 54 , 55 ]。然而,IBD类型与精神症状的关联仍存争议:有研究提示UC与焦虑存在因果关系,而CD则无显著关联 [ 56 ];但亦有证据表明CD患者的抑郁或焦虑患病率高于UC [ 1 ]。此外,抑郁症的遗传易感性与IBD的发生相关,而女性因雌激素信号与应激敏感性等因素,精神共病发生率较男性高30% [ 57 ],但性别差异的分子通路仍需深入探讨。当前IBD共病抑郁/焦虑的治疗采用"药物-心理"综合策略—抗炎制剂联合新型抗抑郁药(如5-羟色胺再摄取抑制剂)可同步改善肠道炎症与神经递质失衡,而正念疗法等心理干预能有效调节HPA轴过度激活,但临床实践面临困境 [ 58 , 59 ]。近些年,研究者们发现靶向药物如抗TNF-α药物虽能改善IBD患者的抑郁症状,但精神共病本身可能增加患者停药风险 [ 60 , 61 ]。此外,动物实验表明,miR-124可抑制抑郁小鼠的炎症并改善抑郁样行为 [ 62 ]。靶向miRNA如ABX-464(靶向miR-124的调节剂)在Ⅱa期临床试验中显示出对中重度UC患者的症状缓解潜力 [ 63 ],可能为共病治疗提供新方向。
然而,当前研究面临以下问题:(1)机制解析不足:肥胖、性别、遗传等混杂因素对IBD与精神共病交互作用的影响尚未明确;(2)转化医学缺口:多数机制研究停留于动物模型,缺乏临床验证和临床应用转化;(3)治疗策略局限:现有治疗以症状控制为主,缺乏针对共病核心通路的精准干预。总之,IBD作为一种心身疾病,心身双向管理对于改善患者的预后至关重要。未来研究需进一步探索机制,为共病治疗提供更多潜在靶点。
来源:中华炎性肠病杂志