礼来Orforglipron获批!且看非肽类小分子GLP-1赛道风云录
发布时间:2026-04-07来源:药事纵横
与肽类GLP-1药物相比,非肽类小分子GLP-1R激动剂具备口服生物利用度高、给药方便等优势,是2型糖尿病和肥胖症治疗领域颇具前景的新方向。2026年4月1日,礼来宣布Orforglipron获得FDA上市批准,Orforglipron成为全球首款非肽类小分子GLP-1R激动剂。面对这一潜力巨大的赛道,国内外药企如何布局?哪些品种进展最快?本文将梳理研发进展靠前的代表性品种。1、Danuglipron与Lotiglipron:从领跑到折戟
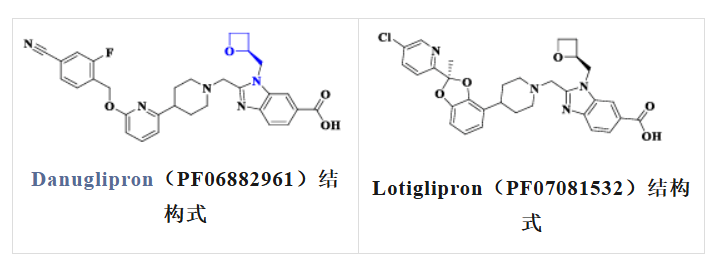
目前全球在研的非肽类小分子GLP-1R激动剂主要分为两大技术路线:辉瑞Danuglipron代表的结构类型和礼来Orforglipron代表的结构类型。从布局的专利来看,多数企业选择了辉瑞Danuglipron路线。所以,我们先从Danuglipron(PF06882961)和Lotiglipron(PF07081532)谈起。Danuglipron由辉瑞开发,在动物模型中展现出显著的降糖、减重及心脏保护效果。Ⅱ期临床试验进一步验证了其疗效:在2型糖尿病及肥胖人群中,可剂量依赖性地显著降低糖化血红蛋白和体重。但突出的胃肠道不良反应(恶心、呕吐、腹泻)成为硬伤,高剂量组停药率超过70%。Lotiglipron由Danuglipron结构优化而得,半衰期显著延长,可以实现每日1次口服给药。Lotiglipron在Ⅰ期临床显示较好疗效,但因导致转氨酶升高等安全性原因,2023年6月,辉瑞宣布在Ⅱ期临床阶段停止推进。2025年4月,尽管Danuglipron疗效确切,辉瑞最终还是因肝毒性、高停药率及管线优先级调整,彻底终止了其临床开发。2、Orforglipron(奥氟格列隆):接棒突围
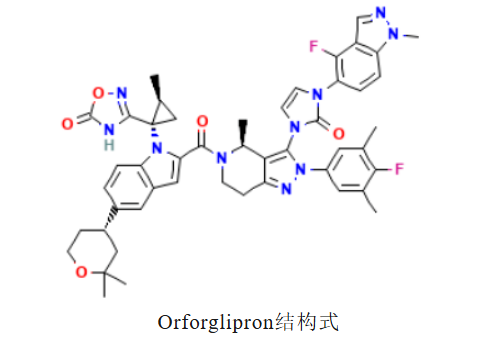
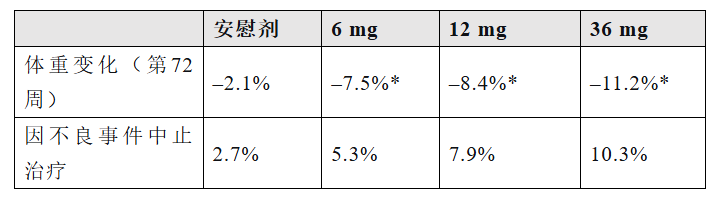
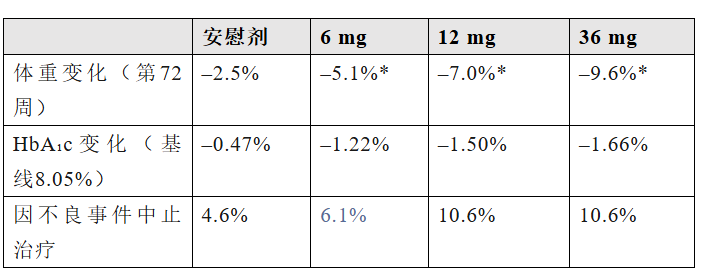
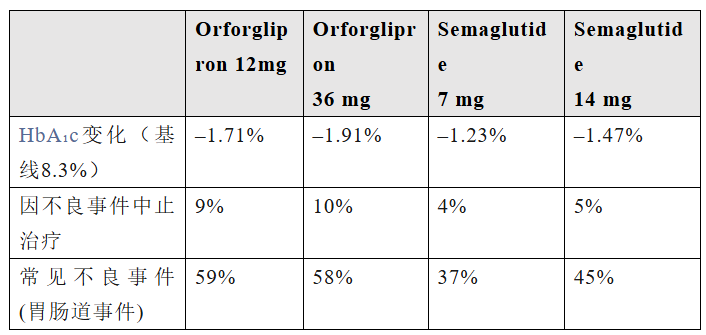
如果说Danuglipron代表了一条技术路线,那么礼来的Orforglipron(LY3502970)则是另一条——两者的分子骨架完全不同。Orforglipron(奥氟格列隆)由Chugai Pharmaceutical开发,2018年将全球开发与商业化权益授权给礼来。2026年4月1日,礼来宣布FDA批准Orforglipron(Foundayo™)上市,用于肥胖/超重。2型糖尿病适应症的上市申请计划今年提交。国内方面,Orforglipron的上市进程也在同步推进。2026年1月,NMPA正式受理奥氟格列隆片的上市申请。从临床数据看,orforglipron的表现理想:(1)肥胖(ATTAIN-1,72周,n=3127):研究结果显示,各剂量组体重降幅均显著优于安慰剂,心血管代谢指标亦显著改善。不良事件以轻中度胃肠道反应为主,安全性特征与已知GLP-1R激动剂一致。(2)肥胖合并2型糖尿病(ATTAIN-2,72周,n=1613):该研究主要终点指标是从基线至第72周体重的平均百分比变化,关键次要终点指标也包括了所有剂量组HbA₁c的平均变化。结果显示如下表,Orforglipron各剂量组体重降幅均显著优于安慰剂,且呈剂量依赖性;安全性方面,不良事件以轻至中度胃肠道反应为主,多发生于剂量递增阶段。(3)2型糖尿病(ACHIEVE-3,52周,头对头vs口服司美格鲁肽,n=1698):该研究主要终点为糖化血红蛋白(HbA₁c)自基线至第52周的变化。结果显示,orforglipron两个剂量组在降糖效果上均不劣于口服司美格鲁肽的两个剂量组,但胃肠道不良反应和因不良事件中止治疗的比例在orforglipron组中更高。Danuglipron和Lotiglipron因肝酶升高而终止开发,其肝毒性原因尚不明确,可能与药物早期筛选的偶然结果有关。这一背景让业界格外关注Orforglipron的肝脏安全性。所幸,从上述试验结果来看,未发现Orforglipron存在肝毒性。3、冲刺阶段:四款国产小分子GLP-1挺进III期
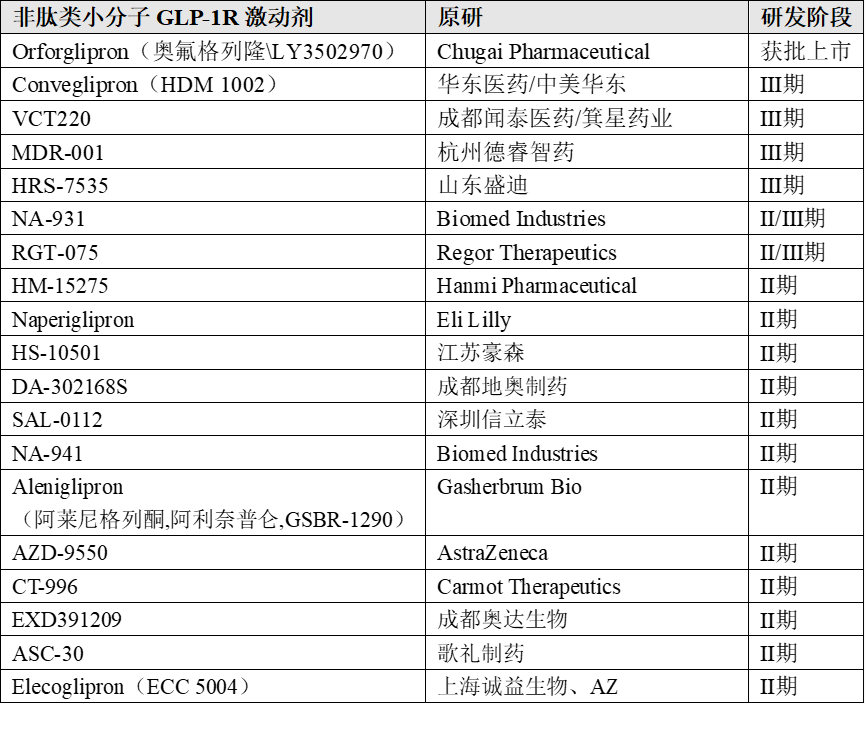
从全球研发格局来看,非肽类小分子GLP-1R激动剂的竞争已进入关键阶段。目前仅礼来的Orforglipron获批,但紧随其后的III期临床阵营中,国内企业占据了绝对主力——华东医药HDM1002、闻泰/箕星VCT220、德睿智药MDR-001、恒瑞HRS-7535均已推进至III期。照此势头,第二款获批上市的小分子GLP-1很可能来自中国。进展靠前的非肽类小分子GLP-1R激动剂
4、从分子结构窥见各药企的“微创新”之路
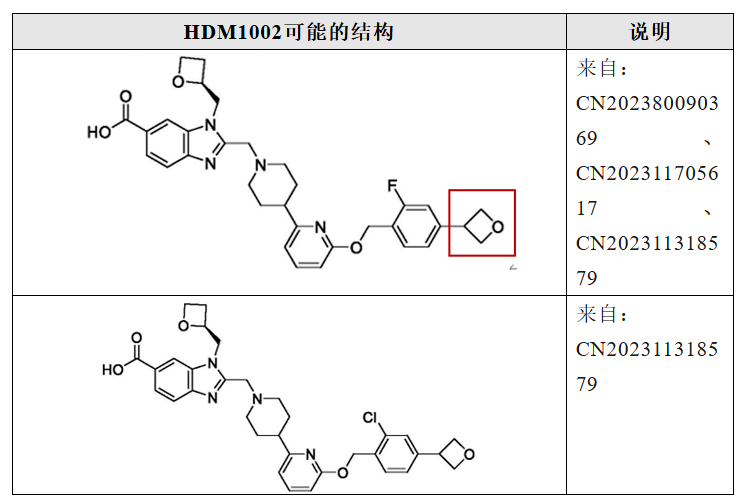
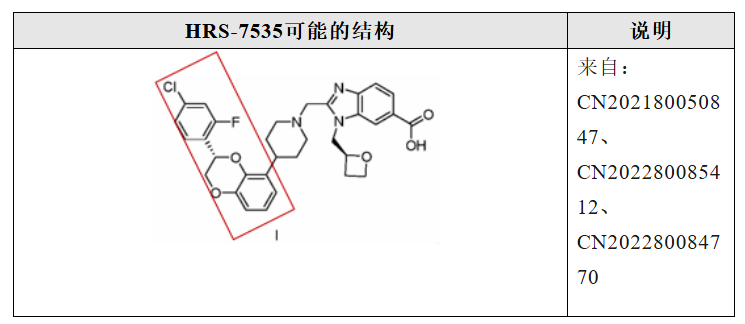
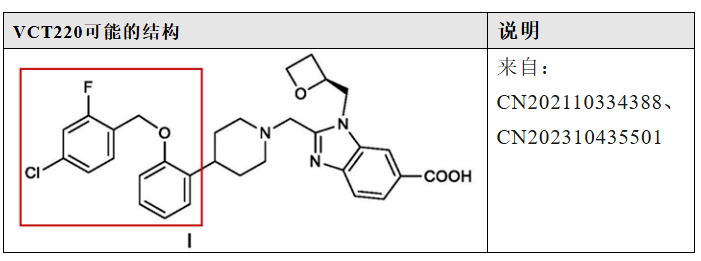
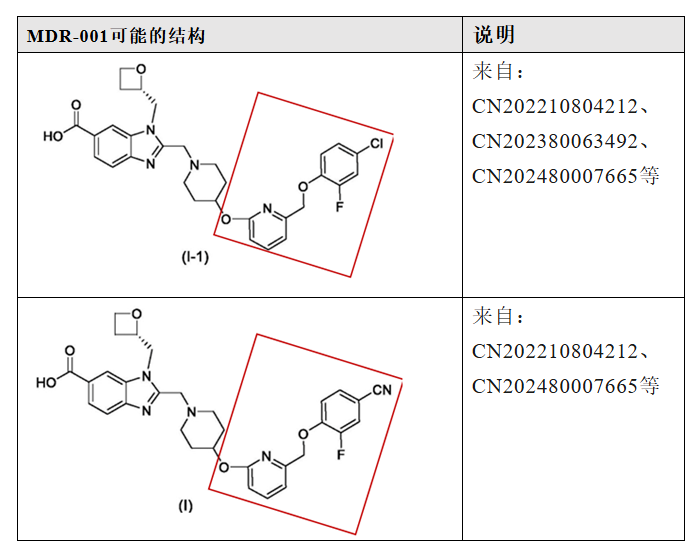
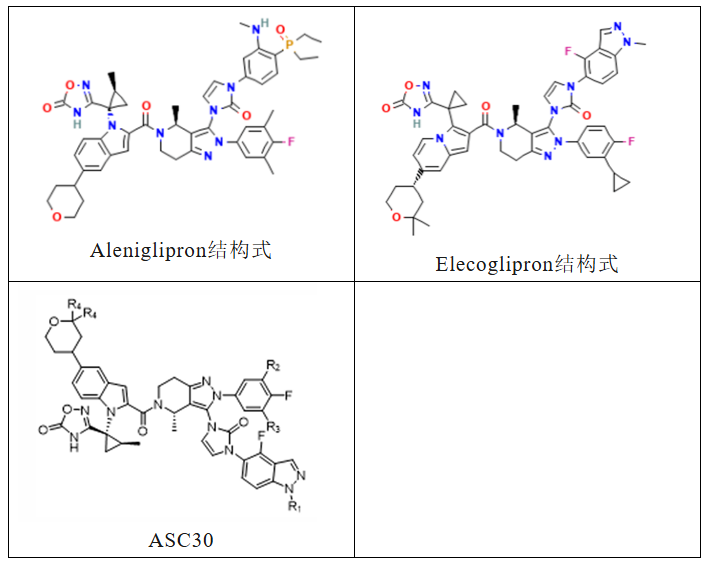
多家药企布局口服小分子GLP-1R激动剂。但目前关于口服小分子GLP-1R激动剂的开发策略仍以Follow为主,从公开的专利来看,大部分企业可能Follow了Danuglipron的结构。包括已经进入Ⅲ期临床的四个品种:HDM1002已进入临床Ⅲ期,适应症为2型糖尿病和超重/肥胖。目前尚未公开HDM1002的结构,根据华东医药公布的专利,HDM1002可能是以下结构,主要是将Danuglipron的氰基替换为氧杂环丁烷。而下图两个结构区别在于氟氯原子的相互替换,与danuglipron的区别下图已圈出。2024年,恒瑞将包括HRS-7535在内的小分子GLP-1权益授权给Hercules公司(除大中华区外)。HRS-7535结构上沿用了Danuglipron骨架。HRS-7535目前已进入临床Ⅲ期,适应症为2型糖尿病和超重/肥胖。尚未公开HRS-7535的结构,根据恒瑞医药公布的专利,HRS-7535可能是以下结构。HRS-7535也沿用了Danuglipron的骨架。与Danuglipron结构的差异已圈出。VCT220(CX11)由成都闻泰开发,2024年12月,箕星获得除中国区以外的全球权益。目前,VCT220已进入Ⅲ期临床,适应症为超重/肥胖,而2型糖尿病适应症的Ⅰ期临床也在开展中。目前尚未公开VCT220的结构,从闻泰公开的专利看,VCT220可能的结构如下,同样也是follow Danuglipron。与Danuglipron结构的差异已圈出。杭州德睿智药的MDR-001是国内首个人工智能设计(AIDD)的药物分子,已进入进入Ⅲ期临床,适应症为超重/肥胖。目前尚未公开MDR-001的结构,从公开的专利看,MDR-001可能的结构如下,同样沿袭了Danuglipron的设计思路,图中圈出的部分即为两者结构差异所在。另外,同样遵循Danuglipron开发路径的,还包括成都地奥制药的DA-302168S、信立泰的SAL-0112等,这些药物也已推进至临床Ⅱ期。围绕orforglipron的专利改造同样活跃。包括Gasherbrum Bio的Aleniglipron(GSBR-1290)、上海诚益生物(后授权给AZ)的Elecoglipron(ECC 5004),歌礼制药的ASC30围绕Orforglipron改造,但仍在临床Ⅱ期。6、Ⅱ期结果:进展靠前的四款国产小分子GLP-1的疗效和安全性如何?
12周中国II期试验(超重/肥胖,无糖尿病):HDM1002 100 mg BID、200 mg BID、400 mg QD组体重变化分别为-4.63%、-6.08%、-6.83%,安慰剂组-2.88%(200 mg BID、400 mg QD组与安慰剂比较差异显著)。腰围、BMI、血压、HbA1c、ALT等代谢指标均改善。安全性良好,不良反应多为轻中度胃肠道反应,各组未见肝酶升高趋势。36周中国II期试验(肥胖,BMI 28~40,无糖尿病):第26周,HRS-7535 30 mg、60 mg、120 mg、180 mg组体重变化分别为-2.99%、-7.17%、-6.17%、-9.36%,安慰剂组-2.50%。180 mg组第36周变化达-9.50%,35.4%受试者减重≥10%(安慰剂组6.5%)。安全性与其他GLP-1类药物一致,不良事件以轻中度胃肠道反应为主(多见于滴定期),因不良事件停药率为2.1%,未见肝酶升高趋势。16周中国II期试验(超重/肥胖,无糖尿病):VCT220 80 mg、120 mg组体重变化分别为-5.8%、-7.4%,160 mg快速/慢速滴定组体重变化分别为-9.7%和-9.4%(p≤0.001),安慰剂组-1.6%。体重相关指标及心脏代谢指标(包括肝酶、血压)均获改善。耐受性良好,主要不良事件为轻中度胃肠道反应,未见肝损伤信号。24周中国IIb期试验(超重/肥胖伴体重相关合并症):MDR-001各剂量组(90~180 mg BID)体重变化-8.2%~-10.3%(绝对减重7.4~9.2 kg),安慰剂组2.4 kg(P<0.00001)。腰围、血脂、血压等代谢指标改善。安全性优异,无药物相关严重不良事件,仅0.8%因不良事件停药;胃肠道反应轻中度,集中于滴定期前6周。受试者整体肝脏方面安全性表现良好,且入组约20%有肝功能异常史者中,未见转氨酶升高,治疗组转氨酶较基线明显下降。仅从数据看,四款口服小分子GLP-1激动剂在超重/肥胖人群中均展现出显著减重疗效与多重代谢获益,耐受性良好,胃肠道反应多为轻中度可控。尤为重要的是,虽结构源自Danuglipron,但II期临床显示它们的肝脏安全性良好。从HRS-7535和MDR-001已公开数据看,因不良事件停药率较低。7、结语
辉瑞折戟在前,Danuglipron和Lotiglipron因肝毒性等问题已终止开发,问题或与分子结构相关。目前推进至Ⅲ期的品种推测均为Danuglipron的follow产品,另有多款follow品种正处于Ⅱ期临床阶段。这不禁引人追问:即便部分Ⅲ期产品在Ⅱ期未显示肝毒性,其他follow品种能否真正摆脱肝毒性与高停药率?follow Orforglipron又是否具有更高的安全性?但对想入局的企业而言,机会同样存在。因为不同于肽类GLP-1,小分子GLP-1结构改造空间大,更易通过专利形成护城河,尤其是Danuglipron专利保护范围窄的情况下,突破空间更大。只是需要警惕,由于结构相似性较高,研发赛道容易“撞车”——毕竟盯着这块蛋糕的人很多。[1] Wharton S, Aronne LJ, Stefanski A, et al. Orforglipron, an Oral Small-Molecule GLP-1 Receptor Agonist for Obesity Treatment. N Engl J Med. 2025;393(18):1796-1806. doi:10.1056/NEJMoa2511774[2] Horn DB, Ryan DH, Kis SG, et al. Orforglipron, an oral small-molecule GLP-1 receptor agonist, for the treatment of obesity in people with type 2 diabetes (ATTAIN-2): a phase 3, double-blind, randomised, multicentre, placebo-controlled trial. Lancet. 2026;406(10522):2927-2944. doi:10.1016/S0140-6736(25)02165-8[3] Rosenstock J, Yabe D, Cox D, et al. Efficacy and safety of once-daily oral orforglipron compared with oral semaglutide in adults with type 2 diabetes (ACHIEVE-3): a multinational, multicentre, non-inferiority, open-label, randomised, phase 3 trial. Lancet. 2026;407(10534):1147-1160. doi:10.1016/S0140-6736(26)00202-3[4] Oral_presentation_ASC30_EASD_20250916_final_version.pdf[5] Gu W, Zhang L, Li L, et al. Efficacy and safety of a novel oral small molecule GLP-1RA in Chinese obese adults without diabetes. Diabetes. 2025;74(Suppl 1):865-P. doi:10.2337/db25-865-P[6] Ji L, Gao L, Meng C, et al. Efficacy and safety of VCT220 in Chinese adults with overweight or obesity. Diabetes. 2025;74(Suppl 1):743-P. doi:10.2337/db25-743-P[7] Zhang H, Wu T, Wu Y, et al. Binding sites and design strategies for small molecule GLP-1R agonists.Eur J Med Chem. 2024;275:116632. doi:10.1016/j.ejmech.2024.116632[8] Șeremet OC, Pușcașu C, Andrei C, Nițulescu G, Zbârcea CE, Olaru OT. Small-Molecule GLP-1 Receptor Agonists: A Promising Pharmacological Approach.Medicina (Kaunas). 2025;61(11):1902. Published 2025 Oct 23. doi:10.3390/medicina61111902
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。