中国药科大学郝海平教授团队:肺腺癌类器官分泌组深度解析新突破:纳米磁珠"钓"出肿瘤信号分子,4.9倍提升助力精准诊疗

2026年3月,中国药科大学团队在期刊《Analytical Chemistry》(IF:6.7)在线发表题为:Protein-Corona-Based Nanomagnetic Enrichment Strategy for In-Depth Secretome Profiling of Lung Adenocarcinoma Organoids 的高水平研究论文。
abstracts
论文摘要
分泌蛋白是细胞间通信的关键介质,它们塑造了肿瘤微环境(TME)。虽然来源于患者的类器官(PDOs)提供了保留患者异质性且生理相关的模型,但全面的分泌组检测仍然具有挑战性。这一困难源于分泌蛋白的低丰度以及维持类器官所需的外源培养基组分的高干扰。
在此,我们报告了一种基于蛋白质冠纳米磁珠的PDO分泌组检测工作流程(PPSP),该流程将磁珠富集与高分辨率质谱数据非依赖获取(HRMS-DIA)结合起来。通过利用蛋白质冠效应来减轻背景干扰,PPSP显著增强了检测深度。在对肺腺癌(LUAD)PDOs的概念验证应用中,该工作流程在单个样本中鉴定了1376种蛋白质——相比直接分析提高了4.9倍——并发现了1095种传统方法无法检测到的蛋白质。
值得注意的是,PPSP使得已知LUAD生物标志物以及与患者生存相关的先前未描述的分泌蛋白均可被检测到。这一稳健且可扩展的平台促进了PDO分泌组的深入剖析以及临床相关信号蛋白的识别。
novelty
创新点
1. 开发了一种基于蛋白冠纳米磁珠的肺腺癌类器官分泌组富集策略(PPSP),通过肽配体功能化磁珠实现高丰度背景蛋白的选择性去除,显著提升低丰度分泌蛋白的检测灵敏度。
2. 单次样本可鉴定1376个蛋白,较直接分析法提升4.9倍,其中1095个蛋白为传统方法无法检测的新发现蛋白,极大拓展了类器官分泌组的鉴定深度。
3. 成功捕获多种已知肺腺癌临床生物标志物(如CEA、CYFRA 21-1、NSE)及新型免疫调控因子(如CIRBP),后者与患者预后显著相关,展现出临床应用潜力。
4. 实现了对IGF信号轴等完整功能通路的定量分析,克服了高丰度背景蛋白对低丰度信号分子的掩蔽效应,为肿瘤微环境研究提供高保真数据。
5. 建立了可扩展、可重复的工作流程,批次内和批次间变异系数均低于20%,在保持患者间异质性的同时确保技术稳定性,适用于大规模临床样本分析。
background
科学背景与研究现状
分泌蛋白是肿瘤细胞间通讯的关键介质,通过重塑肿瘤微环境、调控免疫监视和促进转移等途径影响癌症进展与治疗反应。由于分泌蛋白可进入血液循环,其作为非侵入性诊断标志物具有重要临床价值。然而,现有分泌组分析主要依赖传统细胞系和动物模型,这些方法难以保留患者特异性异质性。患者来源类器官(PDOs)虽能忠实再现原发肿瘤的组织病理学特征和基因组景观,为肿瘤研究提供了生理相关性更高的模型,但其分泌组分析面临独特挑战:培养基中高丰度外源蛋白(如白蛋白、转铁蛋白)严重干扰低丰度内源性肿瘤分泌蛋白的检测,而血清饥饿处理又会损害类器官活性和分化状态。传统富集策略无法有效区分培养基添加剂与肿瘤分泌蛋白,缺乏能够在不干扰类器官培养的前提下选择性去除背景干扰的稳健方法,这成为制约PDO分泌组深度分析的瓶颈。因此,开发一种能够高效去除高丰度背景、富集低丰度信号蛋白的技术平台,对于挖掘PDO模型的临床转化价值具有重要意义。
approach
技术路线与实验方法
一、类器官培养与条件培养基收集:从3例肺腺癌患者手术切除标本中分离培养PDOs,传代至P1代,待类器官直径达100μm时更换新鲜完全培养基,72小时后收集条件培养基(PDO-CM),离心过滤后添加蛋白酶抑制剂,-80℃保存备用。
二、蛋白冠纳米磁珠富集:采用Fe3O4@PDA@Au-PP肽功能化磁珠,经PBS清洗后与1200μg PDO-CM蛋白在28℃、1700rpm条件下孵育1小时,磁分离后弃上清,洗涤去除非特异性结合蛋白。
三、磁珠上蛋白质组学处理:还原烷基化处理后,加入胰蛋白酶37℃消化16小时,甲酸终止反应,磁分离去除磁珠,真空干燥后用C18 ZipTip脱盐,再次干燥后-80℃保存。
四、液相色谱-质谱分析:采用Orbitrap Eclipse Tribrid质谱仪,配备EASY-nLC 1200系统,90分钟梯度洗脱,DIA模式采集数据,60个可变窗口进行MS2扫描。
五、数据分析:使用DIA-NN软件进行蛋白质鉴定和定量,设置1%假发现率,与TCGA数据库联合进行生存分析和免疫相关性分析。
results graph
结果图
Figure 1展示了PPSP工作流程及PCN磁珠和肺腺癌类器官的表征。图A为PPSP工作流程示意图,包括PCN磁珠孵育富集、还原烷基化、磁珠上消化及DIA质谱分析;图B显示磁珠的四层核壳结构(Fe3O4核心、PDA中间层、不连续Au壳层和肽配体外层);图C和D的透射电镜图像证实磁珠呈均匀球形(约250nm)、无聚集;图E的动态光散射显示三批次磁珠粒径分布一致;图F的H&E染色显示类器官保留肿瘤样上皮结构;图G的Calcein-AM染色证实类器官在分泌组收集期间保持高活性。
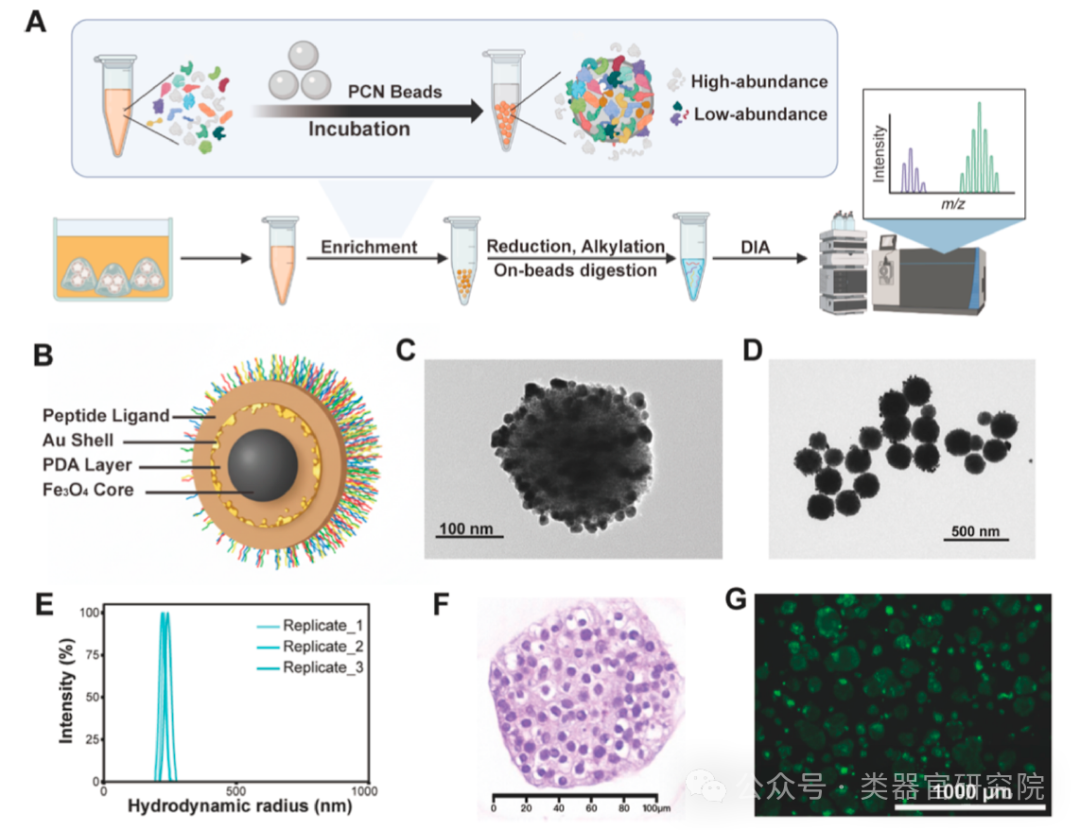
Figure 2展示了PPSP富集分析显著扩展蛋白质鉴定覆盖度的结果。图A和B显示PPSP较直接分析分别提升蛋白鉴定数4.6倍(最高达1376个)和肽段数3倍以上;图C的丰度分布曲线显示PPSP样品动态范围跨越6个数量级;图D的韦恩图显示PPSP独特鉴定1095个蛋白;图E的肽段覆盖图显示TGFB1、CCL20等低丰度蛋白的肽段覆盖率显著提升;图F显示临床标志物鉴定率从10.96%提升至22.9%;图G显示随上样量增加蛋白鉴定数逐步饱和;图H显示PPSP特异性富集血浆中浓度低于1μg/mL的中低丰度蛋白。
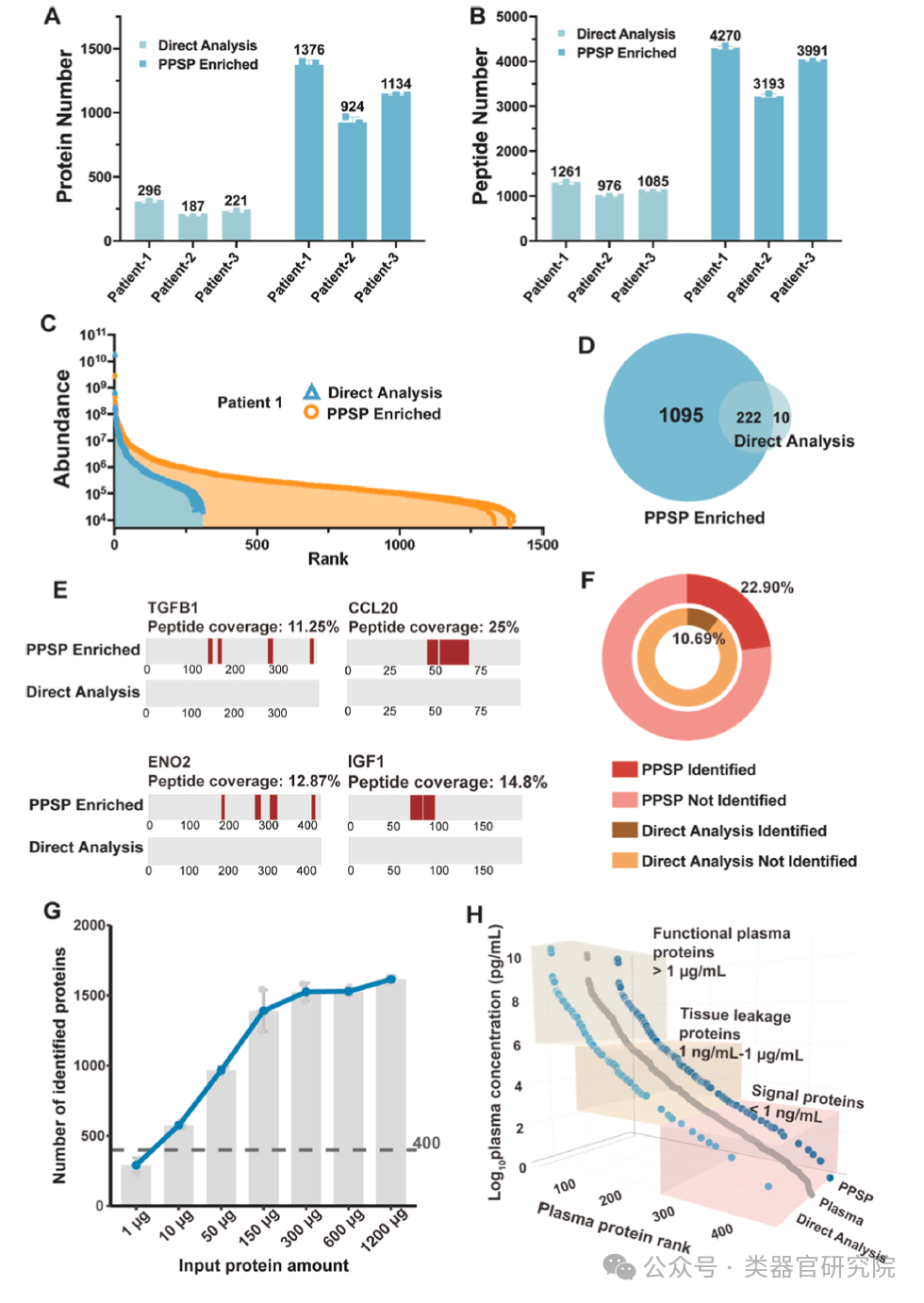
Figure 3评估了PPSP工作流程的重复性和精密度。图A显示三次技术重复间蛋白丰度的Pearson相关系数均≥0.95;图B的小提琴图显示三例患者蛋白定量变异系数中位数分别为17.67%、17.75%和12.52%;图C显示CCL20、CEACAM5等代表性低丰度分泌蛋白的变异系数均低于16%;图D的主成分分析显示技术重复聚类良好且患者间明显分离;图E的韦恩图显示三例患者间共有蛋白占56.6%,患者特异性蛋白占43.4%,提示PPSP能保留患者间异质性。
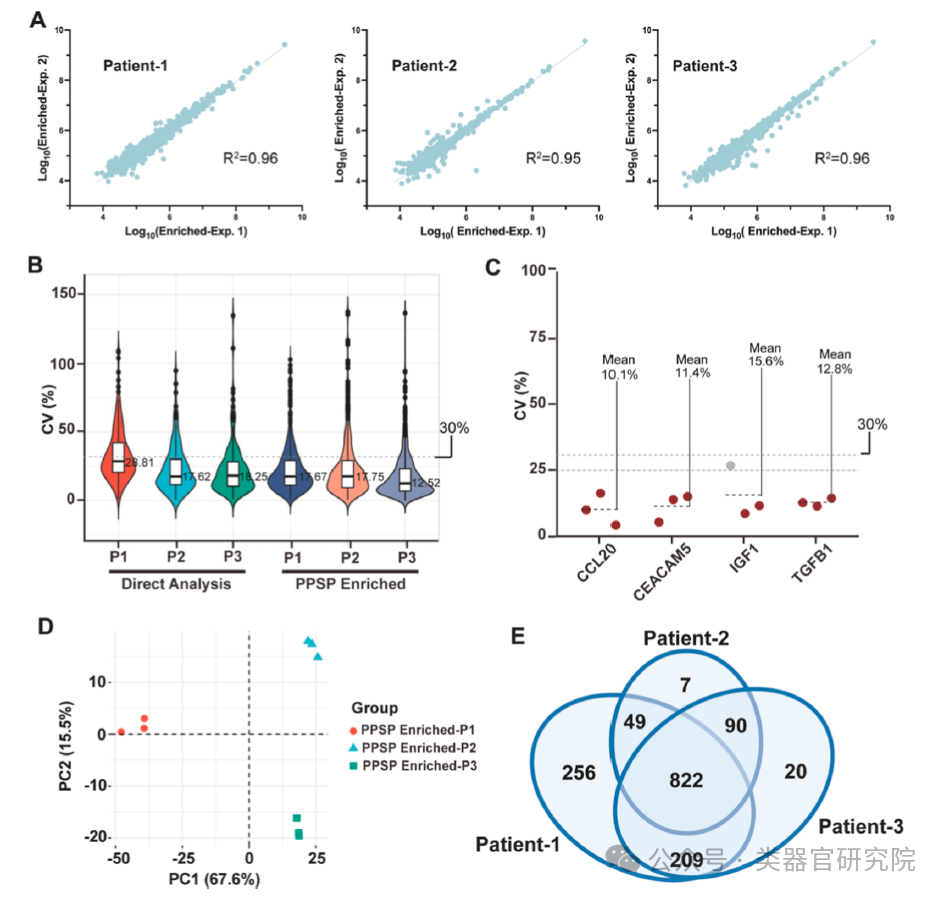
Figure 4评估了PPSP的批次内和批次间重复性。图A为实验设计示意图;图B显示批次内技术重复的变异系数主要分布在20%以下;图C的配对比较显示三次重复间Pearson相关系数达0.98-0.99;图D的主成分分析显示两批次样本无聚类分离;图E显示两批次蛋白鉴定数高度一致;图F显示批次间丰度变化中位数仅为-0.009,证实无系统性偏差。
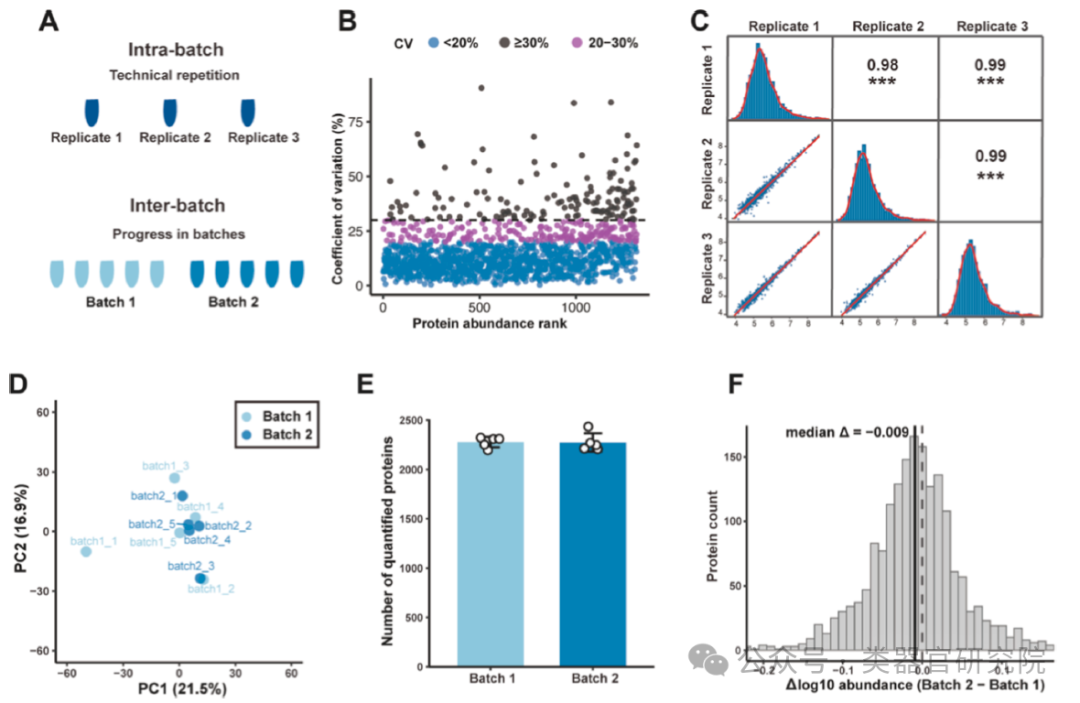
Figure 5表征了PPSP定义的类器官分泌组特征。图A显示PPSP较直接分析显著增加UniProt注释分泌蛋白、信号肽蛋白和跨膜区蛋白的鉴定数;图B显示1498个鉴定蛋白中57.5%为分泌蛋白;图C的基因本体分析显示细胞外囊泡、细胞外区域等细胞外相关组分显著富集,证实PPSP选择性捕获细胞外信号蛋白。
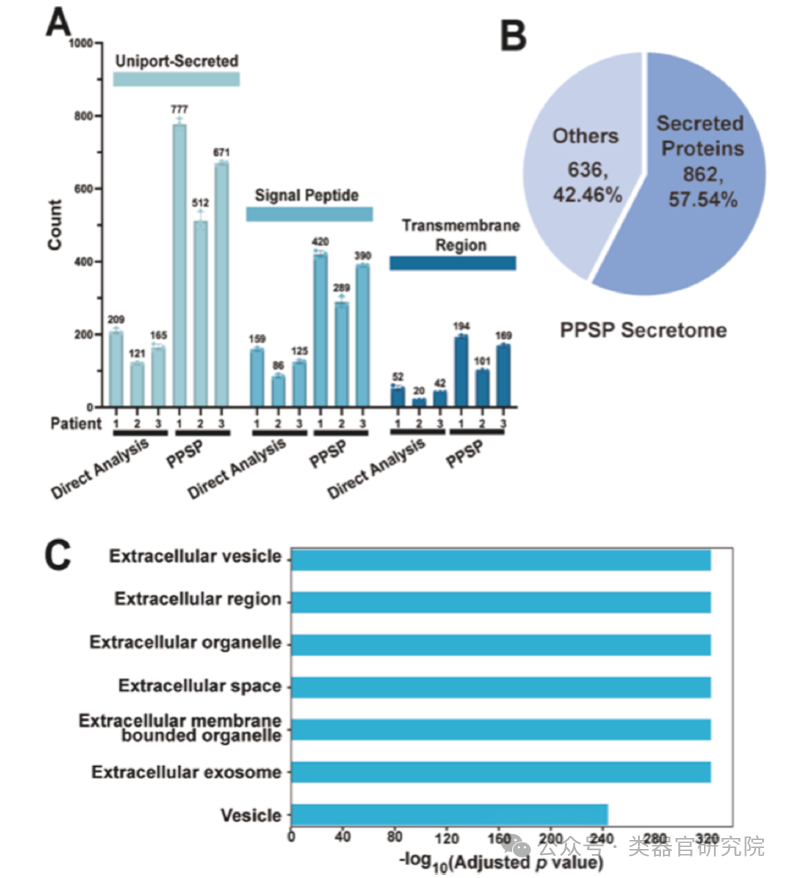
Figure 6展示了PPSP方法增强肺腺癌生物标志物检测的能力。图A显示PPSP将每例患者可检测的已知生物标志物从平均10个提升至25个以上;图B显示CK19、CEACAM5、ENO2、MUC1等经典标志物仅在PPSP富集后检出;图C的热图显示四种关键临床标志物在所有患者PDO-CM中检出,而细胞系培养基中仅检出1种;图D显示PPSP独特鉴定1072个蛋白(占71.56%),突显PDO模型较细胞系的临床保真度优势。
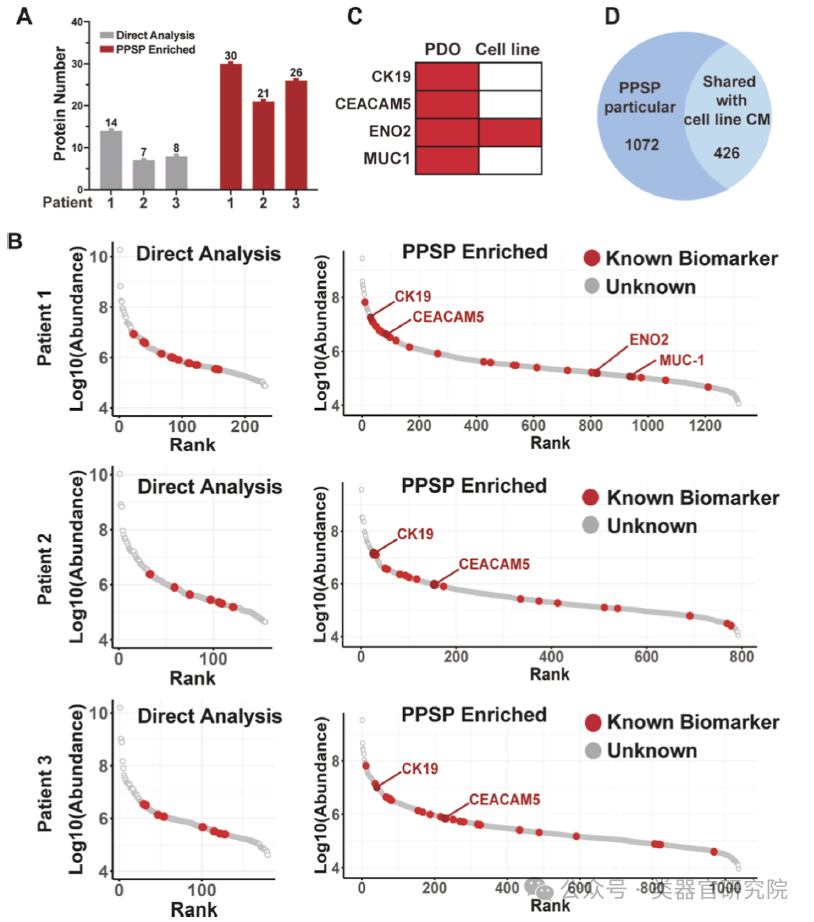
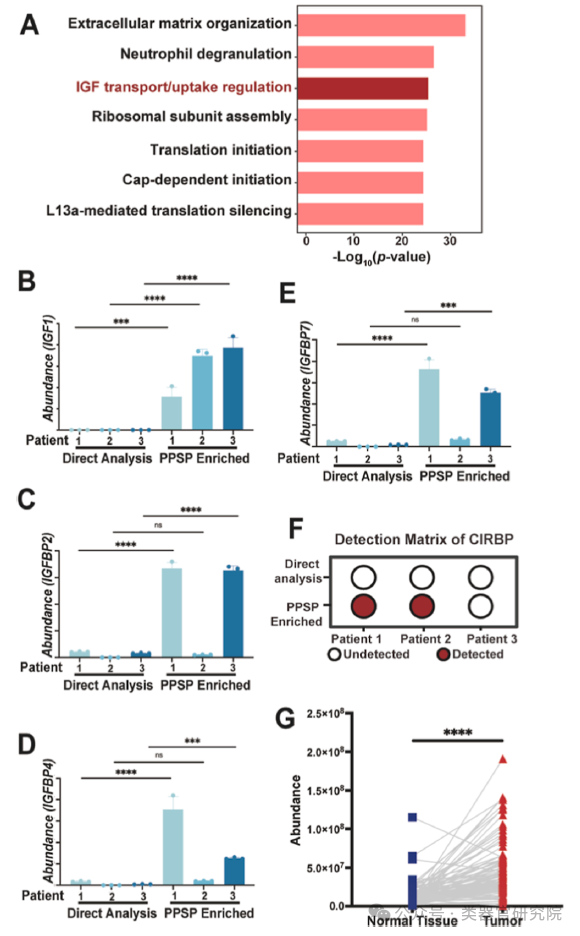
Figure 7分析了PPSP富集的低丰度分泌蛋白。图A的Reactome分析显示细胞外基质组织、IGF转运/摄取调控等通路显著富集;图B-E显示IGF1、IGFBP2/4/7在PPSP富集后丰度显著升高;图F的检测矩阵显示CIRBP仅在PPSP样品中检出;图G显示CIRBP在103例肺腺癌患者肿瘤组织中较癌旁组织高表达8.16倍,提示其作为免疫调控候选标志物的潜力。
原文链接
https://pubmed.ncbi.nlm.nih.gov/41849547/
信息来源:类器官研究院




免责声明
“汇聚南药”公众号所转载文章来源于其他公众号平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请在留言栏及时告知,我们会在24小时内删除相关信息。
本平台不对转载文章的观点负责,文章所包含内容的准确性、可靠性或完整性提供任何明示暗示的保证。
喜欢的点个“看一看”和"喜欢"吧

不然微信推送规则改变,有可能每天都会错过我们哦~
