罗氏铩羽,吉利德50亿接盘“死亡靶点”为哪般?


当地时间4月7日,吉利德宣布收购德国生物技术公司Tubulis,以增强其在抗体偶联药物(ADC)领域的布局。通过此次交易,吉利德将获得TUB-040,一款靶向NaPi2b、针对铂耐药卵巢癌和非小细胞肺癌的ADC药物(目前处于1b/2期临床),以及另一款针对多种实体瘤的5T4靶向ADC药物TUB-030。交易对价包括31.5亿美元前期现金及最高18.5亿美元里程碑付款,预计2026年第二季度完成。收购后,Tubulis将作为吉利德内部独立的ADC研究部门运营,其慕尼黑基地将成为ADC创新中心。


“死靶”复活?从不可成药到ADC新宠

NaPi2b(SLC34A2)是溶质载体家族SLC34中的关键成员,是一种pH敏感型的钠依赖性磷酸盐转运蛋白。它通过钠离子共转运的方式,将无机磷酸盐导入上皮细胞,在较低pH环境下发挥作用,从而帮助维持全身磷酸盐的平衡。在人体中,NaPi2b在肺部高表达,同时在卵巢、胰腺、肾脏、小肠、睾丸、前列腺和乳腺等组织也有分布,并且在非小细胞肺癌、卵巢癌、乳腺癌等多种肿瘤中表现出异常表达。
理论上,NaPi2b是一个颇具潜力的ADC靶点。它的胞外环在肿瘤细胞和正常组织中会呈现不同的构象状态:在正常组织里,由于糖基化程度不足或二硫键未能形成,表位区域往往难以完整暴露,导致抗体不容易结合;而在肿瘤微环境中,这个表位却能充分暴露并维持稳定构象,更容易被抗体高效识别和结合。
然而这个靶点的研发并不顺利。最大的挑战在于NaPi2b在正常肺组织等部位也有表达,一旦抗体结合并释放毒素,很容易引发典型的“ontarget, offtumor”毒性。正因如此,NaPi2b长期被视为一个“高表达但不可成药”的靶点。
Pharma ONE药物研发大数据平台显示,罗氏开发的NaPi2b靶向ADC——Lifastuzumab vedotin在治疗铂类耐药卵巢癌的2期临床试验中未能达到无进展生存期(PFS)的主要终点,最后终止开发。同样,Mersana公司的Upifitamab Rilsodotin也因为2期临床中出现严重安全性问题,且未能达到主要终点而宣告失败。

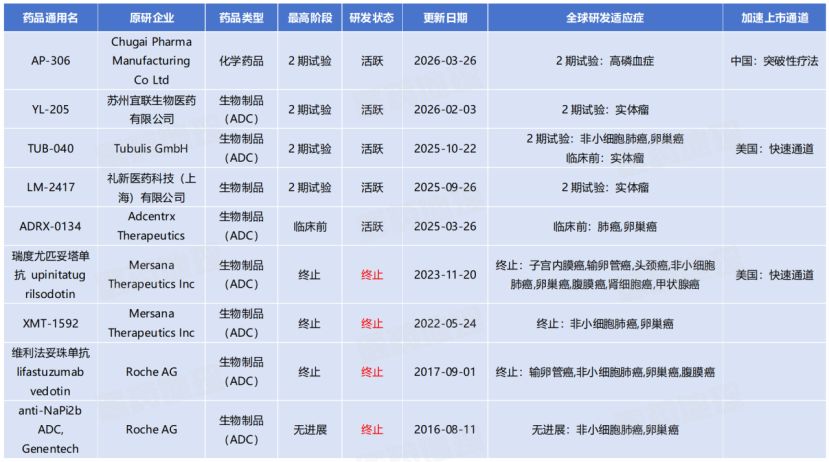
NaPi2b(SLC34A2)靶点研发进度
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
但研发人员并没有彻底放弃NaPi2b。随着ADC技术的不断迭代,这个靶点又重新进入了大家的视野。全球已经有好几款相关药物推进到了临床试验阶段,比如Tubulis公司的TUB-040,以及国内苏州宜联生物的YL205。尤其值得一提的是,TUB-040在去年ESMO 2025公布的治疗铂类耐药卵巢癌的期临床数据里,客观缓解率(ORR)达到了59%,表现相当亮眼。除了ADC,也有企业尝试双抗路线,比如礼新医药的LM-2417。可以说,NaPi2b这个曾经让人望而却步的靶点,正在慢慢打开局面。


来源:Tubulis官网
50天150亿,吉利德在下什么棋?
近50天来,吉利德陆续完成了针对Arcellx、Ouro、Tubulis的三笔并购交易,交易总金额高达约150亿美元。
2月23日,吉利德以78亿美元预付款收购Arcellx,获得BCMA靶向CAR-T药物Anito-cel,该药物目前处于FDA审批阶段,有望成为多发性骨髓瘤治疗领域的潜在最佳药物。同时,吉利德还纳入了Arcellx的细胞治疗技术平台,进一步强化了其在细胞疗法领域的布局。
3月23日,吉利德与Ouro Medicines达成协议,交易总金额最高达21.75亿美元,其中包括16.75亿美元首付款及不超过5亿美元的里程碑付款。由此,吉利德获得了BCMA/CD3双抗药物CM336。该药物具备“免疫重置”潜力,可应用于多种自身免疫疾病的治疗。此外,Ouro的T细胞衔接器(TCE)研发管线也一并纳入麾下,拓展了吉利德在免疫疾病领域的布局。
而此次收购Tubulis,吉利德获得了下一代抗体药物偶联物(ADC)技术平台,以及处于临床阶段的ADC药物TUB040和TUB030,从而显著强化了其在ADC领域的研发能力。


来源:吉利德官网
短短不到两个月时间,吉利德通过这三笔连续交易,在细胞治疗、双抗和ADC三个关键方向同步落子。从BCMA靶向的CAR-T和双抗,到NaPi2b等差异化ADC靶点,吉利德正在构建一条覆盖肿瘤与自身免疫疾病、兼具早期创新与后期临床资产的多元化管线。这种密集而清晰的战略布局,反映出公司管理层对“后新冠时代”吉利德转型的明确思路:以肿瘤和免疫为核心增长引擎,借助外部创新加速内部管线的迭代与拓展。



