创新药速败策略-Fail Fast. Succeed Faster
发布时间:2026-04-09来源:药事纵横
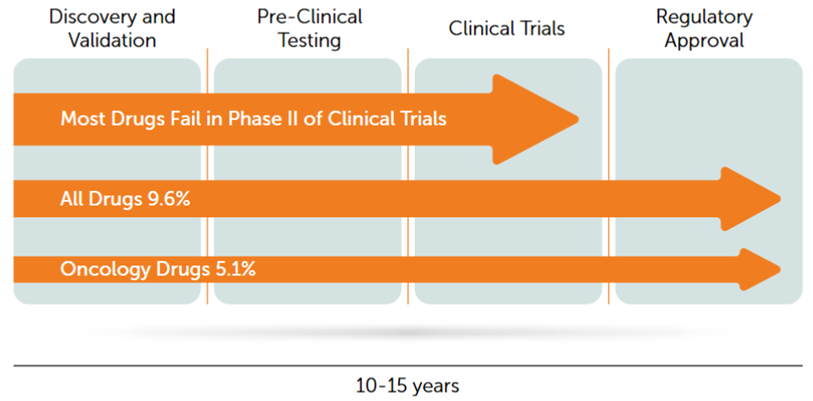
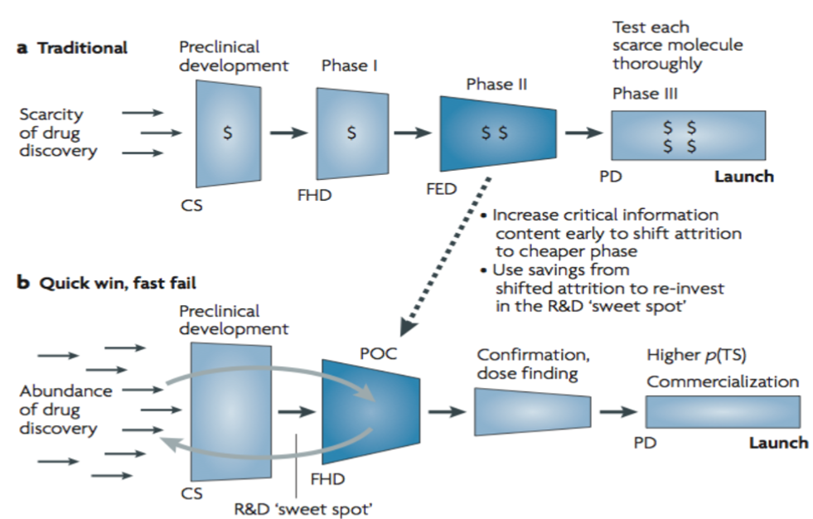
2026年了,我们站在一个科技与认知空前繁荣的时代节点上。基因编辑、细胞疗法、人工智能制药……生命科学的边界以前所未有的速度向外延伸,为攻克顽疾带来了前所未有的曙光。然而,与这激动人心的科学图景形成鲜明对比的,是整个创新药研发行业挥之不去的效率阴霾。一种被称为“反摩尔定律”的现象,如同一个冷酷的咒语,依然笼罩着我们:每十亿美元研发投入所能获得的新药批准数量,大约每九年就会减半。图1药物研发成功率(来源: Clinical Development Success Rates, BIO 2015 THE MIND-BLOWING)我们无法回避一个残酷的现实:一款新药从实验室到患者手中,平均耗时超过十年,耗资动辄超过20亿美元。更令人揪心的是,进入临床试验的候选药物,最终能成功上市的几率不足十分之一,甚至在5%左右徘徊。这意味着,行业中绝大部分——约75%的研发投入——最终都流向了失败的项目。那些代价高昂的后期临床失败案例,不仅造成巨大的财务损失,更占用了宝贵的资源,延缓了无数潜在好药的前进步伐。面对研发成本螺旋式上升、科学复杂性指数级增长、支付方压力日益严峻的三重夹击,传统的、线性的、以“不惜一切代价避免失败”为核心的研发模式,已显得力不从心。我们不禁要问,是否有一条新的路径,能够帮助我们走出这个“高投入、高风险、长周期”的泥潭?在这样的背景下,一个看似反直觉,实则蕴含深刻智慧的战略逐渐走向舞台中央,那就是——“快速失败”。这并非鼓励失败,而是一种主动的、系统性的策略,旨在研发早期、成本最低的阶段,通过“聪明的失败”来为“最终的胜利”铺平道路。图2 “速赢,速败”药物开发范式与传统方法之比较(参考3)“速败”的逻辑:为何放弃比坚持更需要智慧
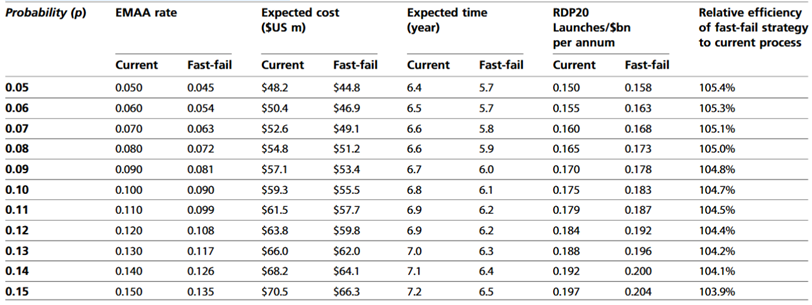
“快速失败”的核心,是一场深刻的思维范式转移。它要求我们从传统的“避免失败”转向“拥抱、管理并从失败中学习”。其背后,有着坚实的经济学、风险管理和知识管理逻辑。表1.对于现行策略与快速失败策略,其预期开发成本、预期开发时间及研发生产力对比如下。快速失败策略的预期成本和开发时间均更低。尽管快速失败策略的上市许可获批预期率更低,但其新产品上市速度更快,且开发成本更低。就研发生产力而言,在整个从p=0.05到p=0.15的概率区间内,快速失败策略的表现均优于现行策略。然而,随着可上市分子概率(p)的升高,快速失败策略的相对效率优势会随之降低。(参考4)从经济学角度看,我们首先要直面一种根深蒂固的认知偏见——“沉没成本谬误”。当一个项目已经投入了数年心血和数千万资金后,即使后续数据已亮起红灯,我们往往也倾向于继续投入,幻想着能“挽救”之前的投资。这种心理极具破坏力,它会让资源被大量浪费在没有希望的“僵尸项目”上。而“速败”策略则要求我们必须理性地认识到:过去的投入与未来的决策无关。决策的唯一依据,应该是项目在当前信息下的未来成功概率和潜在价值。放弃一个项目,其真正的成本并非已经投入的“沉没成本”,而是释放了宝贵资源的机会成本。将这些资源(顶尖科学家的时间、临床试验的预算)重新配置到更高潜力的项目上,才能最大化整个研发投资组合的价值。从风险管理角度来看,创新药研发的本质,就是在高度不确定的未知领域进行探索。传统模式的致命缺陷在于,它将最大的不确定性——药物在真实人体中的疗效和安全性——留到了成本最昂贵的后期临床阶段来验证。这无异于一场豪赌。而“快速失败”则是一种主动的、前置的风险管理方法。它要求我们在研发早期,就系统性地梳理项目面临的关键风险,并设计一系列成本相对较低、周期较短的关键实验,来逐一“拷问”这些风险点。比如,一个项目的最大风险是靶点与疾病的关联性不强,那么就应该在临床前或极早期临床阶段,通过精准的生物标志物来快速验证。一旦验证失败,项目就应果断终止,而不是等到耗费数亿美元的III期临床试验后才追悔莫及。通过这种方式,我们将一个巨大的、集中的后期失败风险,化解为一系列可控的、分散的早期决策点。更重要的是,从知识管理角度来看,一个项目的终止不应被视为个人或团队的失败,而应被定义为组织成功获取了一项关键的知识——即“这条路走不通”。这份知识与“这条路走得通”同样宝贵,它能帮助组织避免在错误的方向上重复投入。我们应当建立起系统性的机制,从失败项目中提取、总结、分享和复用知识。例如,某个化合物因未预见的脱靶毒性而失败,相关的毒理学数据就应被存入中央数据库,为后续项目的设计提供宝贵借鉴。葛兰素史克提出的“烧掉干草堆”模型,通过数学模拟清晰地告诉我们:影响整体研发成本和上市时间的关键变量,并非成功分子的开发成本,而是大量失败项目在研发管线中占用的总时间。压缩这个“失败停留时间”,正是“速败”策略的核心目标,它能让我们更快地找到隐藏在“干草堆”里的那根“针”。战术实践:如何让“速败”贯穿研发全周期
“速败”并非空洞的口号,它需要转化为研发流程中一系列具体的、可操作的战术,贯穿从靶点发现到后期临床的整个链条。在药物发现与临床前阶段,这是实施“速败”的黄金时期,因为此时的试错成本相对最低。我们的目标是,在候选化合物进入昂贵的、受严格监管的临床开发之前,最大限度地“去风险”。生物标志物无疑是我们的“精确制导武器”。在选择靶点时,就必须明确是否存在可靠的生物标志物,能在细胞或动物模型中清晰地证明靶点参与了疾病进程。在筛选化合物时,除了关注其亲和力,更要关注它是否能有效调节目标生物标志物,实现“机制验证”。同时,我们必须尽早利用类器官、器官芯片等先进的三维细胞培养模型。它们能更真实地模拟人体器官的微环境和功能,其预测药物毒性和疗效的能力远高于传统二维细胞培养和动物模型。结合高通量ADMET(吸收、分布、代谢、排泄、毒性)筛选,我们可以在早期就排除大量具有成药性缺陷的“漂亮分子”,真正做到“尽早失败,便宜失败”。当项目进入早期临床开发阶段,设立清晰的“生死门”变得至关重要。这一阶段的核心,就是“概念验证”研究。其目的不是追求统计学上显著的疗效,而是在小规模患者群体中,明确地验证药物能否以安全的剂量,在目标人群中达到预期的生物学效应。一个成功的“概念验证”研究,必须围绕清晰的、可量化的问题来设计,并严重依赖于生物标志物。如果药效动力学标志物没有变化,或者与疗效信号完全脱钩,这就是一个强烈的“终止”信号。同时,我们应积极采用适应性试验设计,允许在试验进行中根据积累的数据动态调整方案,例如调整剂量或富集更敏感的患者亚群,从而更快地找到最佳剂量或识别出药物的无效性。而“篮子试验”和“平台试验”等创新模式,则能让我们在多适应症中同时探索药物的潜力,快速发现最有希望的领域,并果断放弃无效的方向。即使到了成本最高、风险最大的III期临床阶段,“速败”的理念依然重要。它体现在严格的项目进入门槛上——只有那些在早期临床中展示了清晰概念验证、具有良好安全性和明确剂量-效应关系的药物,才有资格进入这个阶段。在方案设计上,我们需要利用所有临床前和早期临床数据,通过建模和模拟来优化方案,并利用真实世界证据来更好地理解疾病和现有疗法。更关键的是,必须在III期试验中设立严格的中期无效性分析。如果中期数据显示药物达到主要终点的可能性极低,基于预设的统计学规则,我们应当有勇气果断终止试验,避免最后的“临门一脚”造成更大的损失。技术赋能:当AI成为“速败”的强大引擎
如果说“速败”是一种战略思想,那么以人工智能为代表的前沿技术,就是将这种思想转化为强大执行力的引擎。AI和机器学习通过从海量、多维度的生物医学数据中学习,为我们提供了前所未有的预测能力。最激动人心的应用之一,是预测临床失败风险。通过训练机器学习模型,整合药物的理化性质、临床前数据、组学数据以及历史临床试验信息,我们可以在项目极早期就预测其因疗效不足或毒性问题而失败的概率。同样,AI在识别新型生物标志物方面也展现出巨大潜力。通过分析海量的患者组学数据,AI可以发现与疾病亚型、预后或药物反应相关的复杂分子特征,帮助我们更早地锁定最可能受益的患者人群,从而设计出规模更小、成功率更高的临床试验。此外,生成式AI模型已被用于从头设计新分子,结合预测性的ADMET模型,我们可以在计算机中生成并筛选数以亿计的虚拟化合物,仅在源头推荐最优秀的分子进行合成。这极大地提高了药物发现阶段的效率,实现了源头上的“速败”。而“数字孪生”技术,则将这一理念推向了未来。通过整合个体的多组学、生理和医学影像数据,在计算机中构建一个高度个性化的“虚拟患者”,我们可以模拟不同药物、不同剂量在虚拟患者身上的反应。这使得“在计算机中失败”成为可能——一个候选药物可能在数千个虚拟患者身上“失败”,而成本几乎为零。这无疑是“速败”策略最理想的境界。文化的重塑:跨越“速败”之路的最大障碍
技术和流程是实施“速败”的必要条件,但绝非充分条件。无数案例表明,该策略在推行过程中遇到的最大阻力,往往来自组织内部的人为因素。科学家对项目投入的巨大心血和情感,使其很难客观地评估负面数据。项目成功与否往往与个人声誉和职业发展紧密相连,这种对失败的职业恐惧,导致人们倾向于“报喜不报忧”,或想方设法拯救一个垂死的项目。同时,僵化的组织流程和冗长的决策链,也使得终止项目的决策缓慢而低效。更致命的是,许多公司的激励机制是错位的——他们奖励的是“推进项目”,而非“做出正确的决策”。这就形成了一种文化惯性:即使数据亮起红灯,大家也更愿意将项目推向下一阶段,而不是停下来反思。要跨越这些障碍,必须进行一场深刻的文化变革。这需要领导层自上而下地推动,公开表彰那些基于充分数据做出艰难终止决策的团队,明确传递一个信号:做出正确的科学决策,比盲目地推进项目更受尊重。核心是建立一种“心理安全”的环境,让员工敢于报告负面数据、敢于承认失败,而不用担心受到惩罚。我们要学会区分“聪明的失败”——源于探索未知的、提供了宝贵学习的失败,与“愚蠢的失败”——源于疏忽或重复已知错误的失败,并严厉惩戒后者,大力褒奖前者。定期举办“项目复盘会”,让被终止项目的团队分享经验教训,将这些知识转化为组织资产。同时,改革决策治理结构也至关重要。成立一个由不同职能部门资深专家组成的、独立的研发投资组合管理委员会,让他们基于客观、预设的标准来评审所有项目,对项目的继续或终止做出统一决策,从而将决策与项目团队的情感和偏见剥离。最后,必须重构激励体系,设立奖项来奖励那些通过严谨实验证明项目应被终止,从而为公司节省大量资源的团队。只有当员工的绩效评估与决策质量、学习速度和对投资组合的贡献挂钩,而非他们所负责项目的“生死”时,“速败”才能真正落地。“快速失败”已不再是制药行业一个可选的工具,而是关乎企业生存与发展的核心战略。它并非简单地追求失败,而是一种基于深刻经济学、风险管理和知识管理原则的智慧选择。通过系统性的早期决策,我们将宝贵的资源从“僵尸项目”中解放出来,优化整个研发投资组合的价值。这场由“速败”理念引领的变革,其终极目标并非仅仅为了降低药企的成本,而是为了构建一个更高效、更可持续、真正以患者为中心的创新生态。通过将资源更精准地导向最有可能成功的创新疗法,我们将能以更快的速度、更低的代价,为全球患者带来更多、更好的治疗选择。在创新药研发这场探索未知的伟大征程中,我们无法预知通往成功的唯一路径,但我们可以通过快速地识别并关闭那些通往失败的道路,从而以更低的成本、更高的效率,最终找到那条能够真正为患者带来希望的光明之路。选择“速败”,未尝不是一种大智若愚的明智之举。- Breaking Eroom’s Law: Biopharma in Transition
- CHALLENGES OF MATURE DRUGS IN THE PHARMACEUTICAL INDUSTRY: ISSUES OF MULTICHANNEL STRATEGIES
- How to improve R&D productivity:the pharmaceutical industry’s grand challenge
- Torching the Haystack: modelling fast-fail strategies in drug development
- FAIL FAST.SUCCEED FASTER. WHITE PAPER What Pharma and Biotech Companies Stand to Gain From Early Drug Development Failures.
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。