同一种病原体,有人只是鼻塞,有人却重症甚至死亡,为什么?

本篇《自然》长文共5090字,干货满满,预计阅读时间16分钟,时间不够建议可以先“浮窗”或者收藏哦。
全文要点速览:
同一种病原体,有人只是鼻塞,有人却迅速重症甚至死亡——差别可能不在“病毒有多毒”,而在“你自身的免疫系统”。
一个离奇的病例与IEI:一种普通的环境细菌竟夺走了一个孩子的生命,答案可能是基因出了小差错——“免疫出生错误(IEI)”。
从“病原体中心”到“宿主中心”:感染并不只是病原体的事,基因的遗传变异会影响人的免疫系统功能。
新冠的启发:重症有时候来自免疫的“自我拆台”。
临床治疗:基因检测成为ICU的首选检查,新生儿的突变筛查使早期干预成为可能。
遗传的预测度:遗传能提供风险线索但不是定论,科学能做的还很有限。
原文作者:Diana Kwon
世界上有数百万人身怀遗传突变,会削弱其免疫系统。

COVID-19疫情期间,一位护士在中国四川省一家医院的重症监护室中工作。来源:Zhong Min/Feature China/Future Publishing/Getty
Michael Levin接到那个马耳他医院紧急电话的时候,刚开始在伦敦担任儿科感染病医生。当时是1980年代初,一个小男孩因为严重感染就诊,感染正蔓延至他全身,破坏多个脏器和组织。但他的医生找不到病原的踪迹。
男孩被转运至Levin的医院作进一步测试。令Levin和同事震惊的是,元凶是一种普通的细菌:偶发分歧杆菌(Mycobacterium fortuitum),存在于水和土壤中,通常是无害的。“人人都接触这种菌,但几乎没人得病。”如今任职于伦敦帝国理工学院的Levin说。尽管接受了积极治疗,这个男孩还是去世了。
这个病例显示出一个困扰医学界几十年的问题:为什么某些病原会使一些人严重感染,但其他人却毫发无损?有些人的免疫系统有什么特征,会使他们易感?这些差异又如何影响医生的防治策略?
后来发现,这名马耳他男孩有个兄弟和一个表亲也因分歧杆菌感染得过重病。经过数年搜寻,Levin和同事终于识别出了这些孩子重病的原因:一个遗传变异影响了干扰素- γ受体,这是一个多功能免疫分子,参与调控炎症[1]。之后不久,一组法国研究者发现,类似的突变还导致了另一种分歧杆菌导致的重病——这次是结核疫苗的减毒株。
那以后,研究者已经积累了数百个此类“免疫出生错误(IEI)”背后基因的突变数据库,它们使全球数百万人对许多传染病和免疫相关疾病易感,而这些疾病对大多数人不构成威胁。
个体免疫系统的差异影响他们与病原作战的能力,这一点似乎不言自明。但找到这些变异的具体原因,能够让研究者找到方法,治疗(乃至预防)一度被视作随机厄运的严重感染,比利时荷语鲁汶大学研究IEI的肿瘤学家和免疫学家Isabelle Meyts说。
这些发现已经开始改变临床实践。例如,医生可以为患者做相关突变的遗传筛查,或补充缺失的免疫因子。科学家也在持续拼凑出遗传因素影响感染疾病的多种方式——特别是在威胁生命的情况下。“我们越来越意识到,可能存在遗传因素,能够预测哪些人会产生严重的反应。”美国Montefiore Einstein医学中心研究感染性疾病的医学科学家Michael Abers说。
从细菌到宿主
19世纪路易·巴斯德推广的疾病的病原体理论是革命性的。人们意识到肉眼不可见的微生物会致病,这催生了公共卫生举措,如改善卫生、疫苗和抗菌药物,这些进展极大改善了感染患者的预后。
但即使有了这些工具,仍然有人(尤其是一些儿童和老人)会因为通常可预防和治疗的感染患病甚至死亡,这意味着在感染疾病中仅关注病原体是不够的。
20世纪50年代,一些科学家已经开始关注宿主,特别是在通常无害的微生物致病的案例中。研究者自那时起已经发现,感染易感性的一个关键决定因素可能是人的基因。
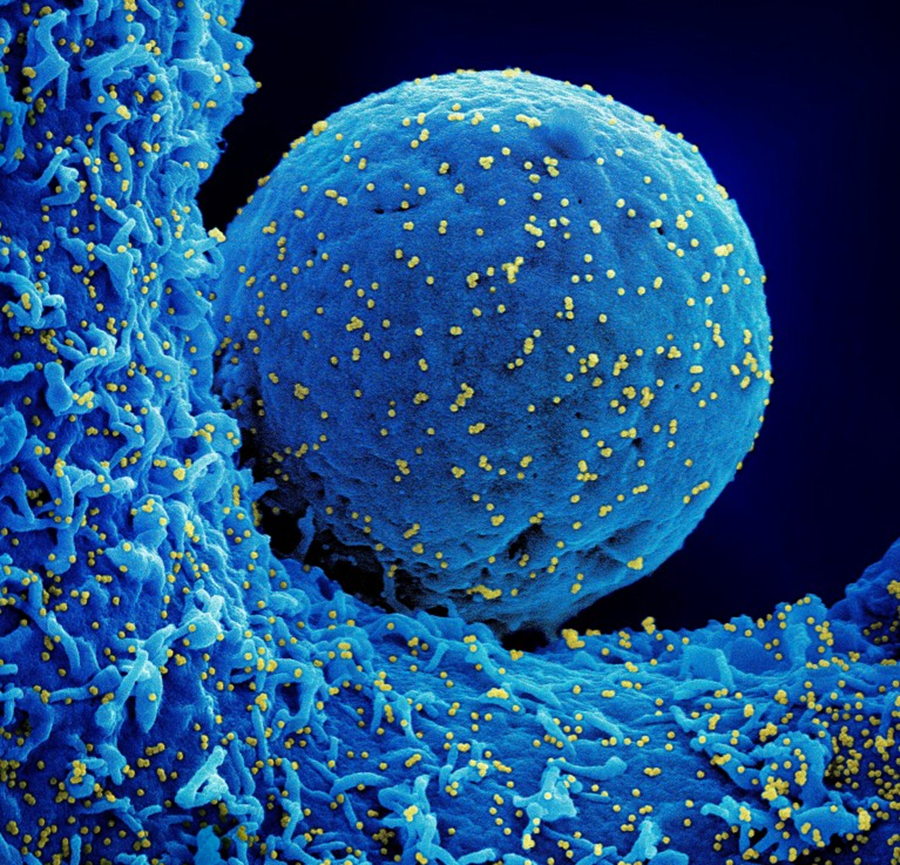
SARS-CoV-2病毒颗粒(黄)感染一个细胞(蓝)。来源:NIAID/NIH/SPL
一个著名的影响感染的遗传突变,是严重联合免疫缺陷症(SCID),这种遗传病导致患者丧失免疫系统功能,与十几个基因的突变有关。如果不加治疗,它通常会导致患儿在2岁前死亡。
好在SCID很罕见,估计50000例新生儿中仅有一例。但会导致免疫系统问题的遗传突变要常见得多。过去几十年里,研究者发现先天免疫缺陷与超过500个基因有关[3]。除了对感染性疾病的易感,这些突变还与其他免疫系统异常有关,包括自身免疫性疾病和过敏。
一些突变会削弱免疫系统,降低它与感染作战的能力。另一些会使人对感染过度响应,导致免疫反应失控,甚至危及生命。
虽然某些IEI导致患者对病原体普遍缺乏抵抗,但大多数是让人面临特定微生物的风险,如分歧杆菌、禽流感病毒、单纯疱疹病毒和脑膜炎奈瑟菌(Neisseria meningitidis)。
“每种感染都有不同的机制。”美国国立卫生研究院(NIH)的传染病专家Steven Holland说。“不同基因应对不同感染,这并不意外。目前已知的突变大多导致重症,但也有一些和反复发生的轻度感染有关。”
此外,有些基因还能增强抵抗病原的能力。例如,编码CCR5(白细胞表面的一个受体)基因的一个突变会让人能够抵抗HIV[4](但会增加西尼罗河病毒重度感染的风险)。编码FUT2(一种肠道粘膜上的蛋白质)的基因的突变,能帮助人们抵御诺如病毒,这种病毒会引发传染性很强的胃肠道感染。
病毒宇宙扩张
2020年COVID-19疫情的高峰期,人们发现有些感染者病情危重,另一些人只有一点鼻塞。美国洛克菲勒大学儿科医生和免疫学家Jean-Laurent Casanova领导的一个庞大的科学家联盟发现,有10%的重症新冠患者有自身抗体——这些异常蛋白质会攻击患者自身。这些自身抗体会攻击那些调动免疫反应的信号分子,抑制了免疫防疫[5]。
Casanova团队随后在季节性流感、西尼罗河病毒等多种疾病的重症患者群体中,以及对黄热病疫苗等疫苗产生罕见不良反应的群体中,发现了同样的自身抗体。
目前还不清楚自身抗体为何以及如何形成。包括Casanova在内的一些科学家怀疑,这可能是遗传或后天突变的结果。他和另一些研究者已经鉴别出了一些可能产生这些自身抗体的突变,如多种干扰素相关基因的缺陷。还不清楚这些突变是否就是造成这些疾病中大部分重症病例的原因。
研究者仍然在探索遗传对感染结局造成影响的复杂机制。拥有突变不总是导致某人易感:IEI的表现难以预测。许多人携带免疫缺陷相关的突变,但从来没出现症状——这一现象称为不完全外显(incomplete penetrance)。虽然大多数后果严重的IEI会在儿童期显现,但有些也可能蛰伏几十年。在一篇未发表的工作中,Meyts和她的团队发现一名患者带有炎症性疾病相关突变,但其症状只在感染了SARS-CoV-2之后才出现。
科学家仍然在探索哪些因素影响IEI的严重程度。在一项2025年的研究中,美国哥伦比亚大学的儿科免疫学家Dusan Bogunovic和同事发现,在约4%的IEI中,致病的变异在不同细胞中表达存在差异[6]。该团队还发现证据表明,这一过程可能受到表观遗传机制调控,而这受到环境因素影响——这意味着,不仅同样的IEI在不同人中表现不同,这些突变的效应也会随着同一人的生命阶段而不同。Bogunovic团队目前正在寻找能控制这些可变等位基因表达的因素,如炎症或特定的感染。
治疗与预防
影响免疫的遗传变异库已经投入使用。有越来越多的医生,在遇到严重感染患者时会要求进行基因检测,特别是在儿科重症监护室。“有太多的基因,而测序现在变得越来越可及和经济,这几乎已经成为患者入院时的首选检测。”美国加利福尼亚大学的儿科免疫学家Jennifer Puck说。“机会不容错过。”
基因检测可以为医生提供治疗方法的关键信息,例如,假如有个人携带某种变异导致缺乏特定免疫分子,就可以补充这种分子。免疫响应过度活跃的人,比如有自身抗体的人,可以通过抗炎药物治疗。而有特定免疫缺陷的人则可以通过骨髓移植来替换缺陷免疫细胞[7]。为了实现重症的长期预防,基因疗法等手段也正在兴起[8]。
理想情况下,医生能在感染失控前采取行动。过去十年,新生儿的突变筛查已经大为普及——如今也涵盖了与先天性免疫缺陷有关的基因。以SCID为例,新生儿筛查使临床医生能提供早期治疗,这极大改善了预后。
但在扩大基因筛查涵盖的突变范围时,需要考虑一些重要的问题。很多情况下,有IEI并不必然意味着某人有免疫缺陷——即使有,许多IEI目前也无法修正。“婴儿的筛查存在许多伦理问题还有情绪动力。” Puck说。“要是发现了基因变异,又不知道它是否会致病——家人要如何应对这一信息,这又将如何颠覆他们与新生儿的关系?”
Puck参与一个专项小组,致力于确定哪些变异应纳入BEACONS项目(美国一项大规模新生儿基因组筛查试验)。“我们真正关注的是那些如果有突变,能在新生儿第一年里干预的基因。”
预测
遗传因素研究在多大程度上能帮助我们识别感染病高风险人群?一些专家如Casanova 和Meyts认为,大多数严重感染的病例都是缺陷所致,通常有着遗传起源,这些缺陷影响了免疫系统,来自先天或随着生命进程在细胞中后天获得。事实上,Casanova提出了“完全宿主理论”:他认为微生物只是潜在免疫缺陷的环境诱因,就像花生了引发花生过敏。他认为,在那些因感染死亡的人中,疾病根源远早于接触病原体之前就存在于体内了。
然而,其他人指出,遗传仍只能解释很少一部分病例[9],其他因素[10]如患者的病史、环境和致病微生物的特性等也非常重要。“毫无疑问,遗传对感染的结局有着重大作用,但这不是唯一的答案。” Holland说。病原体基因组也会作出适应好感染宿主。“感染性疾病的深奥之处,在于至少存在两个平行演化的基因组。”他补充说。
一些研究者,如德国弗莱堡大学的儿科免疫学家Philipp Henneke,认为研究早期免疫发育将有助于揭示:是什么让有些人日后会对感染性疾病易感。Henneke参与了德国的“免疫细胞拓扑学围产期发展(PILOT)”项目,该项目旨在追踪婴儿在妊娠期、出生及生命头几周中的免疫系统发育。该项目包括了十多个研究项目,旨在解析从昼夜节律到早期感染等所有因素的作用。
终极目标在于,使用遗传和其他因素来预测一个人会对感染作何反应。此刻这个目标还遥不可及。
“从遗传学角度,你或许能发现一些风险,但说到底了我们无法确定。我们有的只是概率。”美国约翰斯·霍普金斯大学的微生物学家、免疫学家Arturo Casadevall说。“作为感染性疾病医生,我见过18岁身体倍棒的患者因流感去世。这个人与别人不同在哪里?我们不知道。”
参考文献:
Newport, M. J. et al. N. Engl. J. Med. 335, 1941–1949 (1996).
Jouanguy, E. et al. N. Engl. J. Med. 335, 1956–1962 (1996).
Poli, M. C. et al. J. Hum. Immun. 1, e20250003 (2025).
O’Brien, S. J. Proc. Natl Acad. Sci. USA 121, e2321907121 (2024).
Bastard, P. et al. Science 370, eabd4585 (2020).
Stewart, O. et al. Nature 637, 1186–1197 (2025).
Cheminant, M. et al. Blood 141, 60–71 (2023).
Booth, C. et al. N. Engl. J. Med. 393, 1486–1497 (2025).
Carlsson, F. & Råberg, L. Proc. Natl Acad. Sci. USA 121, e2319605121 (2024).
Casadevall, A. & Pirofski, L.-A. Infect. Immun. 86, e00636‑17 (2018).
原文以The infection enigma: why some people die from typically harmless germs标题发表在2026年1月14日《自然》的新闻特写版块上
© nature
Doi:10.1038/d41586-026-00082-1
点击阅读原文查看英文原文
往期精彩文章


版权声明:
本文由施普林格·自然上海办公室负责翻译。中文内容仅供参考,一切内容以英文原版为准。欢迎转发至朋友圈,如需转载,请邮件China@nature.com。未经授权的翻译是侵权行为,版权方将保留追究法律责任的权利。
© 2026 Springer Nature Limited. All Rights Reserved
星标我们🌟,喜欢就点亮小爱心哦!
